LYS KİMYA YT.indd
advertisement

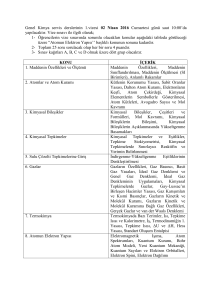
KAZ AN Test 3 1. Baş (birincil) kuantum sayısı (n) ile ilgili; KİMYA 4. Aşağıdaki sınır yüzey diyagramlarından hangisi, , = 2 açısal momentum kuantum sayısına sahip orbitale ait değildir? I. Elektronun çekirdekten uzaklığını ifade eder. II. Elektronun temel enerji düzeyini gösterir. A) III. Elektronun enerjisini ifade eder. 12 - B KAVRAMA STİ TE Modern Atom Teorisi – 3 IM z yargılarından hangileri doğrudur? A) Yalnız I y x B) Yalnız II D) II ve III z B) y x C) I ve II E) I, II ve III C) z D) y z y x x 2. Bir orbitalin uzaydaki yönlenmesini gösteren kuantum sayı- sına ...............I.................. orbitalin şeklini açıklayan kuantum sayısına .................II.................. denir. z y Yukarıdaki cümlede I ve II numaralı boşluklara aşağıdakilerden hangisi gelmelidir? I A) B) C) D) E) x II Baş kuantum Manyetik kuantum sayısı sayısı İkincil kuantum Açısal momentum sayısı kuantum sayısı Manyetik kuantum Spin kuantum sayısı sayısı Manyetik kuantum İkincil kuantum sayısı sayısı Açısal momentum Manyetik kuantum kuantum sayısı sayısı MEB 2016 - 2017 E) 5. n , m, I.3 2 0 II.2 2 +2 III.41-2 Yukarıdaki öncüllerde bulunan kuantum sayısı setlerinden hangileri mümkün değildir? A) Yalnız I B) Yalnız II D) II ve III C) Yalnız III E) I, II ve III 6. Defne; orbitallerin enerjileri ile ilgili yaptığı bir ödevde şu cümleleri kullanıyor. 3. Orbital n , m, 2s 2 1 1 3p 3 1 –1, 0, +1 3d 3 2 –2, –1, 0, +1, +2 4p 4 2 –1, 0, +1 4d 3 2 –1, 0, +1 I. 4f orbitalinin enerjisi 6s orbitalinden büyüktür. II. Orbitallerin enerjileri (n + ,) değerleri ile orantılıdır. III. n + , değerleri eşit olan orbitallerden n değeri büyük olanın enerjisi büyüktür. IV. Tek elektronlu taneciklerde aynı temel enerji düzeyine sahip orbitallerin enerjileri eşittir. V. Elektronlar orbitallere önce düşük enerjili orbitalleri Yukarıda verilen kuantum sayıları yazılırken kaç tane kutucukta hata yapılmıştır? A) 4 B) 5 C) 6 D) 7 E) 8 doldurarak yerleşirler. Bu cümlelerden kaç tanesi doğrudur? A) 5 B) 4 C) 3 D) 2 E) 1 12 - B Test 3 KİMYA Modern Atom Teorisi – 3 10.I.12Mg2+ – 8O2– 7. Elektron dağılımında temel halde 7 tane tam dolu orbitali bulunan nötr X atomu için; 2+ II. 20Ca – 22Ti I. Paramanyetiktir. 3+ III. 18Ar – 21Sc II. Küresel simetriktir. III. 14 tane elektronu vardır. ifadelerinden hangisi doğrudur? A) Yalnız I B) Yalnız II D) I ve II Yukarıdaki tanecik çiftlerinden hangileri izoelektroniktir? A) Yalnız I B) Yalnız II D) II ve III C) Yalnız III C) I ve III E) I, II ve III E) I, II ve III 11. 29Cu atomunun temel hal elektron dağılımı yapıldığında n + , değeri 4 olan orbitallerde kaç tane elektron bulunur? 8. Temel hal elektron dağılımı 3d10 ile sona eren nötr X I. Küresel simetriktir. II. 15 tane tam dolu orbitali vardır. III. En büyük baş kuant sayısı 4’tür. A) 1 MEB 2016 - 2017 atomu için; B) 2 C) 7 D) 11 E) 17 ifadelerinden hangisi kesinlikle doğrudur? A) Yalnız I B) Yalnız II D) I ve II C) Yalnız III E) I ve III 12. Deniz, yaptığı bir ödevde 24Cr atomunun temel hal elektron dağılımı için; I. [Ar] 4s2 3d4 şeklindedir. II. Küresel simetrik değildir. 9. Açısal momentum kuantum sayısı (,) için; I. Orbitallerin şekillerini açıklar. II. Alacağı değerler başkuantum sayısına bağlıdır. III. , = 3 değeri f orbitaline karşılık gelir. IV. En büyük baş kuant sayısı 4’tür. ifadelerini kullanıyor. Buna göre bu ifadelerin doğru (D) veya yanlış (Y) oluşu aşağıdaki seçeneklerden hangisinde doğru verilmiştir? yargılarından hangileri doğrudur? A) Yalnız I B) Yalnız II D) II ve III KAVRAMA IM STİ TE KAZ AN III. Paramanyetiktir. A) D, D, D, D C) I ve II B) Y, Y, D, D D) Y, D, D, Y E) I, II ve III 1 2 3 4 5 6 7 C) D, D, Y, Y E) Y, D, Y, D 8 9 10 11 12 Adı :......................................................... Doğru :..................................... Soyadı :......................................................... Yanlış :..................................... Sınıf :......................................................... Boş No :......................................................... :..................................... Puan :..................................... E E E E E E E E E E E E