FEN VE
TEKNOLOJİ
1.
3.
3
A
4
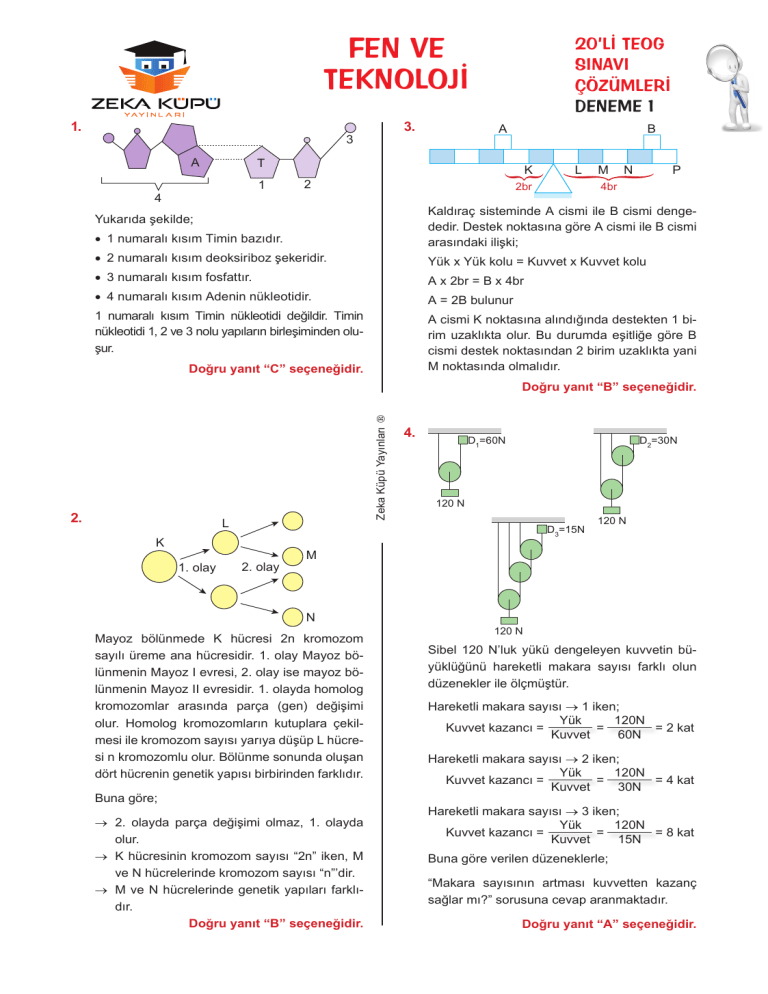
Yukarıda şekilde;
• 1 numaralı kısım Timin bazıdır.
• 2 numaralı kısım deoksiriboz şekeridir.
• 3 numaralı kısım fosfattır.
• 4 numaralı kısım Adenin nükleotidir.
1 numaralı kısım Timin nükleotidi değildir. Timin
nükleotidi 1, 2 ve 3 nolu yapıların birleşiminden oluşur.
Zeka Küpü Yayınları Ò
L
2. olay
N
P
4br
Kaldıraç sisteminde A cismi ile B cismi dengededir. Destek noktasına göre A cismi ile B cismi
arasındaki ilişki;
Yük x Yük kolu = Kuvvet x Kuvvet kolu
A x 2br = B x 4br
A = 2B bulunur
A cismi K noktasına alındığında destekten 1 birim uzaklıkta olur. Bu durumda eşitliğe göre B
cismi destek noktasından 2 birim uzaklıkta yani
M noktasında olmalıdır.
Doğru yanıt “B” seçeneğidir.
4.
D1=60N
D2=30N
120 N
D3=15N
K
M
120 N
M
N
L
2br
Doğru yanıt “C” seçeneğidir.
1. olay
B
K
2
A
T
1
2.
20’Lİ TEOG
SINAVI
ÇÖZÜMLERİ
DENEME 1
Mayoz bölünmede K hücresi 2n kromozom
sayılı üreme ana hücresidir. 1. olay Mayoz bölünmenin Mayoz I evresi, 2. olay ise mayoz bölünmenin Mayoz II evresidir. 1. olayda homolog
kromozomlar arasında parça (gen) değişimi
olur. Homolog kromozomların kutuplara çekilmesi ile kromozom sayısı yarıya düşüp L hücresi n kromozomlu olur. Bölünme sonunda oluşan
dört hücrenin genetik yapısı birbirinden farklıdır.
120 N
Sibel 120 N’luk yükü dengeleyen kuvvetin büyüklüğünü hareketli makara sayısı farklı olun
düzenekler ile ölçmüştür.
Hareketli makara sayısı → 1 iken;
Yük
120N
Kuvvet kazancı =
=
= 2 kat
Kuvvet
60N
Hareketli makara sayısı → 2 iken;
Yük
120N
Kuvvet kazancı =
=
= 4 kat
Kuvvet
30N
Buna göre;
→ 2. olayda parça değişimi olmaz, 1. olayda
olur.
→ K hücresinin kromozom sayısı “2n” iken, M
ve N hücrelerinde kromozom sayısı “n”’dir.
→ M ve N hücrelerinde genetik yapıları farklıdır.
Doğru yanıt “B” seçeneğidir.
Hareketli makara sayısı → 3 iken;
Yük
120N
Kuvvet kazancı =
=
= 8 kat
Kuvvet
15N
Buna göre verilen düzeneklerle;
“Makara sayısının artması kuvvetten kazanç
sağlar mı?” sorusuna cevap aranmaktadır.
Doğru yanıt “A” seçeneğidir.
2. DÖNEM
TEOG
DENEME 1
5.
Fen ve Teknoloji
1
Adet
Kanaması
4
Kasların
Gelişmesi
7
2
Sesin
Kalınlaşması
5
Göğüslerin
Belirginleşmesi
8
Koltukaltı
Kıllanması
Boy
Uzaması
8.X → 2. periyot 3 A grubunda
3
Sperm
Üretimi
6
Sivilce
Oluşumu
9
Ter Bezlerinin
Aktif Hale
Gelmesi
Sadece Kızlarda
Görülenler
1 Adet kanaması
2 Sesin kalınlaşması
5 Göğüslerin 3 Sperm Üretimi
belirginleşmesi
Y → 3. periyot 4A grubunda
Z → 4. periyot 5 A grubunda
3A
3. periyot
Sadece Erkeklerde
Görülenler
4A
Y
5A
Z
Doğru yanıt “B” seçeneğidir.
9.
•
•
•
•
•
6.
A
4
3
5
x
7
6
y
x yönünde dönenler
1 - 3 - 5 - 7
4 tane dişli
y yönünde dönenler
2-4-6
•
•
•
••
•
•
Z
X → 2 katmanı vardır. 2. periyotta bulunur. Son
yörüngesinde 2 elektronu vardır. 2A grubunda yer alır.
Y → 1 katmanı vardır. 1. periyotta bulunur. Son
yörüngesinde 1 elektoronu vardır. 1A grubunda yer alır.
Z → 2 katmanı vardır. 2. periyotta bulunur. Son
yörüngesinde 7 elektronu vardır. 7A grubunda yer alır.
3 tane dişli
Doğru yanıt “C” seçeneğidir.
Zeka Küpü Yayınları Ò
2
1
•
•
Y
X
X
4. periyot
Doğru yanıt “B” seçeneğidir.
2. periyot
X
2A
Y
Z
1A 7A
Doğru yanıt “B” seçeneğidir.
7. Görüş
Bilim İnsanı
10.Y3 Z bileşiği kovalent bağlı ise;
Periyodik Sistemi
atom numaralarına
göre düzenlemiştir.
Y → ametal
Gilen Siborg
Periyodik sistemin
en altında yer alan
iki sıra halindeki
elementleri düzenleyerek periyodik
sisteme son şeklini
vermiştir.
Elementleri atom
ağırlıklarına göre
sıralamıştır.
Oluşturduğu tablo
12 satır ve 8 sütundan oluşmaktadır.
Z → ametal
XY2 bilesiği iyonik bağlı ve Y ametal ise
X → metal
Henry Moseley
Dimitri Mendeleyev
Doğru yanıt “B” seçeneğidir.
X ile Z arasında kovalent bağlı bileşik oluşmaz. Çünkü X metal, Z ametaldir.
X metal, Y ametaldir.
Z elementi elektirik ve ısıyı iletemez çünkü X
ametaldir.
Y3 Z bileşiği kovalent bağlık bileşik olduğu için
elektron ortaklaşması ile bağ kurulmuştur.
Doğru yanıt “A” seçeneğidir.
2. DÖNEM
TEOG
DENEME 1
Fen ve Teknoloji
11.
•
•
•
1p
2p
3p
H
He
•
•
•
14.
Turnusol
Kağıdı
Turnusol
Kağıdı
X çözeltisi
Y çözeltisi
Li
He → 1A grubunda ametal
He → 8A grubunda soygaz
Li → 3A grubunda metal
H ve Li arasında iyonik bağ oluşur. (Doğru)
H ile Li arasında bağ oluşur.
He ile Li arasında bağ oluşmaz.
H ile He arasında bağ oluşmaz.
Doğru yanıt “A” seçeneğidir.
Turnusol kâğıdı asit çözeltisinde kırmızı renge
dönüşür, baz çözeltisinde ise mavi renge dönüşür.
Bu yüzden X çözeltisi asit, Y çözelitisi ise bazdır.
X’in pH’ı 7’den küçüktür.
Y’nin tadı acıdır.
X ile Y nötralleşme tepkimesi verir. (Doğru)
Y’nin pH değeri 7’den büyüktür.
12. Limon kuvvetli bir asit olduğu için pH değeri 0-7
arasında 0’a daha yakındır.
Kabartma tozu zayıf bir baz olduğu için pH değeri 7-14 arasında 7’ye daha yakındır. Bu nedenle;
1 2 3 4 5 6 7 8 9 10 11 12 13 14
Limon
Zeka Küpü Yayınları Ò
Doğru yanıt “C” seçeneğidir.
Kabartma
Tozu
Doğru yanıt “D” seçeneğidir.
15. K gazı
L gazı
13. 1A
8A
H
Li Be
3A 4A 5A 6A 7A
Asit
çözeltisi
Baz
çözeltisi
K gazı asit çözeltisi ile nötralleşme tepkimesi
verdiğine göre K gazı baziktir.
I. H ve Li elementlerinin son yörüngesinde
1e- vardır.
L gazı baz çözeltisi ile nötralleşme tepkimesi
verdiğine göre L gazı asidiktir.
II. Li ve Be elementlerinin katman sayısı eşittir
ve 2 katmanları vardır.
III. H’nin proton sayısı 1’dir.
Li’nin proton sayısı 3’tür.
Be’nin proton sayısı 4’tür.
K gazı bazik olduğu için pH değeri 7’den büyüktür.
L gazı asidik olduğu için çözeltisine H+ iyonu
Yukarıda verilen elementlerle ilgili;
Be’nin proton sayısı en büyüktür.
Doğru yanıt “D” seçeneğidir.
verir. (Doğru)
K gazı bazik olduğu için turnusol kağıdını mavi
renge dönüştürür.
Doğru yanıt “C” seçeneğidir.
2. DÖNEM
TEOG
DENEME 1
Fen ve Teknoloji
16. Kimyasal tepkimeye ait tanecik modeli şekilde-
19. Bir maddenin oksijen gazı ile tepkimeye gire-
ki gibidir.
rek yeni bir ürün meydana getirdiği tepkimelere
yanma tepkime denir.
+
Buna göre;
Girenler ve ürünler kısmında bulunan atom
sayısı 3 olup korunmuştur.
Atom sayısı korunduğu için kütle de korunmuştur.
Giren maddeler kendi özelliklerini kaybedip
yeni madde oluşmuştur.
Yeni atom oluşmamıştır.
H2O → H2 + 1/2 O2 (Bu tepkimede su bileşenlerine ayrılmıştır. Yanma tepkimesi değildir.)
HCl + NaOH → NaCl + H2O (Bu tepkimede
asit ve baz tepkimeye girip tuz ve su oluşmuştur. Bir nötralleşme tepkimesidir.)
CH4 + 2O2 → CO2 + 2H2O (Bu tepkimede CH4
oksijen gazı ile tepkimeye girip karbondioksit ve
su oluşmuştur. Bir yanma tepkimesidir.)
Zn + 2HCl → ZnCl2 + H2
(Metallerin asit ile
tepkimesidir. Hidrojen gazı açığa çıkıp tuz oluşmuştur.)
Doğru yanıt “C” seçeneğidir.
dır.
Y → elektron vermeye yatkın olan element metaldir.
Zeka Küpü Yayınları Ò
17. X → soygaz grubunda bir element olup kararlı-
Doğru yanıt “C” seçeneğidir.
Z → mat görümünlü olan element ametaldir.
Doğru yanıt “A” seçeneğidir.
20. Havada bulunan CO2, SO2 ve NO2 gibi atık gazOksijen
gazı
Yanıcı
Yakıcı
Söndürücü
Yukarıda verilen kimyasal tepkimeye göre yanıcı olan hidrojen gazı ile yakıcı olan oksijen
gazında oluşan su bileşiği (H2O), bileşenlerden
farklı olarak söndürücü özellik göstermektedir.
ların su buharı ile birleşimi sonucu asit yağmur-
Su
{
+
{
Hidrojen
gazı
{
18.
Yukarıda verilen bu bilgilerle kimyasal tepkime
sonucunda farklı özelliklerde yeni maddeler
oluştuğu sonucuna ulaşılır.
Doğru yanıt “D” seçeneğidir.
ları oluşur.
Asit yağmurlarına aktif yanardağ, fabrikalar ve
motorlu araçlardan çıkan gazlar neden olur.
Asit yağmurları yeryüzünde bitki örtüsüne zarar
verir. Su kaynaklarının kirlenmesine sebep olup
suda yaşayan canlılar olumsuz etkiler. Ayrıca,
yeryüzünde bulunan tarihi ve doğal yapıtların
zarar görmesine neden olur. İnsanlarda ise solunum yolları rahatsızlıklarına neden olur.
Doğru yanıt “D” seçeneğidir.