www.kimyafull.com
PERİYODİK SİSTEM VE ELEKTRON DİZİLİMLERİ#6
www.kimyafull.com
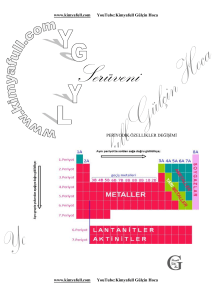
Periyodik sistemde yatay sıralara ………………
Düşey sütunlara ………….. adı verilir.
1.periyotta ……………… element,
2 ve 3. periyotlarda …………..element,
4 ve 5.periyotlarda ……………….element
6 ve 7. periyotlarda ise ……………….element bulunur.
Periyodik sistemde gruplar,……….tane A ve…….tane B olmak üzere
……………….. tanedir.
Sütunların sayısı ise ………….dir. Bu ………… sütun, yeni bir yaklaşım
olarak IUPAC (Uluslararası Temel ve Uygulamalı Kimya
Birliği)önerisinde ise 1’den ………….e kadar sırayla numaralandırılır.
s blok ile p-blok elementleri arasında bulunan d-blok elementleri,geçiş
elementleri olarak adlandırılır.
İç geçiş elementleri olarak da adlandırılan f-blok elementleri periyodik
sistemde alt kısma yerleştirilmiştir. İki sıra hâlinde düzenlenmiş olan fbloku elementlerinden ilk sıradakilere ……………, ikinci sıradakilere ise
…………………………….denir.
Bir elementin, elektron dizilişinde en büyük baş kuantum sayısı periyot
numarasına eşittir.
Elementlerin en dış katmanındaki elektron dizilişleri elementin blokunu ve grup
numarasını belirler.
Buna göre elektron dizilimi
s ile bitenler s blokta,
p ile bitenler p blokta,
d ile bitenler d blokta yer alır (f-bloku bu kurala uymaz.).
s ve p-bloku elementleri A grubunu,
d ve f-bloku elementleri de B grubunu oluşturur.
www.kimyafull.com
Grup 1A’dan grup 7A’ya kadar olan bütün elementler baş (ana) grup elementleri
olarak da adlandırılır.
8A grubu elementleri soy gazlardır (Elektron dizilişi helyum için 1s2, diğer soy gazlar
için ns2np6 dır. n ise en dış kabuğun baş kuantum sayısını göstermektedir.).
Geçiş metalleri 3B’den 2B’ye kadar olan elementlerdir.
www.kimyafull.com
PERİYODİK CETVELDE YER BULMA:
7N
s
16
20Ca
24Cr
29Cu
33As
35Br
Atom Numarası Bulma:
4.periyot 5A grubu:
3.periyot 7A grubu:
4.periyot 7B
www.kimyafull.com
PERİYODİK
ÖZELLİKLER
Kovalent Yarıçapı
Kovalent yarıçap,tek bir kovalent bağla bağlanmış eş değer iki atomun çekirdekleri
arasındaki uzaklığın yarısıdır.
Van der Waals Yarıçapı
Soy gazlar yüksek basınç ve düşük sıcaklıkta katı hâle gelir. Bunları katı hâlde bir arada tutan
kuvvetler Van der Waals kuvvetleridir. Katı hâlde soy gazlar için hesaplanacak yarıçapa Van
der Waals yarıçapı denir
www.kimyafull.com
İYONİK YARIÇAP
Metal atomu ile ametal atomu arasında oluşan iyonik bileşikteki bir katyonun ya da anyonun
yarıçapına iyonik yarıçap denir
İzoelektronik (eş elektronlu) iyonlarda, çekirdek yükü büyük olanın yarıçapı daha küçüktür
ÖRNEK:
ÖRNEK:
www.kimyafull.com
METALİK VE AMETALİK
Periyodik sistemdeki elementlerin büyük çoğunluğu metaldir ve metallerin
endüstride kullanımı çok önemlidir. s, d ve f bloklarında bulunan bütün
elementler metaldir (1H hariç). p-blokunun ise bazı elementleri(AI, Ga, In, Sn,
TI, Pb ve Bi) metal özelliktedir.
Bir periyotta soldan sağa doğru elementlerin elektron vermesi
zorlaşacağından elektron alma eğilimi artmaya başlar. Buna göre periyodik
sistemde metaller sol tarafta, ametaller ise sağ tarafta toplanmıştır
(1H hariç). 3. periyot elementlerinin metal ve ametal özelliklerini
incelendiğimizde Na, Mg ve AI elementlerinin metal; Si’un yarı metal; P, S ve
CI elementlerinin ise ametal özellikte olduğu görülür.
Aynı grupta ise yukarıdan aşağıya doğru metalik özellik artarken ametalik
özellik azalır.
Aynı gruptaki elementlerin aşağıya doğru enerji katman sayıları artar ve buna
bağlı olarak atomun çapı büyür.
Çekirdeğin, en dışta bulunan elektronları çekebilme yeteneği zayıflar. Buna
göre bir grupta yukarıdan aşağıya doğru elementlerin elektron verebilmesine
bağlı olan metal özelliği artarken, elektron alabilmesine bağlı olan ametal
özelliği azalır.
Periyodik sistemin 4A grubunda bu durum çok açıktır. Grupta
C ametal, Si ve Ge yarı metal, Sn ve Pb ise metalik özellik gösterir.
İYONLAŞMA
ENERJİSİ
Gaz hâlde bulunan nötr bir atomdan bir elektronun
uzaklaştırılması için verilmesi gereken bu enerjiye iyonlaşma enerjisi denir.
www.kimyafull.com
Bir periyotta, birinci iyonlaşma enerjilerinin soldan sağa doğru arttığı yönde
bazı istisnalar vardır.
Birinci istisna, aynı periyottaki grup 2A ile grup 3A arasındadır. Grup 2A
elementleri, grup 3A elementlerinden daha yüksek iyonlaşma enerjisine
sahiptir.
İkinci istisna ise grup 5A ve 6A arasındadır.
O hâlde periyodik sistemin aynı periyodunda iyonlaşma enerjisi değişimi,
1A < 3A < 2A < 4A < 6A < 5A < 7A < 8A
www.kimyafull.com
Elektron İlgisi
Gaz hâlindeki bir atomun bir elektron alarak anyon oluşturması sırasındaki
enerji değişimine elektron ilgisi denir.
F(g) + e– F–(g) E İ = –328,2 kJ/mol
Yukarıdaki tepkimede bir elektron, flor atomunun + yüklü çekirdeği tarafından
çekileceği için atom, negatif iyon durumuna geçer ve reaksiyon ekzotermiktir.
Bir periyotta soldan sağa gidildikçe elektron ilgisi yani elektron alma eğiliminde
artış gözlenmektedir.
Halojenler (7A) en yüksek elektron ilgisine sahiptir.
Bir grupta, yukarıdan aşağıya doğru elektron ilgisi azalır.
ELEKTRONEGATİFLİK
Elektronegatiflik bir atomun, ortak olduğu kimyasal bağdaki elektronu çekme gücünün bir
ölçüsü olarak ortaya atılmıştır.
Elektronegatiflik değerleri 0,7 ile 4,0 arasında değişir
En çok elektronegatif elementler flora yakın olanlar, en az elektronegatif elementler de
fransiyuma yakın olanlardır.
Elektronegatiflikler arasındaki fark büyüdükçe bağın sağlamlığının arttığı görülmüştür.
Örneğin H – F için fark 1,9 iken C – H bağının elektronegatiflik farkı 0,4’tür.
elektronegatiflik farkı arttıkça bağın iyonik karakteri artar.
Önemli not:
www.kimyafull.com
Periyodik Sistemde Elementlerin Asitlik ve Bazlık Özelliklerinin Değişimi
Oksitler, suda çözündüklerinde H+ veya OH– iyonu derişimlerini artırmalarına göre asidik ya da bazik
olarak sınıflandırılır. Bazı oksitler ise hem asidik hem de bazik özellik gösterdiklerinden amfoterdir
1- Na2O suda çözündüğünde bir baz olan sodyum hidroksidi oluşturur:
2- MgO suda az çözülür. Ancak asitlerle nötrleşme reaksiyonu verir
3- Al2O3 asitlere karşı baz, bazlara karşı da asit özellik gösterir yani amfoterdir:
4- Si yarı metaldir. Oksidi (SiO2) üç boyutlu ağ yapısına sahiptir. SiO2 çok derişik bazlarla reaksiyona
girdiği için zayıf asidik özellik taşır
5- P4O10, SO3 ve Cl2O7 moleküler bileşiktir ve asidik özellik gösterir. Bu bileşikler, sırasıyla suyla
reaksiyona
girdiklerinde fosforik asit (H3PO4), sülfürik asit (H2SO4) ve perklorik asit (HCIO4) oluşturur
www.kimyafull.com
Gruplarda ise elementlerin metalik karakteri yukarıdan aşağıya doğru arttığından atom yarıçapı
büyük olan elementlerin küçük olanlara göre oksitlerinin daha bazik olduğu söylenebilir
7A grubu elementlerinin oksitlerinden OCI2 , OBr2 ve OI2 incelendiğinde en fazla asidik özellik
gösterenin OCl2, en az asidik özellik gösterenin ise OI2 olduğu görülür.