106 HASTANE KÖKENLİ PNÖMONİLER Prof.Dr
advertisement

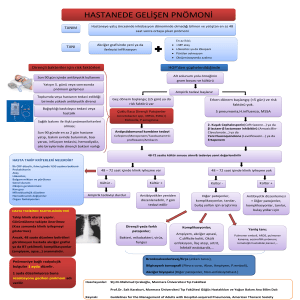
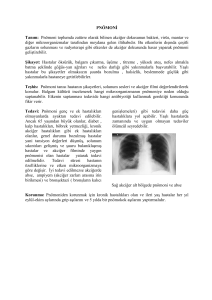
HASTANE KÖKENLİ PNÖMONİLER Prof.Dr.Eyüp Sabri Uçan Hastane kökenli pnömoni(HKP), hastaneye herhangi bir bedenle yatıştan en az 48 saat sonra yada çıktıktan sonraki ilk 48 saatte gelişen pnömonileri tanımlar. HKP’nin önemli bir alt grubu da entübasyonu, invaziv mekanik ventilasyonu izleyerek ortaya çıkan ventilatörle ilişkili pnömonidir(VİP). ABD verileri 1000 yatışta 5-20 oranında saptandığını ancak mekanik ventilatör uygulanan olgularda sıklığın 6-20 kat arttığını ortaya koymaktadır. Hastanede geçirilen günler arttıkça kolonize olan ve giderek pnömoniye yol açan bakterilerin de niteliği değişmekte ilk günlerde saptanan Gram pozitif etkenler yerlerini Gram negatif etkenlere bırakmakta ve doğaldır ki mortalite oranları da % 30 - 70’lere ulaşmaktadır(1,2). Ülkemizden Akalın’ın 163 olguluk serisinde HKP görülme sıklığı %1.4 ( yoğun bakımlarda %9.5, diğer kliniklerde %0.5) ve mortalite oranı da %45 olarak bildirilmiştir(3). HKP, patogenezinde temel unsur orofaringeal sekresyonların mikroaspirasyonudur. Hastanede yatan kişide başlangıçta orofarinkste Gram pozitif etkenler kolonize iken giderek hastane florasından etkilenerek dirençli Gram negatifler ve metisiline dirençli S. aureus kolonize olur. Hastada hastaneye yatışı gerektiren ileri yaş, nörolojik problemler, bilinç kaybı gibi çok sayıda durum ise mikroaspirasyona yol açar. İnhalasyon yolu ise daha çok kontamine solunumsal cihazlardan kaynaklanır. İnfekte nebülizatörler, ventilatörler ve devreleri, nemlendiriciler HKP gelişimine yol açabilir. Özefagus ve gastrik içeriğin aspirasyonu, hematojen yol, komşuluk yolu ile plevral bir infeksiyonun akciğere ulaşması da söz konusu olabilir. HKP patogenezinde çok önemli yer tutan bir diğer mekanizma da entübe hastalarda bakımı üstlenen personelin el yıkama alışkanlığının olmaması nedeni ile direk bakteri inokülasyonudur. HKP patogenezinde kolaylaştırıcı faktörlerin diğer bir deyimle risk faktörlerinin neler olduğu bir çok araştırmada incelenmiş ve ortaya konmuştur (Tablo 1, 2, 3). Genel kabul gören kriterler ise; 48 saatten daha uzun süren mekanik ventilatör uygulanımı, antibiyotik kullanımı, yoğun bakımdaki ve hastanedeki yatış süresi, altta yatan hastalığın şiddeti(APACHI skoru) ve ARDS varlığıdır(2). Tablo 1. HKP gelişimine yol açan risk faktörleri ve göreceli risk oranları(4) risk faktörü göreceli risk oranı p Solunum yetmezliği 2.7 0.032 Yoğun alkol alımı 1.93 0.03 KOAH 1.92 0.02 Hava yolu girişimleri 2.67 0.04 Gastrik içeriğin aspirasyonu 5.33 <0.0001 Cerrahi girişim 1.66 0.0058 Mekanik ventilasyon 2.45 0.06 Nemlendirme sistemleri 2.25 0.02 Trakeostomi 3.05 0.04 PEEP 1.96 0.03 Reentübasyon 7.4 <0.0001 MV süresi > 3 gün 1.94 0.013 Hastane kökenli pnömoni tanısı; akciğer grafisinde başka bir nedenle açıklanamayacak yeni bir infiltrasyon varlığına eşlik eden 38°C’yi aşan ateş, 10000/mm3 aşan lökositoz, balgam veya solunumsal sekresyonların pürülansı yada bu materyallerde her sahada en az 25 nötrofil görülmesi kriterlerinden birinin varlığı ile konulur(5). Hastane kökenli pnömoniler, pnömoninin geliştiği güne göre etken spektrumunda değişiklik gösterir. Bu nedenle erken ve geç hastane kökenli pnömonilerden söz etmek olasıdır. 48-96.saat arasında (ilk 4 gün) gelişen pnçömoniler “erken hastane kökenli pnömoni”lerdir ve burada saptanan kor etkenler: Haemophilus influenzaei Streptococcus pnemoniae metisiline duyarlı Staphyloccus aureus’ tur. “Geç hastane kökenli pnömoni” tanımı 5.günden daha geç olarak gelişen pnömonileri kapsar, saptanan etkenler ise : 106 Pseudomonas aeriginosa, Enterobacteriaseae, Acinetobacter baumannii, Stenotrophomonas maltophilia gibi aerobik Gram negatif bakteriler ve metisiline dirençli Staphylococcus aureus’ tur(1,2). Tablo 2. HKP gelişimine yol açan risk faktörleri ve göreceli risk oranları(5) risk faktörü Kronik akciğer hastalığı Bilinç bozukluğu Entübasyon Büyük volümlü aspirasyon Torako-abdominal cerrahi Yaş > 70 göreceli risk oranı 3.7 5.8 6.7 10.6 4.7 2.3 p 0.0003 0.0002 0.0001 0.0003 0.0018 0.04 Tablo 3. Yoğun bakımda HKP gelişimine yol açan risk faktörleri ve göreceli risk oranları (EPIC çalışması) (6) risk faktörü Yoğun bakımda kalınan süre (gün) 1-2 3-4 5-6 7-13 14-20 > 21 PA kateterizasyonu CVP Stress ülseri profilaksisi Üriner kateterizasyon Mekanik ventilasyon Travmalı olgu göreceli risk oranı 2.54 8.99 15.01 30.75 60.4 76.06 1.20 1.35 1.38 1.41 1.75 2.07 Klinik gidişi, empirik tedavi yaklaşımını, mortaliteyi belirleyen bir diğer unsurda pnömoninin ciddiyetidir. “Ciddi hastane kökenli pnömoni” tanımı ile pnömoninin yoğun bakımda izlenmeyi gerektirmesi, mekanik ventilatör tedaviyi gerektirecek kadar ağır solunum yetmezliği, PaO2/FiO2 oranının 200’ün altında olması, hızlı radyolojik progresyon, multilobar yada kaviter radyolojik görünüm, sepsis yada septik şok varlığı kriterlerinden en az birisinin bulunduğu durum olarak kabul edilir(Tablo 4)(1,7,8). HKP kavramı ile iç içe geçen ve hemen değerlendirilmesi gereken bir başka durum da “çoğul dirençli bakteriler” dir. KOAH veya bronşektazi gibi yapısal akciğer hastalığı varlığı, antibiyotik kullanımı, kortikosteroid kullanımı, 6 günü aşan invaziv mekanik ventilatör uygulanması çoklu ilaç direnci olan bakterilerin seçilmesini, kolonize olmalarını ve dominant hale gelmeleri sürecine yol açarlar. Sonuçta MRSA, Acinetobacter baumanii, Klebsiella pneumoniae, Pseudomonas aeriginosa sorun bakteriler olarak seçilirler(Tablo 5)(8). Tablo 4: Ciddi hastane kökenli pnömoni (7,8,9) Yoğun bakım gerektirmesi / yoğun bakımda gelişmesi Solunum yetmezliği (PaO2/FiO2 < 200 ) Grafide multilobar, kaviter infiltrasyon yada hızlı progresyon Hipotansiyon yada uç organ disfonksiyonu ile birlikte seyreden ciddi sepsis varlığı: şok < 90 / 60 mmHg dört satten fazla vazopressör gerektirmesi üriner debinin saatte 20 ml, 4 saatte 80 ml’den daha az olması dializ gerektiren akut böbrek yetmezliği 107 Tablo 5: Hastane kökenli pnömonilerde etkenler ve kolaylaştırıcı faktörler(8) Kolaylaştırıcı faktörler Etkenler Aspirasyon, abdominal cerrahi geçirilmesi Anaeroblar Koma, kafa travması,influenza geçirilmesi, İV ilaç bağımlılığı, diabetes mellitus,böbrek yetmezliği S.aureus Yüksek doz steroid kullanımı Legionella Yoğun bakımda izlem,steroid kullanımı, antibiyotik kullanımı, yapısal akciğer hastalığı, malnütrisyon, uzamış hospitalizasyon, invaziv mekanik ventilasyon uygulanması P.aeruginosa Antibiyotik kullanımı, invaziv mekanik ventilasyon Acinetobacter Antibiyotik kullanımı, uzamış invaziv mekanik ventilasyon MRSA ABD ve Kanada 1997 verilerinin yayınlandığı SENTRY çalışmasında Gram pozitif etkenlerden S.aureus’ un ilk sırada yer aldığı, P.aeruginosa ve H. İnfluenzae’ nin onu izlediği belirtilerek; yıllar içerisinde giderek artan sıklıkta ortaya çıkan vankomisin dirençli enterokoklara ve Gram negatif bakterilerin de genişlemiş etki spektrumlu beta laktamaz (ESBL) ile yüksek düzeyli amp-C beta laktamaz içermeleri nedeni ile 3.kuşak sefalosporinlere yüksek oranda direnç gelişimine dikkat çekilmiştir(Tablo 6)(10). Ülkemizden yapılan yayınlarda ise Gram negatif bakteriler ilk sırayı almaktadır (Tablo 7)(11-14). Ülkemiz yayınlarında K.pneumoniae suşlarının %68-88 gibi çok yüksek oranda ESBL ürettiği vurgulanırken bir başka çalışmada izole edilen 74 P.aeruginosa suşunun %50’sinin tüm antibiyotiklere dirençli olduğu bildirilmiştir; bir başka çalışmada ise 5 ayrı yoğun bakımda üretilen P.aeruginosa suşlarının çok güçlü Gram negatif spektruma sahip antibiyotiklere duyarlılıklarının ortalamalarının sırası ile imipenem, siprofloksasin, amikasin, seftazidim, seftriakson, gentamisine %43, %36, %56, %40, %11, %21 gibi inanılmaz düşük düzeyde olduğu vurgulanmıştır(12-14). Tablo 6: ABD ve Kanada’da hastane kökenli pnömonide etkenler (10) Etkenler S.aures P.aeruginosa H.influenzae Klebsiella S.pneumoniae Enterobacter E.coli S.maltophilia M.catarrhalis Serratia marcescens % oranlar 22.9 18.1 10.3 8.7 7.7 7.4 4.7 3.6 3.3 2.6 Ayırıcı tanıya giren non infeksiyöz patolojilerin varlığı ve çok yüksek direnç oranları nedeniyle HKP tanısı konulduğu anda empirik tedavi hemen başlanmalı ve ileri incelmeler yapılarak doğru etkene ulaşılarak tedavi spektrumu uygun antibiyotiklerle daraltılmalıdır. Bu nedenle tanı ve tedavi yaklaşımını özetleyen algoritmaların dikkatle uygulanması gereklidir. 108 Tablo 7: Ülkemizde hastane kökenli pnömoniler, ventilatörle ilişkili pnömoniler ve yoğun bakımda gelişen pnömonilerdeki etkenler ve % olarak oranları (11-14) Etkenler P.aeruginosa MRSA Acinetobacter spp K.pneumoniae MSSA E.coli Kuagülaz (-) stafilokoklar Enterobacter spp • • • HKP (11) 23 * 22 17 * 5 ? ? HKP (13) 36 ** 22.8 14.6 ** 2.7 ? 2.7 VİP (12) 38 15 12 12 4 3 3 3 YB (14) 25 ? 14 11 ? 5.3 ? ? * MRSA/MSSA ayırımı yapılmadan S.aureus olarak bildirilmiş: % 15 ** MRSA/MSSA ayırımı yapılmadan S.aureus olarak bildirilmiş: % 16.8 ? : oran bildirilmemiş Toraks Derneği tarafından hazırlanmakta olan ve 2002 yılında Toraks Dergisi’nde yayınlanacak olan “Toraks Derneği Hastane Kökenli Pnömoniler Tanı ve Tedavi Rehberi”ne göre hastalar erken HKP, geç HKP ve çoğul dirençli bakteri olasılığı göz önüne alınarak 3 alt grupta toplanmışlardır. Grup 1, Grup 2 ve yoğun bakımda izlenmeleri gerekli olan Grup 3 hastalardaki empirik antibiyotik seçimleri ve yaklaşım şekli özetlenmiştir(Tablo 8) (15). Erken HKP grubundaki hastalar eğer çoğul dirençli bakteri riski taşımıyorlarsa Grup 1’de yer alacaklardır. Bu hastalarda olası etkenler göz önüne alınarak 2. kuşak sefalosporinler, betalaktam-betalaktamaz inhibitörleri yada levofloksasin kullanılabilecektir. Benzer şekilde geç ortaya çıkan ancak çoğul dirençli bakteri olasılığı taşımayan Grup 2’ deki olgularda da antipsödomonal spektrum taşımayan betalaktam antibiyotiklerle aminoglikozit/kinolon kombinasyonu önerilmiştir. Bu grupta monoterapide antipsödomonal ajanların tek başına kullanılabileceği(özellikle ESBL üreten K.pneumoniae göz önüne alınarak) belirtiliyorsa da bu gruptaki çok güçlü, geniş spektrumlu ve ancak zor durumda kullanılacak ilaçları Grup 3 için saklamanın daha doğru olacağı da vurgulanmaktadır (Tablo 9). Grup 3 ‘de artık pnömoninin erken yada geç geliştiğinden çok daha önemli bir faktör; çoğul dirençli bakteri olasılığı ön plandadır; P.aeruginosa, Acinetobacter, MRSA,ESBL üreten K.pneumoniae gibi tedavisi çok güç olan etkenler söz konusudur ve tedavide kaçınılmaz olarak antipsödomonal bir betalaktam antibiyotikle kinolon yada aminoglikosit kombinasyonuyla başlamalı, etken izole edilir edilmez gerekirse spektrum daraltılmalıdır. Grup1,2,3’de belirtilen antibiyotikler grupları içerisinden hangilerinin seçileceğini o hastanede, hatta o birimde üreyen bakteriler ve direnç oranları belirleyecektir. Aynı hastanenin değişik birimlerinde (yoğun bakım, servis) farklı etkenler, farklı direnç oranları olabileceğinden empirik tedavi seçenekleri de o birime özgü olarak seçilmeli ancak aynı endikasyonla gelen hastalarda aynı antibiyotik kullanılarak diğer antibiyotikler korunmalı, tümüne birden direnç gelişimi engellenmeğe çalışılmalıdır. Örneğin bir ünitede Grup 3’de yer alan her hastada empirik olarak önceden belirlenmiş olan aynı antibiyotik kombinasyonu titizlikle uygulanmalı ve uzun bir süre (direnç paterni değişimi göz önüne alınarak 6 ay – 1 yıl) bu seçim değiştirilmeyerek, diğer antibiyotikler korunmalıdır. Rehberde söz konusu edilen önerıler yalnızca empırık antıbıyotık uygulanması ıçın geçerlıdir, etken ızole edıldıkten sonra antıbıyotık duyarlılığına göre spektrum daraltılmalıdır. Empirik tedavide seçilecek antibiyotiğin farmakolojik ve farmakokinetik özellikleri gözönüne alınmalıdır.Solunum sekresyonlarına penetrasyonu düşük olan aminoglikozidlerin pnömoni gelişimine bağlı düşük pH da inaktive olabileceği gözönüne alınarak HKP' de asla monoterapi ajanı olarak kullanılmamalıdır. Ancak Grup 2 ve 3’ de kombine tedavide yer almalıdır. Yine empirik tedavide antibiyotiklerin bakterisidal etki mekanizmaları da göz önüne alınmalıdır. Aminoglikozitler konsantrasyona bağlı bakterisidal etkileri ve postantibiyotik etkileri nedeni ile günde tek doz şeklinde uygulanmalıdır. 109 Tablo 8: HKP’DE EMPIRIK TEDAVI YAKLAŞIMI (15) Erken ≤ 4 gün Grup 1 Monoterapi - 2. kuşak sefalosporin - betalaktamaz inhibitörlü betalaktam* - levofloksasin A-Yüksek riskli, potansiyel çoklu dirençli bakteri infeksiyonu olasılığı varsa; • Önceden antibiyotik kullanımı, • 7 günden uzun mekanik ventilasyon • 48 saatten uzun yoğun bakımda kalmak • Acil entübasyon B-Mortaliteyi artıran diğer faktörler • Bilateral, multilober, kaviter tutulum, apse, ampiyem, hızlı radyolojik progresyon, • PaO2/FiO2< 250 • Ağır sepsis/ septik şok 1111111111111 Geç ≥5 Grup 2 Monoterapi - kinolon - 3.kuşak nonpsödomonal sefalosporin -betalaktamaz inhibitörlü betalaktam ** - moksifloksasin** Grup 3 Kombine tedavi - antipsdomonal penisilinler (piperasilintazobaktam) - antipseudomonal sefalosporinler (seftazidim, sefaperazon/sulbaktam,sefe pim) -karbapenem (imipenem,meropenem) + - aminoglikozid - kinolon ± glikopeptidler***(vankomi sin, teikoplanin) *Farmokinetik özellikleri nedeni ile parenteral tedavide sulbaktam ampisilin, ardışık tedavi protokolünde oral tedavide klavulinik asid amoksisilin tercih edilmelidir. ** Ünite/hastanede ilk tercih monoterapi ya da kombine tedavi ajanlarına direnç sözkonusu ise ve önerilen ajanlara duyarlılık dikkate alınarak tercih edilmelidir. ***MRSA infeksiyonu için risk faktörleri varsa, başlangıç empirik tedaviye 72 saat içinde yanıt alınamıyorsa eklenmelidir 110 Tablo 9: HKP’de gruplar ve olası etkenler (15) Grup 1 S. pneumoniae H. influenzae M.catarrhalis MSSA Grup 2 S. pneumoniae H. influenzae M.catarrhalis MSSA (İnfluenza virüs infeksiyonu Enterobakter türleri geçirilmesi, koma, kafa travması, K. pneumoniae SSS cerrahisi, diabetes mellitus, renal S. marcescens yetmezlik risk faktörleridir.) E. coli Diğer Gram(-) çomaklar MRSA Grup 3 P.aeruginosa, Acinetobacter türleri MRSA K.pneumoniae S. maltophila İleri yaş ve renal fonksiyonları bozuk hastalarda aminoglikozidlerden kaçınılmalı yada serum düzeyleri dikkate alınarak tedavi sürdürülmelidir. İki beta laktam antibiyotik kombine edilmesinden kaçınılmalıdır. Sinerjistik olmayacağı gibi antagonist etkili olabilir; beta laktamaz indüksiyonu nedeni ile her iki ajan inaktive olarak tedavi başarısız olabilir. Pseudomonas aeruginosa infeksiyonlarında ortak direnç mekanizmalarını indüklemesi nedeni ile karbapenem+ kinolon kombinasyonlarından mümkün olduğunca kaçınılmalıdır. Glikopeptidler empirik tedavide yer almamalıdır. Ancak noninvaziv ya da invaziv yöntemle alınan alt solunum yolu örneğinin Gram boyalı incelemesinde stafilokok morfolojisi destekleniyorsa Grup 3’ de empirik tedaviye glikopeptid eklenmelidir. Bu hastalarda empirik olarak başlanan glikopeptid etkenin stafilokok olmadığı gösterilince kesilmelidir. MRSA sıklığının yüksek olduğu birimlerde kültür pozitifliğinin kolonizasyonu yansıtabileceği unutulmamalıdır. HKP’li tüm olgularda tedaviye parenteral yoldan başlanmalıdır. Klinik yanıt elde edilen, en az 24 saat ateşsiz dönem saptanan, lökosit sayısının normale döndüğü olgularda ardışık tedavi ilkelerine uygun olarak oral tedaviye geçilebilir. HKP’de tedavi süresi 10-14 gün olarak belirtilmiştir ancak ağır, yaygın, komplikasyonlu, altta yapısal akciğer hastalığı varlığı, yavaş rezolüsyon, çoğul dirençli bakteri varlığında süre uzatılmalıdır (15). Tanı Yöntemleri HKP’de tanı yöntemleriyle; grafide ortaya çıkan yeni infiltrasyonun pnömoniye bağlı olup olmadığınıortaya koyarak noninfeksiyöz süreçleri dışlamak, pnömoni tanısı doğru ise doğru etkeni ve direnç paternini saptamak ve hastalığın şiddetini ortaya koymak amaçlanır. HKP tanısı en çok karıştırılan, yanlış negatif ve yanlış pozitif tanı oranını 1/3’e kadar yükseldiği bir klinik tablodur. Grafideki yeni infiltrasyon; ARDS, kalp yetmezliği,ilaç akciğeri,radyasyon pnömonitisi, aspirasyon pnömonisi, alveolar hemoraji,kolajen vaskülitin alkciğer tutuluşu, zeminde var olan malignitenin akciğer tutuluşu, primer akciğer kanseri, bronkoalveolar hücreli kanser, pulmoner emboli, atelektazi, akciğer kontüzyonu veya metasataza bağlı olabilir. HKP tanısı konulmadan önce ayırıcı tanı olasılıkları gözden geçirilmeli ve gerekirse bilgisayarlı tomografi ve bronkoskopi planlanmalıdır. Ancak bu süreçte, HKP’nin tedaviye rağmen yüksek olan mortalite oranları göz önüne alınarak hasta tedavisiz bırakılmamalı, empirik tedaviye önerilen algoritmalara uygun olarak başlanmalı , HKP dışlandığı anda da tedavi kesilmelidir. Bilgisayarlı toraks tomografisi, arter kan gazı, hemogram, biyokimyasal incelemeler HKP’nin ağırlığını; multipl organ yetmezliğinin, solunum yetmezliğinin eklenip eklenmediğini yansıtırken; kavite, abse, plörezi gibi komplikasyonların da araştırılmasına olanak sağlayacaklardır. Bilgisayarlı tomografi şüphesiz tedaviye yanıtın alınmadığı, ayırıcı tanı olasılıklarının dışlanmasının gerekli görüldüğü, pulmoner komplikasyonların irdelenmesinin gerekli olduğu olgularla sınırlı tutulmalıdır. 111 HKP’de etkeni izole temeğe yoğun olarak çaba harcanmalıdır. Etkenlerin toplum kökenli pnömoni etkenlerine göre göreceli olarak daha kolay üremesi, atipik etkenlerin çok geri planda olması kolaylaştırıcı faktörlerdir. Diğer yandan direnç oranlarının bilinmesi, doğru etkene ulaşarak spektrumun daraltılması gerekliliği nedeniyle bakteriyoloji tanıda önemli yer tutar. Balgam yada uyarılmış balgam önemli bir materyaldir. Balgam nitelikliyse(her sahada 25’den çok nötrofil, 10’dan az epitel içeren balgam) preparata hakim olan bakteri etkendir ve bu balgam kültürünün invaziv yöntemlerle benzer duyarlılıkta olduğunu yansıtan çok sayıda çalışma vardır. Entübe hastalarda sürveyans kültürü gerekli değildir, hatta kolonize bakterilerin tedavisini yanlışlıkla gündeme getireceğinden zararlı da olabilir, yapılmamalıdır. HKP tanısı konulduğunda, etken nedir sorusu sorulduğu zaman ileri incelemeğe yönelinmelidir. Bu amaçla endotrakeal aspirasyon(EA) yada körleme yöntemle(bronkoskop rehberliği olmadan) ucu korunmuş fırçalama(PSB) yapılabilir. Her 2 yöntemde de kolonizasyon/etken ayırımı için, sonuçta hastadaki gerçek etkeni öğrenip tedavi etmek, entübasyon tüpünü tedavi eder konuma düşmemek için mutlaka kantitatif kültür yapılmalıdır. Sınır değerler endotrakeal aspirasyon için 105, PSB için 103’dür. Körleme yapılan EA ve PSB’nin bronkoskop(FOB) eşliğinde yapılanlarla aynı spesifite ve sensitiviteye sahip olduğu bir çok çalışmada vurgulanmıştır(16-19). FOB gerekli olan olgularda PSB, BAL yapılabilir. BAL için sınır değer 104 olarak bildirilmektedir. ProBAL da yapılabilirse de maliyet etkinlik açısından konvansiyonel BAL, ek tek kullanımlık malzeme gerektirmemesi, bakteriyolojik incelemelerin yanı sıra sitolojik, parazitolojik,ARB bakılarına da olanak sağlaması nedeniyle tercih edilmelidir. FOB yapılabilmesi için trombosit sayısının en az 20000/mm3, INR < 1.5 olması gereklidir. Fungal pnömoni yada noninfeksiyöz ayırıcı tanı olasılığı nedeni ile trans bronşiyal parankimal biyopsi(TBB) planlanıyorsa trombosit sayısı en az 50000/mm3 olmalıdır. Ventilatöre bağlı olmayan HKP olgularında 25 numaralı Chiba iğnesi ile 5cc’serum fizyolojik içeren 20 cc’lik enjektörle, perkütan yatak başında matite alınan alandan girmek, 4 cc serum fizyolojiği verip aspire ederek kantitatif kültür yapmanın yüksek tanısal verimliliğe sahip olduğu, yan etkinini minimal pnömotoraksla sınırlı olduğu bildirilmişse de bu konuda ülkemizde henüz deneyim yoktur(20). Ateşli dönemlerde 30 dakika ara ile alınan hemokültür tanıda önemli bir basamaktır. Doğru etkene ve bakteriyemi tanısına ulaşmağa olanak sağlar. Korunma Orofaringeal, gastrik, trakeal kolonizasyonu önlemek:stres ülserlerinden kaçınmak amacı ile kullanılan antasit ve H2 reseptör blokerleri yerine asiditeyi değiştirmeden mukoza koruyan sucralfatı kullanmak gereklidir. Üst gastrointestinal traktusun selektif dekontaminasyonuyonu (SDD), sadece travma, immunsüpresyon ve kemik iliği transplante edilmiş olan hastalarda uygulanması önerilmektedir. Son yıllarda uygulanmakta olan bir diğer yaklaşım da enteral beslenmedir. Nasogastrik sonda yerine jejunuma kadar uzanan tüplerle hastaların beslenmesi, kolonizasyon ve sızıntı ile oluşan pnömoni riskini azaltabilir. Orofaringeal ve gastrik floranın aspirasyonun önlenmesi: Hastaların yarı oturur durumda yataklarının başı kaldırılarak beslenmeleri, sürekli infüzyon yerine küçük volümlerde sık beslenmeleri, endotrakeal tüp çekilme ve yer değiştirmelerinde balon söndürülmeden enteral beslenme tüpünün aspire edilerek midenin boşaltılması, aylarca süren bilinç yitiminin olduğu nörolojik olgularda perkütan gastrostomi(PEG) açılması gereklidir. Enteral beslenme yoğun bakım kökenli pnömonlerde giriş kapılarından biri niteliğindedir ancak bu durum, hastalarda fizyolojik olmayan, çok pahalı, barsak kaynaklı gram bakteri sepsis insidensini ve vasküler tromboz riskini artıran parenteral beslenmenin tercih edilebileceği anlamında algılanmamalıdır. Konuyu irdeleyen bir çok çalışma ve editörlerin derlemelerinde parenteral beslenmenin ilk kontrendikasyonu enteral beslenme olanağının (oral / nasogastrik / enteral / PEG) bulunmasıdır. Endotrakeal tüp ve mekanik ventilasyon / nemlendiriciler / aspirasyon: Endotrakeal tüpün steril koşullarda takılması, orogastrik entübasyonun tercih edilmesi, aspirasyonların steril kapalı sistemler 112 aracılığı ile yapılması, bakteri filtrelerinin kullanılması, hortum ve diğer iletici sistemlerin tek kullanımlık olması, bu sistemlerdeki kolonizasyonları engellemek amacı ile ventilatör devrelerinin sık değiştirmekten kaçınılması, değiştirmek gerektiğinde önce hastaya yakın kısımdan başlanarak hortum içeriğinin aspire edilmemesine özen gösterilmesi, yoğun bakım personelinin sık sık ellerini yıkamaları özellikle hastaya / aletlere / ekipmana dokunmadan önce ve sonra ellerini yıkamaları yada dezenfektan solüsyonlarla ellerini dezenfekte etmeleri gereklidir.Benzer amaçla steril eldiven kullanımının yaygınlaştırılması(her dokunuş öncesinde) pahalı bir seçenek olarak düşünülebilir, daha da tehlikeli olanı böyle bir uygulamada sağlık personeli kendini güvende hissettiğinden hastadan hastaya geçerken yada aynı hastanın farklı anatomik bölgelerine/aletlere dokunurken kendini daha özgür hisssedecek ve kontaminasyon daha da kolaylaşabilecektir. Alveole ve bronşlara penetrasyonu iyi olmayan aminoglikosit grubu antibiyotikleri Gram spektrumlarını da göz önüne alarak endotrakeal / nemlendirici ile vermek hayal kırıklığı ile sonuçlanmıştır: rezistan suşlarla daha ağır pnömoniler gelişmiştir. Benzer sonuçlar profilaktik geniş spektrumlu antibiyotik kullanımında da sözkonusudur, HKP önlemek amacı ile geniş spektrumlu antibiyotiklerin profilaktik kullanımları açıkça tıbbi hatadır. Diğer bir yaklaşımda en sık gözlenen etkene yöneliktir: lipopolisakkarit pseudomonas aşısı ve hiperimmun anti-pseudomonas globulini araştırma aşamasında olan, etkinlikleri büyük olgu serileri ile kanıtlanamamış yeni yaklaşımlardır. Hastane personelinin özellikle yoğun bakım gibi kritik yerlerde görev alan personelin yıllk grip aşısı yaptırması önemlidir. HKP korunmasında en önemli yöntemlerden birisi de , doğru / rasyonel antibiyotik kullanım ilkelerine sıkı sıkıya uyulması, hastane genelinde kısıtlanmış antibiyotik politikaları uygulanması, antipsödomonal ajanların kullanımına kısıtlama getirilerek bu antibiyotiklerin korunmasıdır(21). Ülkemizden bildirilen çok sayıda makalede P.aeruginosa, Acinetobacter, Klebsiella suşlarındaki inanılmaz ve yurt dışı örneklerinden birkaç kat yüksek olan direnç oranları ülkemiz için korunma önlemlerinin ve kısıtlı antibiyotik kullanım ilkelerinin ne denli gerekli olduğunu ortaya koymaktadır. 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. 19. 20. 21. KAYNAKLAR American Thoracic Society. Hospital-acquired pneumonia in adults:diagnosis, assesment of severity, initial antimicrobial therapy, and preventative strategies: A consensus statement. Am J Respir Crit Care Med 1995;153:1711-25. Lynch JP. Hospital-acquired pneumonia. Chest 2001;119:373s-384s. Akalın H,Özakın C,Kahveci F, ve ark. Hastane kökenli pnömoniler. Flora 1999;4:253-7. Torres A,Aznar R,gatell JM,et al. Incidence, risk, and prognosis factors of nosocomial pneumonia in mechanical ventilated patients. Am Rev Respir Dis 1990;142:523-8. Celis R,Torres A,Gatell JM,et al. Nosocomial pneumonia. Chest 1988;93:318-23. Vincent JL,Bihari DJ,Suter PM,et al. The prevalance of nosocomial infection in intensive care units in Europe. JAMA 1995;274:639-44. Rello J, Paiva JA,Baraibar J et al. International conference for the development of consensus on the diagnosis and treatment of ventilator associated pneumonia. Chest 2001;120:955-70. Fiel S. Guidelines and critical pathways for severe hospital-acquired pneumonia. Chest 2001;119:412s-8s. Biberoğlu K,Kılınç O,Çakır N, ve ark. Toraks Derneği Hastane Kökenli Pnömoniler Tanı ve Tedavi Rehberi. Toraks Bülteni 1998;3(1):15-25. Jones RJ. Resisitance patterns among nosocomial pathogens. Chest 2001;119:397s-4004s. Akalın H,Özakın C,Sütçü S,ve ark. Uludağ Üniversitesi Tıp Fakültesinde hastane infeksiyonları. Klimik 1999;12:55-7. Uzel S,Çağatay A,Özsüt H, ve ark. Yoğun bakım biriminde ventilatörle ilşkili pnömoni etkeni olabilecek bakteriler ve antibşiyotiklere duyarlılıkları. Klimik 1999;12:60-4. Sevinç C,Uysal Ü,Kılınç O,et al. Clinical and bacteriological features of hospital acquired pneumonias. ERS Annual Congress Abstract Book 2001:p . Akalın H,Özakın C,Kahveci F. Yoğun bakım biriminde en sık izole edilen Gram-negatif bakteriler ve antibiyotik duyarlılıkları. Klimik 1999;12:65-8. Ece T,Arman D ve ark.Toraks Derneği Hastane Kökenli Pnömoniler Tanı ve Tedavi Rehberi 2002. Toraks Dergisi 2002 (baskıda) Pedro SG. Are quantitave cultures useful in the diagnosis of hospital-acquired pneumonia. Chest 2001;119:385s-90s. Sanchez-Neito JM,Torres A,Garcia-Cordoba F,et al. Impact of invasive and noninvasive quantitative culture sampling on outcome of ventilator-associated pneumonia. Am J Respir Crit Care Med 1998;157:371-6. Marquette CH,Copin M,Wallet F,et al. Diagnostic tests for pneumonia in ventilated patients:prospective evaluation of diagnostic accuracy using histology as a diagnostic gold standart. Am J Resrir Crit Care Med 1995;151:1878-88. Chastre J,Fagon JV,Lesco MB,et al.Evaluation of bronchoscopic techniques for the diagnosis of nosocomial pneumonia. Am J Respir Crit Care Med 1995;152:231-40. Dorca J,Manresa F,Esteban L,et al. Efficacy, safety, and therapeutic relevance of transthoracic aspiration with ultrathin needle in nonventilated nosocomial pneumonia. Am J Respir Crit Care Med 1995;151:1491-6. Center for Disease Control and Prevention. Guidelines for prevention of nosocomial pneumonia. MMWR 1997;46:22. 113