PERİYODİK
TABLO
ALİ DAĞDEVİREN
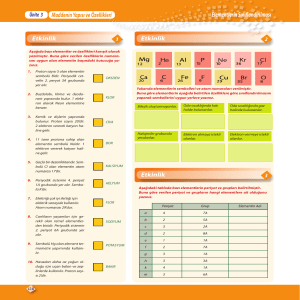
Elementlerin atom numaraları belirli bir kurala uyarak
sıralanması ile periyodik cetvel oluşur.
ALİresmi
DAĞDEVİREN
Periyodik tablo
Periyodik cetvelde yatay sıralara PERİYOT, düşey
sıralara GRUP denir.
Periyodik cetvelde 7 tane periyot, 8 tane A grubu, 8 tane B
grubu
vardır. 8 B grubu 3 tanedir. Her periyot kendine ait olan
1A grubu ile başlayıp, 8A grubu ile sona erer. 1 nci
periyotta 2, 2 ve 3 ncü periyotta , 4 ve 5’nci periyotta 18, 6
ncı periyotta 32 element vardır. 7’ nci periyot daha
tamamlanmamıştır.
Periyodik cetvelde, aynı grupta bulunan elementlerin
değerlik elektron sayıları aynı olduğundan, benzer
kimyasal özellik gösterir.
Atomların son yörüngesine (son enerji düzeyde) değerlik
tabakası, bu tabakada bulunan elektronlara da
DEĞERLİK ELEKTRONLARI denir.
Bir elementin bulunduğu A grup numarası o elementin
değerlik elektron sayısını gösterir.
ALİ DAĞDEVİREN
Gruplarda Yukarıdan
Aşağıya Doğru İnildikçe
Periyotlarda Soldan
Sağa Doğru Gidildikçe
Atom Numarası
Artar
Artar
Atom Hacmi
Artar
Azalır
İyonlaşma Enerjisi
Azalır
Artar
Metalik Özellik
Artar
Azalır
Ametalik Özellik
Azalır
Artar
ALİ DAĞDEVİREN
Periyodik tabloda “1A,2A,3A”grubu
elementleri metal, “4A,5A,6A,7A”
grubu elementleri ametal, “8A”grubu
elementleri yarımetaldir.
1A grubu elementlerine alkali metal,
2A grubu elementlerine toprak alkali
Metal,
3A grubu elementlerine halojenler,
8A grubu elementlerine soygazlar
denir.
ALİ DAĞDEVİREN
Bu grupları tanıyalım.
ALİ DAĞDEVİREN
METALLER
•
•
•
•
•
•
•
•
•
•
Yüzeyleri parlaktır.
Isı ve elektiriği iletirler.
Tel ve levha haline gelebilirler.
Oda sıcaklığında(cıva hariç)katı hÂldedirler.
Kendi aralarında alaşım yaparlar.
Ametallerle iyonik bağlı bileşik yaparlar.
Son yörüngelerinde 1,2,3 elektron bulundururlar.
Erime noktaları yüksektir.
Atomik yapıdadırlar.
Şimdi metallerle ilgili kısa filmimizi izleyelim.
ALİ DAĞDEVİREN
ametaller
•
•
•
•
•
•
•
Son yörüngelerinde 4,5,6,7 elektron bulunduran
Elementlerdir.
Yüzeyleri mattır.
Isı ve elektriği iletmezler(grafit hariç).
Kırılgandırlar.
Oda koşullarında sıvı,gaz,katı olabilirler.
Metallerle iyonik yapılı,kendi aralarında kovalent
yapılı bileşik oluştururlar.
• Erime ve kaynama noktaları düşüktür.
• Molekül yapılıdırlar.
•Şimdi ametallerle ilgili kısa filmimizi
izleyelim.
ALİ DAĞDEVİREN
Alkali metaller
1A grubu elementlere alkali metaller denir.
1A grubunun ilk üç metali lityum, sodyum ve potasyum
düşük yoğunluğa sahip olup suyun üzerinde yüzerler.
Bir elektron kaybederek +1 değerlik kazanırlar.
Alkali metaller ametaller ile reaksiyona girerek iyonik yapılı
bileşik oluştururlar.
İyonik bileşiklerle beyaz renkli katılar oluşturup suda
çözünerek renksiz çözelti elde edilir.
Reaktif elementlerdir. Su ile reaksiyona girip metal hidroksit
ve hidrojen gazı oluştururlar.
ALİ DAĞDEVİREN
Geçiş metalleri
Demir ve bakır gibi elementleri içeren periyodik tablonun
ortasında yer alan bölümdür.
Geçiş metallerini alkali metallere göre karşılaştıracak
olursak;
Daha az reaktiflerdir. Oksijenle veya su ile temas
edildiklerinde paslanmazlar.
Sert, güçlü ve dayanıklıdırlar.
Oda sıcaklığında sıvı hâlde bulunan civa hariç yüksek
kaynama noktalarına sahiptirler.
Geçiş metalleri yaşantımızdaki pek çok araç ve gereçlerde
kullanışlıdırlar. Örneğin; ütü yapımında çelik, elektrik
kablolarında bakır kullanılır.
Bir çok geçiş metalleri katalizör olarak kullanılır.
Bir çok geçiş metali renkli ALİ
bileşiklerin
yapımında kullanılır
DAĞDEVİREN
halojenler
•
7A grubu elementlerine halojenler denir. Halojenler ametal
elementlerden oluşurlar.
•
Halojenlerin hepsi zehirli ve renklidir.
•
Halojenler element molekülü hâlinde bulunurlar
•
Halojenler elektron alarak – 1 değerlik kazanırlar.
•
Halojenler metallerle reaksiyona girerek iyonik tuzları oluştururlar.
•
Halojenler diğer ametal elementlerle kovalent bağlar oluştururlar.
•
7A grubunda yukarıdan aşağıya doğru inildikçe elementlerin
reaktifliği azalır, erime ve kaynama noktaları yükselir.
•
7A grubu elementlerinden flor ve klor oda sıcaklığında gaz, brom
sıvı ve iyot ise katı bir hâlde bulunur.
•
Reaktifliği fazla olan halojen reaktifliği düşük olan halojenle yer
değiştirerek tuz meydana getirir.
ALİ DAĞDEVİREN
SOYGAZLAR
• 8A grubu elementlerine soy gazlar veya asal gazlar
denir.
• Soy gazlar en kararlı elementlerdir.
• Son yörüngelerindeki elektron sayılarını sekizdir.
• Diğer element molekülü yapısındaki gazlara göre tek
atomlu hâlde bulunurlar.
• Soy gazlar lâmba yapımında kullanılırlar.
• Helyum soy gazı havadan daha hafif olduğu için uçan
balonların yapımında kullanılır.
ALİ DAĞDEVİREN
Periyodik tabloda elementlerin gösterimi
Z=P
A=Z+N
İ.Y.=p-e
ALİ DAĞDEVİREN
Grup ve periyodun bulunması
• Elementlerin son yörüngelerindeki
elektron sayısı grup numarasını,enerji
düzeyi ise periyodunu verir.
ALİ DAĞDEVİREN
Örnek sorular:
1) Atom numarası Cvp:
23 olan x
X ) ) ) )
elementinin e
2 8 8 5
dağılımın ve
4. periyot
grup,periyot
5A gurubu
numaralarını
bulunuz .
elementidir.
ALİ DAĞDEVİREN
• 2.periyot 5A
grubundaki X
elementinin atom
no.su kaçtır?
• Cvp:
X ) )
2 5
ALİ DAĞDEVİREN
= 7
Bir elementin periyodik cetveldeki yeri
hangisiyle belirlenir?
A)atom ağırlığı
B)değerlik
C)atom numarası
D)kimyasal özellikleri
ALİ DAĞDEVİREN