TÜRKİYE CUMHURİYETİ
ANKARA ÜNİVERSİTESİ
SAĞLIK BİLİMLERİ ENSTİTÜSÜ
BAKTERİ ENDOTOKSİNLERİNİN
VİRAL AŞI ÜRETİMİNDE KULLANILAN
DEVAMLI HÜCRE HATLARINA ETKİSİNİN
ARAŞTIRILMASI
Züleyha ERGÜN
MİKROBİYOLOJİ ANABİLİM DALI
YUKSEK LISANS TEZI
DANIŞMAN
Prof. Dr. HAKAN YARDIMCI
2013 - ANKARA
TÜRKİYE CUMHURİYETİ
ANKARA ÜNİVERSİTESİ
SAĞLIK BİLİMLERİ ENSTİTÜSÜ
BAKTERİ ENDOTOKSİNLERİNİN
VİRAL AŞI ÜRETİMİNDE KULLANILAN
DEVAMLI HÜCRE HATLARINA ETKİSİNİN
ARAŞTIRILMASI
Züleyha ERGÜN
MİKROBİYOLOJİ ANABİLİM DALI
YUKSEK LISANS TEZI
DANIŞMAN
Prof. Dr. HAKAN YARDIMCI
2013 - ANKARA
İÇİNDEKİLER
Kabul ve Onay
ii
Ġçindekiler
iii
Önsöz
vi
Simgeler ve Kısaltmalar
vii
ġekiller
viii
Çizelgeler
x
Resimler
xi
1.
GİRİŞ
1
1.1. Endotoksinlerin Genel Özellikleri ve Önemi
2
1.2. Endotoksin AraĢtırmalarının Tarihçesi
4
1.3. Endotoksinlerin Fiziko-Kimyasal Özellikleri
5
1.4. Endotoksinlerin Etki Mekanizması
8
1.5. Endotoksinlerin Tespit Yöntemleri
10
1.6. Hücre Hatları ve Bakteri SuĢları
12
1.6.1. Vero Epitelyal Hücre Hattı
12
1.6.2. Baby Hamster Kidney (BHK-21) Fibroblast Hücre Hattı
13
1.6.3. Madin-Darby Bovine Kidney (MDBK) Epitelyal Hücre Hattı
13
1.6.4. Pseudomonas aeruginosa SuĢu
14
1.6.5. Escherichia coli SuĢu
15
2. GEREÇ VE YÖNTEM
17
2.1. Gereç
17
2.1.1. Bakteri SuĢları
17
2.1.1.1. Pseudomonas aeruginosa SuĢu
17
2.1.1.2. Escherichia coli SuĢu
17
2.1.2. Hücre Hatları
18
2.1.2.1. Vero Epitelyal Hücre Hattı
18
2.1.2.2. Baby Hamster Kidney (BHK-21) Fibroblast Hücre Hattı
18
iii
2.1.2.3. Madin-Darby Bovine Kidney (MDBK) Epitelyal Hücre
Hattı
2.1.3. Besiyerleri
18
2.1.3.1. Nutrient Agar
18
2.1.3.2. Nutrient Broth
19
2.1.3.3. Kanlı Agar
19
2.1.3.4. Hücre Üretme Vasatı
19
2.1.4. Tripsin ve EDTA
20
2.1.5. Trypan Blue Boyası
20
2.1.6. LAL Test Kiti
20
2.1.7. ELISA Reader Cihazı ve Kitleri
20
2.1.8. Sarf Malzemeleri
21
2.2. Yöntem
21
2.2.1. P. aeruginosa ve E. coli SuĢlarının Çoğaltılması
21
2.2.2. Mikro API Cihazı ile SuĢların Saflığının Gösterilmesi
21
2.2.3. SuĢların Çoğaltılması
22
2.2.4. Koloni Sayım Yöntemi ile Bakteri Sayımı
22
2.2.5. Endotoksinlerin Açığa Çıkarılması
23
2.2.6. Sterilite Kontrolü
23
18
2.2.7. Jel Klot LAL Testi ile Stok Solüsyonlarında Endotoksinlerin
Tespiti
2.2.8. Jel Klot LAL Testi ile Endotoksin Yoğunluğunun
23
Saptanması
2.2.9. Hücre Kültürlerinin Çoğaltılması
24
24
2.2.10. Hücre Üretme Vasatları Ġçerisinde Stok Solüsyonlardan
Endotoksinli Seri Dilüsyonların Hazırlanması
25
2.2.11. Hücre Kültürlerinin 96 Gözlü Pleytlere ve Hücre Kültürü
Flasklarına Aktarılması
25
2.2.12. 96 Gözlü Pleytler ve Flasklardaki Vasatların Endotoksinli
Vasatlar ile DeğiĢtirilmesi
26
2.2.13. Morfolojik DeğiĢikliklerin Saptanması
26
2.2.14. Kristal Viyole Boyama yöntemi ile Endotoksinlerin Hücre
27
iv
Canlılığına Etkisinin Tespiti
2.2.15. Trypan Blue Boyama yöntemi ile Endotoksinlerin Hücre
Sayısına Etkisinin Tespiti
28
3. BULGULAR
29
3.1. Bakterilerin Çoğaltılması
29
3.2. Mikro API Cihazı ile SuĢların Saflığının Gösterilmesi
29
3.3. Koloni Sayım Yöntemi ile Bakteri Sayımı
29
3.4. Endotoksinli Stok Solüsyonlarının Sterilite Testleri
30
3.5. Jel klot LAL testi ile Endotoksin Kontrolü
30
3.6. ÇalıĢmada Kullanılacak Dilüsyon Basamaklarının Belirlenmesi
31
3.7. Hücre Hatlarının Endotoksinle Muamele Öncesi Sayısal Değerleri
31
3.8. Hücre Morfolojisindeki DeğiĢiklikler
32
3.9. Kristal Viyole Boyama Yöntemi ile Endotoksinlerin Hücre
Canlılığına Etkisinin Tespiti
34
3.10. Trypan Blue Boyama Yöntemi ile Endotoksinlerin Hücre Sayısına
Etkisinin Tespiti
37
4. TARTIŞMA
42
5. SONUÇ
49
ÖZET
51
SUMMARY
53
KAYNAKLAR
55
v
ÖNSÖZ
Bakteriyal endotoksinler hücre kültürlerinde kullanılan ana materyallerin sıkça
rastlanan kontaminantlarıdır. Bu endotoksinler çeĢitli sebeplerle su, serum ve
vasatlara karıĢtığında biyolojik maddelerin kalitesini olumsuz etkileyebildiği bilinen
bir gerçektir. Bunun baĢlıca sebebi olarak, özellikle aĢı hazırlamada kullanılan hücre
kültürlerinde meydana getirdiği toksik etki, ve sulandırma sıvılarına karıĢması
durumunda da kullanıcıya olan etkisi gösterilebilir.
Bu çalıĢmada, bakteri endotoksinlerinin varlıkları Jel klot LAL testi ile tespit
edilerek, aĢı üretiminde kullanılan Vero, MDBK, BHK-21 gibi hücre hatlarına
etkilerinin deneysel olarak araĢtırılması ve bunun yanı sıra, çalıĢma süresince hücre
hatlarında meydana gelen sayısal ve morfolojik değiĢikliklerin belirlenmesi ve
kıyaslanması hedeflenmiĢtir.
Bu tezin konusunun ortaya çıkmasında katkısı bulunan ve tezin her aĢamasında
beni tüm içtenliği ile destekleyen ve değerli önerileri ile bana yön veren danıĢman
hocam Sayın Prof. Dr. Hakan YARDIMCI'ya ve Ankara Üniversitesi Veteriner
Fakültesi Mikrobiyoloji Anabilim Dalı BaĢkanı Sayın Prof. Dr. Serdar DĠKER'e,
Yüksek Lisans eğitimim ve tez çalıĢmam boyunca bilgi tecrübe ve önerilerinden
yararlandığım Mikrobiyoloji Anabilim Dalı Öğretim Üyeleri Sayın Prof. Dr. Müjgan
ĠZGÜR,
Sayın
Prof.
Dr. Mehmet
AKAN'a ve
Sayın
Doç.
Dr. BarıĢ
SAREYYÜPOĞLU'na, ve Tez Savunmasındaki olumlu katkılarından dolayı
Viroloji Anabilim Dalı Öğretim Üyesi Doç. Dr. Taner KARAOĞLU'na;
Tez çalıĢmam süresince manevi desteklerini esirgemeyen, çalıĢma ortamı
hazırlayan, bilgi, tecrübe ve önerilerinden yararlandığım Veteriner Kontrol Merkez
AraĢtırma Enstitüsü Viral AĢı Üretim Laboratuvarı ġefi Sayın Dr. Özden
KABAKLI'ya, tez çalıĢması boyunca benden yardımlarını esirgemeyen, özveri ile
yanımda olan değerli çalıĢma arkadaĢlarıma, ayrıca çalıĢmalarım sırasında sonsuz
özveri ile yanımda olan sevgili annem Emine ERGÜN'e ve kardeĢlerime teĢekkürü
bir borç bilirim.
vi
SİMGELER VE KISALTMALAR
MDBK
: Madin Darby Bovine Kidney
BHK-21
: Baby Hamster Kidney – 21
LAL
: Limulus Amebocyte Lysate
E. coli
: Escherichia coli
P. aeruginosa
: Pseudomonas aeruginosa
Gram (-)
: Gram Negatif Bakteri
LPS
: Lipopolisakkarit
EDTA
: Ethylenediaminetetraacetic acid
EU/kg/sa
: Endotoksin Unit / kilogram / saat
tNF
: Tümör Nekrozis Faktör
kDA
: Kilodalton
°C
: Santigrat derece
Lip A
: Lipit A
KDO
: 3- deoksi-D-manno-2 oktulosonik asit
MDCK
: Madin Darby Canine Kidney
FT-IR
: Kırmızı altı spektrometresi
NMR
: Nükleer Manyetik Rezonans
Mm
: Milimetre
Dk
: Dakika
M
: Molar
Ng/ml
: Nanogram / mililitre
µm
: Mikrometre
µl
: Mikrolitre
OD
: Optik Dansite
Gr
: Gram
Yy
: Yüzyıl
GMP
: Good Manufacturing Practice
FCS
: Fötal Kan Serumu
vii
ŞEKİLLER
Şekil 1. Lipopolisakkaritlerin yapısı
Şekil 2.A. P. aeruginosa endotoksini uygulanmıĢ Vero hücresinde tespit edilen
ELISA sonuçları
Şekil 2.B. P. aeruginosa endotoksini uygulanmıĢ MDBK hücresinde tespit edilen
ELISA sonuçları
Şekil 2.C. P. aeruginosa endotoksini uygulanmıĢ BHK-21 hücresinde tespit edilen
ELISA sonuçları
Şekil 3.A. E. coli endotoksini uygulanmıĢ Vero hücresinde tespit edilen ELISA
sonuçları
Şekil 3.B. E. coli endotoksini uygulanmıĢ MDBK hücresinde tespit edilen ELISA
sonuçları
Şekil 3.C. E. coli endotoksini uygulanmıĢ BHK-21 hücresinde tespit edilen ELISA
sonuçları
Şekil 4.A. P. aeruginosa endotoksini uygulanmıĢ Vero hücre kültürünün
1 ml’sinde tespit edilen canlı ve ölü hücre sayıları
Şekil 4.B. E. coli endotoksini uygulanmıĢ Vero hücre kültürünün 1 ml’sinde tespit
edilen canlı ve ölü hücre sayıları
Şekil 5.A. P. aeruginosa endotoksini uygulanmıĢ MDBK hücre kültürünün
1 ml’sinde tespit edilen canlı ve ölü hücre sayıları
Şekil 5.B. E. coli endotoksini uygulanmıĢ MDBK hücre kültürünün 1 ml’sinde tespit
edilen canlı ve ölü hücre sayıları
Şekil 6.A. P. aeruginosa endotoksini uygulanmıĢ BHK-21 hücre kültürünü
1 ml’sinde tespit edilen canlı ve ölü hücre sayıları
Şekil 6.B. E. coli endotoksini uygulanmıĢ BHK-21 hücre kültürünün 1 ml’sinde
tespit edilen canlı ve ölü hücre sayıları
viii
ÇİZELGELER
Çizelge 1. ÇeĢitli maddelerde kabul edilebilir endotoksin konsantrasyonları
Çizelge 2. Jel Klot LAL test protokolüne göre testin değerlendirmesi
Çizelge 3. P. aeruginosa ve E. coli için bakteri sayım sonuçları
Çizelge 4. Vero hücresinde canlı/ölü hücre sayıları ve toplam hücre sayısına göre
yüzdesi
Çizelge 5. MDBK hücresinde canlı/ölü hücre sayıları ve toplam hücre sayısına göre
yüzdesi
Çizelge 6. BHK-21 hücresinde canlı/ölü hücre sayıları ve toplam hücre sayısına göre
yüzdesi
ix
RESİMLER
Resim 1: (A) P. aeruginosa (10-1 dilüsyon) endotoksini uygulanmıĢ Vero hücre
hattının görüntüsü x 100. (B) Vero hücre kontrol x 100.
Resim 2: (A) E. coli (10-1 dilüsyon) endotoksini uygulanmıĢ Vero hücre hattının
görüntüsü x 100. (B) Vero hücre kontrol x 100.
Resim 3: (A) P. aeruginosa (10-1 dilüsyon) endotoksini uygulanmıĢ MDBK hücre
hattının görüntüsü x 100. (B) MDBK hücre kontrol x 100.
x
1
1. GİRİŞ
Endotoksinler Gram negatif bakterilerin dıĢ membranından köken alan, bakteri
Ģeklinin organizasyonu ve stabilitesinden sorumlu, lipopolisakkarit olarak bilinen
moleküllerdir (Joiner ve ark., 2002; Ryan, 2004).
Farmasötik endüstrilerinde üretim süreçleri boyunca veya final üründe
endotoksinleri bulmak mümkündür. Her ne kadar endotoksinler bakteri hücre
duvarına bağlı bulunsalar da, çevreye sürekli salınırlar. Bu salınım, sadece bakteri
ölümü ile değil, aynı zamanda üreme ve bölünme sırasında da meydana gelir.
Bakteriler su, tuz ve tampon gibi zayıf besleyiciliğe sahip ortamlarda da
üreyebildiğinden, endotoksinler hemen hemen her yerde bulunurlar. Tek bir
Escherichia coli, hücre baĢına yaklaĢık 2 milyon lipopolisakkarit (LPS) molekülü
içerir. Endotoksinler pek çok değiĢik fizyopatolojik etkilere sahiptir. Organizma
LPS‟lere fazla miktarda veya sistematik olarak (LPS kan dolaĢım sistemine küçük
miktarlarda sürekli girdiğinde) maruz kaldığında sistemik bir yangısal reaksiyon
meydana gelebilir ve bu da endotoksin Ģoku, doku hasarı ve ölüm gibi çoklu
fizyopatolojik etkilere sebep olabilir (Anspach, 2001; Ogikuba ve ark., 2004).
Bununla birlikte, endotoksinler hücre ve organlara direkt etki etmezler (Heilman,
1965; Heilman, 1968), bunun yerine immun sistemin aktivasyonu, özellikle de
monosit ve makrofajlar baĢta olmak üzere immun sistem hücrelerinin aktive edilmesi
ve dolayısıyla immun yanıtın artırılması ile etki gösterirler. Bu hücrelerin
sentezledikleri maddeler özellikle tümör nekroz faktörü (tNF), birçok interlökinler,
prostoglandinler, koloni sitümüle edici faktörler, trombosit aktive edici faktör ve
serbest radikaller gibi mediyatörlerdir (Forehand ve ark., 1989; Rietschel ve ark.,
1994). Memelilerde endotoksinlerin düĢük konsantrasyonlarının bile (1ng/ml)
intravenöz enjeksiyonunu takiben pirojenik reaksiyonları ve Ģoku indüklediği
bildirilmiĢtir (Fiske ve ark., 2001; Magalhães ve ark., 2007).
Endotoksinler, yoğunluklarına bağlı olarak, farklı hücre hatları ve hücre
kültürleri üzerine oldukça değiĢken toksik etki gösterebilmektedir (Dawson, 1998;
2
Ryan, 2002). Endotoksinler, su, serum ve vasatlara karıĢtığında aĢıların kalitesini
olumsuz etkileyebilir (Geier ve Geier, 2002). Bunun baĢlıca sebebi olarak, özellikle
aĢı hazırlamada kullanılan hücre kültürlerinde meydana getirdiği toksik etki, ve
sulandırma sıvılarına karıĢması durumunda da kullanıcıya olan etkisi gösterilebilir
(David ve Mark, 2002).
Laboratuvar
çalıĢmalarında
ve
biyolojik
ürünlerin
endotoksin
ile
kontaminasyonu sonucunda; zaman ve para kaybının yanı sıra, hücre kültürü üzerine
olumsuz etkileri, deney sonuçlarının yanlıĢ ve hatalı olması, değerli ürünlerin kaybı
ve/veya personel iĢ gücü kaybı görülebilir (Ryan, 2002).
Bu olumsuzlukların önüne geçmek için, GMP (Ġyi Üretim Uygulamaları)
laboratuvar Ģartlarının bir maddesi, endotoksin varlığının tespit edilmesi gerektiğini
vurgulamaktadır. Dolayısıyla endotoksinlerin laboratuvar çalıĢmalarında ve biyolojik
ürünlerde tespit edilmesi çok önemlidir. Endotoksinden kaynaklanan kontaminasyon
tamamen elimine edilmeyebilir, fakat hem olayların sıklığını hem de kontaminasyon
sonuçlarının ciddiyetini azaltmak için özellikle aĢı ve biyolojik ürün üretim safhası
iyi yönetilebilmelidir (Ryan, 2004).
1.1.
Endotoksinlerin Genel Özellikleri
Endotoksinlerin boyutu yaklaĢık 10 kDa - 1.000 kDa arasındadır (Bui, 2012). Birimi
Endotoksin Unit (EU)‟tir. Sıcağa dayanıklıdırlar. 60°C‟ın üzerinde dahi toksik
etkilerini kaybetmeden saatlerce dayanabilmektedirler. Interleukin-1 ve diğer
mediyatörlerin salınmasıyla konakta ateĢ yaparlar. Dolayısıyla pirojendirler (Bates ve
ark., 1998). OluĢturdukları immünojenite zayıftır ve bunlara karĢı oluĢan immun
yanıt toksini nötralize etmekte yetersiz kalır. Formaldehitle muamele edilince toksoid
elde edilmez (Bui, 2012). Endotoksinlerin toksisitesi zayıftır, nadiren öldürücüdürler
fakat endotoksin miktarı artıkça septik Ģok gibi ölümcül sonuçlar doğurabilirler. Her
3
hücrede
endotoksinlere
ait
spesifik
reseptör
bulunmaz.
Lipopolisakkaritler
bakterilerin kromozomal genleri tarafından yönetilirler ve antijenik kodları sadece
kromozomlardadır.
Ġntravenöz olarak uygulanan biyolojik ve farmasötik ürünlerde, uygulama
sırasında
organizmanın
alabileceği
maksimum
endotoksin
seviyesi
tüm
farmakopilerde 5 endotoksin ünitesi (EU)/kg/saat olarak belirlenmiĢtir. Buradaki EU
terimi, bir endotoksinin biyolojik aktivitesini tanımlamaktadır. Bu eĢik değerinin
geçilmesi biyolojik araĢtırmaların ve farmasötik endüstrinin her zaman bir sorunu
olmuĢtur (Berthold ve Walter, 1994; Petsch ve Anspach, 2000).
Endotoksinlerin oldukça stabil moleküller olmaları ve dolayısı ile aĢırı sıcaklık
ve pH değerlerine dayanıklı olmaları sebebiyle, bunları ortamdan uzaklaĢtırmak için
pek çok teknik geliĢtirilmiĢtir. Bunlar arasında 2 fazlı ekstraksiyonlar, ultra
filtrasyon, hidrofobik etkileĢim kromotografisi, iyon değiĢim kromotografisi ve
membran absorbanlarının kullanılması yer alır (Lin ve ark., 2005).
Her ne kadar biyolojik madde endüstrilerinde ve laboratuvar çalıĢmalarında
kullanılan serum ve diğer besiyerleri filtreden geçirilerek veya ısı ile steril edilse de,
endotoksinler filtrelerden geçebilirler ve sterilizasyon Ģartlarına dayanıklıdırlar
(Freshney, 2005). Böylece endotoksinler çeĢitli potansiyel kaynaklar ile hücre
kültürlerine ve diğer biyolojik ürünlere bulaĢabilirler. Endotoksinlerin potansiyel
kaynakları arasında; gerek vasat ve solüsyon yapmak için gerekse yıkama yapmak
için kullanılan su, ticari olarak üretilen ve kullanılan vasat veya serum, vasat
bileĢenleri ve katkı maddeleri, laboratuvar cam ve plastik malzemeleri sayılabilir
(Case-Gould, 1984; Ryan, 2004). Bunların herhangi biri ile endotoksinin hücre
hatlarında etkinliğine bakıldığında, endotoksin yoğunluğunun seviyesine bağlı
olarak; tek tek hücrelerin morfolojisinde değiĢim, hücrede düĢük endotoksin
varlığında hafif ĢiĢme, endotoksin miktarı arttıkça hücrede büzüĢme ve dalgalı yüzey
(Brown, 1982; Berker ve Hold, 1983), hücre sayısında azalma, intraselüler
4
granülasyonda artma ve sitoplazmada vakuol oluĢumları görülebilmektedir
(Takiguchi ve Koga, 1988; Dawson, 1998; Magalhães ve ark., 2007).
1.2.
Endotoksin Araştırmalarının Tarihçesi
Belli solüsyonların intravenöz uygulamasından sonra neden ateĢ görüldüğü
hakkındaki çalıĢmalar 19 yy‟dan önce kaydedildi.
1912 yılında, organizmaya enjekte edildiğinde hipertermiye sebep olan suları
tanımlamak için „pirojenik‟ tanımı kullanılmaya baĢlanmıĢtır. Bu tip tanımlama
1923‟te daha da geliĢtirilerek, gerek ölü/sağlam gerekse parçalanmıĢ bakterileri
içeren, patojenik olsun veya olmasın ya da denatürize olmuĢ endotoksin/ekzotoksin
gibi bakteriyel ürünlerin hepsini hipertermize edici maddeler olarak adlandırılmıĢtır.
(Probey ve ark., 1945; Magalhães ve ark., 2007). Daha sonraları pirojen teriminin
sıklıkla kullanılmasının üzerine bu terim daha popüler olmuĢtur.
Pirojenleri daha iyi anlamak amacıyla en büyük çaba 1925 ve 1945 arasında
gerçekleĢtirildi. Özellikle Co-Tui, Gram negatif bakterilerin en tehlikeli pirojen
üreticisi olduğunu göstermiĢtir (Co ve ark., 1944).
Daha sonra, farmasötik preperasyonlara bulaĢmasından korkulan pirojenlerin
Gram negatif bakterilerin endotoksinleri olduğu ve lipopolisakkarit kompleksleri
olan bu endotoksinlerin bakteri hücre duvarının dıĢ katmanında bulunduğu tespit
edildi
(Westphal,
1975).
Yine
Westphal
(1975),
aslında
pirojenlerin
Enterobacteriaceae ailesindeki mikroorganizmalardan köken aldığını ve uygun bir
dezenfeksiyon ve sterilizasyon süreci olmaksızın hazırlanan enjekte edilebilir
solüsyonların ana kontaminantı olduğunu öne sürmüĢtür. YaklaĢık 20 yıl sonra,
solüsyonların pirojenitesini değerlendirmek için, 14 farmasötik enstitü tarafından
hayvan sistemleri geliĢtirilmiĢtir. Bu çalıĢma, 1942‟de tavĢanlarda ilk resmi pirojen
testinin geliĢtirilmesiyle sonuçlandı. Aynı zaman sürecinde, endotoksinlerin
5
karakterizasyonu ve saflığı üzerine birçok çalıĢma yapıldı ve çok çeĢitli pirojen
türleri izole edildi (Westphal, 1975; Magalhães ve ark., 2007).
Westphal ve Jann (1965), endotoksinleri saflaĢtıran ilk araĢtırıcılar olmuĢtur.
Bu araĢtırıcılar değiĢik Gram negatif bakterilerden sıcak fenol-su ekstraksiyon
yöntemini kullanarak yüksek oranda saf, biyolojik olarak aktif endotoksin elde
etmiĢlerdir. Elde ettikleri ürün, proteinden yoksun olup, sadece karbonhidrat, yağ
asiti ve fosfor içermekte idi. Bu araĢtırıcılar aynı zamanda endotoksinleri tanımlamak
için "lipopolisakkarit" (LPS) terimini ilk kullananlardır (Westphal ve Jann, 1965).
Günümüzde LPS'lerin Gram negatif bakterilerin dıĢ katmanı içerisinde gömülü
olduğu ve LPS biyosentezinin erken basamaklarında defektlere sahip bakteriyel
mutantların
yaĢayamadıklarını
biliyoruz.
Tüm
bu
araĢtırmaların
sonunda,
endotoksinlerin olumlu ve olumsuz etkilerinin altında yatan mekanizmalar ve
bunların moleküler organizasyonunu dahi iyi anlamak adına çok büyük geliĢmeler
kaydedilmiĢtir (Petsch ve Anspach, 2000; Heumann ve Roger, 2002).
1.3.
Endotoksinlerin Fiziko-Kimyasal Özellikleri
Lipopolisakkaritler olarak da adlandırılan endotoksinler, Gram negatif bakterilerin
dıĢ membranının ana bileĢenidir (Kirikae ve ark., 1998). Bakterilerin sitoplazmik
membranında lipopolisakkarit veya lipoprotein yapısında bulunurlar. Bu bileĢikler,
bakterileri dıĢ ortama karĢı korumak ve yarı geçirgen bir membran oluĢturmak için
tasarlanmıĢlardır. Bunlar hidrofobik bir lipid parçasına kovalent olarak bağlanan bir
hidrofilik polisakkarit parçasından oluĢmuĢtur (Raetz ve ark., 1991; Hirayama ve
Sakata, 2002; Ogikuba ve ark., 2004). Pek çok türün lipopolisakkaridi 3 farklı
bölgeden oluĢur (ġekil 1):
0 - antijen bölgesi,
Oligasakkarit bir çekirdek
Lipid A (Lip A)
6
Bakteri yüzeyi
Şekil 1. Lipopolisakkaritlerin yapısı
Lipid A, endotoksinlerde en yoğun bulunan ve en sağlam bölgedir (Vaara ve
Nurminen 1999; Petsch ve Arspach, 2000) ve birçok yağ asiti ile her biri eĢleĢmiĢ iki
fosforilat gruptan (glukozamin) oluĢur (Ryan, 2004). Bu bölge, toksisite de dahil
olmak
üzere
endotoksinin
pek
çok
biyolojik
aktivitesinden
sorumludur.
Endotoksinler 12-16 karbon atomuna sahip bir 3-hidroksi asil grubuna amin ve ester
bağlarıyla bağlanmıĢ b-1, 6-D glikozamin rezidülerinden oluĢurlar. Bunlar doymuĢ
yağ asitleriyle esterlenebilirler. Endotoksinlerin bu hidrofobik kısmı hekzagonal bir
düzen içerisinde bulunur. Bu da molekülün geri kalan kısmına göre daha sert bir yapı
oluĢmasına sebep olur (Stanislavsky ve ark., 1997; Petsch ve Anspach, 2000; Lin ve
ark., 2005). Lipid A veya endotoksinden yoksun suĢ bilinmemektedir.
Çekirdek
oligosakkariti
bir
iç
3-deoksi-D-manno-2-oktulosonik
asit
(KDO) - heptoz bölgesi ve bir dıĢ hekzoz bölgesinden oluĢan bir yapıyla korunur.
E. coli türlerinde 5 değiĢik çekirdek tipi bilinmektedir. Çekirdek bölgesi Lipid A‟ya
çok yakındır ve Lipid A‟nın kendisi kısmen fosforilatlanmıĢtır. Böylelikle
endotoksin molekülleri protein solüsyonları içinde net elektriksel negatif yük
sergilerler (Hou ve Zaniewski, 1990; Petsch ve Anspach, 2000).
0 - antijeni genellikle identik oligosakkaritlerin bir dizininden oluĢurlar.
Bunlar suĢlara spesifiktir ve serolojik kimliğin belirleyicisidirler (Petsch ve Anspach,
7
2000). Memelilerde Gram negatif etkenlerin neden olduğu enfeksiyonlarda bağıĢıklık
sağlanması sırasında spesifik antikor yanıtından sorumludur (Kessel ve ark., 1966).
Bir
endotoksin
monomerinin
molar
kütlesi
oligosakkarit
zincirinin
değiĢkenliğine bağlı olarak 10-20 kDa arasında değiĢir. Endotoksinlerin amfipatik
yapıları sebebiyle akıĢkan solüsyonlar içerisinde değiĢik supramoleküler agregatlar
(çöküntü) oluĢturduğu iyi bilinmektedir. Bu agregatlar lipid zincirleri arasındaki
kutupsal olmayan etkileĢimlerin yanısıra fosfat grupları arasında oluĢturulan
köprülerin bir sonucu olarak da meydana gelebilirler (Anspach, 2001). Bu
agregatların yapıları elektron mikroskobu, X-ray difraksiyonu, FT-IR spektroskopisi
ve NMR gibi değiĢik tekniklerle çalıĢılmıĢtır. Bu çalıĢmaların sonucunda akıĢkan
sıvılarda endotoksinlerin lamel, kübik, ve hekzagonal gibi değiĢik Ģekillerde, 0,1 mm
çapında ve 1000 kDa büyüklüğüne kadar değiĢik Ģekillerde bulunabileceği ve bu
Ģekillerin solüsyonun özelliklerine (pH, iyonlar, sürfaktantlar vs.) bağlı olarak
yüksek stabilitede olabileceği ortaya konmuĢtur (Darkow ve ark., 1999). Moleküler
dinamik kurallarına göre endotoksinin 3 boyutlu yapısı, özellikle uzun yüzey antijeni
proteinlerin globüler yapısına göre çok daha esnektir.
Endotoksinler bakteri ölümünün yanı sıra bakteri bölünmesi ve üremesi
sırasında da yüksek miktarda salınırlar. Bunlar yüksek oranda ısıya dayanıklıdırlar ve
bilinen sterilizasyon koĢullarında yok edilemezler. Endotoksinler 250°C'de
30 dakikadan fazla veya 180°C'de 3 saatten fazla tutuldukları zaman inaktive olurlar
(Ryan, 2004; Gorbet ve Sefton, 2006). E. coli LPS‟i 170-250°C‟de kuru sıcak hava
ile yok edilebilir (Tsuji ve Harrison, 1978). Hecker ve ark. (1994) ise, bakteriyal
endotoksinlerin kuru sıcak havada 200°C‟de 60 dk bekletilmesiyle yoğunluklarının
3 log düĢtüğünü tespit etmiĢlerdir. En az 0,1 M oranındaki asit ve alkaliler de
endotoksinleri yok etmek için kullanılabilir (Magalhães ve ark., 2007).
8
1.4.
Endotoksinlerin Etki Mekanizması
Endotoksinlerin oluĢturduğu doku hasarı, Ģok ve ölüm gibi fizyopatolojik etkileri
oldukça çeĢitlilik gösterir (Ogikubo ve ark., 2004). Endotoksinler hücre ve organlar
üzerine direkt etki etmezler, fakat bunun yerine, monosit ve makrofajlar baĢta olmak
üzere immun sistemin aktive edilmesiyle ve dolayısıyla immun yanıtın artırılması ile
etki gösterirler. Bu durum, aktive edilen immun sistem hücrelerinden özellikle tümör
nekroz faktör (tNF), birçok interlökinler, prostoglandinler, koloni sitümüle edici
faktörler, trombosit aktivite edici faktörler ve serbest radikaller gibi mediyatörlerin
salınmasına sebep olur (Forehand ve ark., 1989; Rietschel ve ark., 1994; Magalhães
ve ark., 2007). Bu mediyatörler güçlü biyolojik aktiviteye sahiptir ve endotoksinlerin
oluĢturduğu
yan
etkilerden
sorumludur.
Organ
ve
hücrelerin
yapı
ve
fonksiyonlarında meydana getirdiği değiĢiklikler arasında metabolik fonksiyonda
değiĢiklikler, vücut ısısında artma, koagülasyon aktivitesi, hemodinamiklerin
değiĢimi ve Ģok indüksüyonu sayılabilir. Ġmmun sistem hücreleri üzerine
endotoksinlerin zararlı etkilerini önlemek veya tedavi etmek, bunun yanı sıra
anti-endotoksin antikorlarının kullanımını ve endotoksin reseptör antagonistlerini
bloklamak için birçok araĢtırma yapılmıĢtır (Loppnow ve ark., 1989; Golenbock ve
ark., 1991; Pugun ve ark., 1995). Bununla birlikte endotoksinlerin immun hücreler
ile etkileĢimine sadece spesifik reseptörler aracılık etmez. Hücre etkileĢimleri aynı
zamanda hedef hücrelerinin membranlarının içine endotoksin moleküllerinin
non spesifik interkalasyonu ile de meydana gelebilir (Schromm ve ark., 2000).
LPS'lerin moleküler aktiviteleri, LPS molekülünün kendisinden kaynaklanmaz.
Bunun yerine endotoksinin, LPS'lere duyarlı hücrelerle etkileĢimi sonucu üretilen
medyatörler tarafından indirekt olarak indüklenir (Galanos ve Freudenberg, 1993).
Maktofajların,
LPS
molekülünün
Lipid
A
bölümü
tarafından
indüklenen
aktivasyonu, biyoaktif lipidlerin, reaktif oksijen türlerinin ve özellikle de tümör
nekroz faktörü α (TNF α), interleukin-1 (IL-1), IL-6, IL-8 ve IL-10 gibi peptit
mediyatörlerinin üretilmesine yol açar (Vogel ve Hogan, 1990). Yapılan çalıĢmalar
LPS'in tam bir endotoksik aktivite gösterebilmesi için Lipid A bölgesinin iki
9
heksozamin rezidüsü (D-gluko olarak konfigüre olmuĢ), iki fosforil grubu,
3-asiloksiasil grupları içeren 6 adet yağ asidi (doymuĢ, kısmen 3-hidroksilatlanmıĢ)
içermesi gerektiğini ortaya koymuĢtur (Rietschel ve ark., 1994).
Konakçının endotoksinlere bağlanma özelliğine sahip bazı plazma proteinleri,
endotoksinlerin aktivitesini etkileyebilir (artırabilir veya baskılayabilir). Bu plazma
proteinleri arasında yüksek ve düĢük yoğunluklu lipoproteinler (HDL ve LDL) ve
LPS-bağlanma proteini sayılabilir (Schuhmann ve ark., 1990). Enfeksiyondan
kaynaklanan
endotoksin Ģoku
durumlarında,
enfeksiyonu meydana
getiren
mikroorganizmadan salgılanan LPS'nin toksik etkisi, Omp A gibi bakteriyel
proteinlerden de etkilenebilir (Freudenberg ve ark., 1991).
Endotoksinlerin az miktarları, memelilerin normal intestinal florası olarak
yaĢayan Gram (-) bakterilerden salındığında organizmalar için olumlu etkiye sahip
olabilir. Enfeksiyona karĢı vücut ısısında artma, bakteriyal, viral enfeksiyonlar,
tümör nekrozuna karĢı savaĢma gibi yararlı etkiler görülür (Bui, 2012).
Sonuç olarak, endotoksinlerin yararlı etkilere de sahip olabileceği göz ardı
edilmemelidir. Bu yararlı etkiler yüksek ateĢin tedavisinde, tümörlerin yok
edilmesinde ve non-spesifik olarak immun yanıtın geliĢtirilmesinde kullanılmaktadır
(Golenbock ve ark., 1991; Pugun ve ark., 1995).
Öte yandan komplikasyonların önüne geçmek için endotoksine herhangi bir
Ģekilde maruz kalınmasından kesinlikle kaçınılmalıdır. Bu durum özellikle damar içi
verilen ilaçlar için geçerlidir.
10
1.5.
Endotoksinlerin Tespit Yöntemleri
Endotoksinler, su, serum ve vasatlara karıĢtığında aĢı ve biyolojik maddelerin
kalitesini olumsuz etkilemektedir (Geier ve Geier, 2002). Bunun baĢlıca sebebi
olarak, özellikle aĢı ve biyolojik madde hazırlamada kullanılan hücre kültürlerinde
meydana getirdiği toksik etki ve sulandırma sıvılarına karıĢması durumunda da
kullanıcıya olan etkisi gösterilebilir. Bu olumsuzlukların önüne geçmek için, GMP
laboratuvar Ģartlarının bir maddesi, endotoksin varlığının tespit edilmesi gerektiğini
vurgulamaktadır. Dolayısıyla endotoksinlerin üretim aĢamasının baĢında tespit
edilmesi çok önemlidir.
Endotoksin kontaminasyonların tespiti için ilk metot, insanlara enjekte edilecek
su ve solüsyonların taranması için 1940‟larda geliĢtirilen TavĢan Pirojen Testidir.
Bang 1956 yılında, Gram negatif bakterilerin öldürüldüklerinde dahi at nalı
yengecinin kanını yarı katı bir kütle haline çevirdiğini bildirmiĢtir. Bu geliĢmeden
sonra, 1970‟lerde bu mekanizmaya dayanan Limulus Amebocyte Lysate (LAL) testi
geliĢtirilmiĢtir. (Ryan, 2004; Sargent, 2002).
Geier ve ark. (1978) beĢeri uygulamalar için hazırlanmıĢ çiçek, rubella,
poliomyelitis, kuduz, influenza, kabakulak, difteri ve kolera aĢılarından oluĢan
20 örneğin 16'sında endotoksin miktarının 0,1 ng/ml‟den daha fazla olduğunu ve bu
aĢılarda endotoksin içeriğinin 10-5 dilüsyona kadar varlıklarını koruduğunu LAL testi
ile göstermiĢlerdir. Bu durumun aĢılarda yan etki oluĢturabileceğini ve en az
endotoksin varlığına sahip aĢı lotlarının seçiminin, bu yan etkileri azaltacağını
vurgulamıĢlardır.
Limulus polyphemus adı verilen at nalı yengecinin kanından (amoebocytes)
elde edilen ekstraktın Gram negatif bakterilerin endotoksinleri ile reaksiyona girmesi
ve pıhtı meydana getirmesi testin ana prensibini oluĢturmaktadır (Bui, 2012).
11
Günümüzde biyolojik materyallerde endotoksinlerin tespiti, tavĢan pirojen
testi, jel klot LAL yöntemi, türbidimetrik LAL yöntemi, kromojenik LAL yöntemi ve
floresan yöntemi ile yapılabilmektedir. LAL testinin endotoksinlerin tespitinde
kullanılan en hassas test olduğu bilinmektedir (Hussaini ve Ready, 1981). Dahası bu
test 0,03 EU/ml altındaki miktarları tespit edebilme özelliğindedir (Bates ve ark.,
1998; Ryan, 2004). Test sonuçlarının kolay okunabilir olması, pH değiĢikliklerine ve
glikanlara karĢı dirençli olması ve ticari olarak ihtiyaca yönelik değiĢik miktarlarının
var olması ve en önemlisi testin duyarlılığının yüksek olması sebebiyle günümüzde
endotoksinlerin tespitinde LAL testi daha çok tercih edilmektedir.
Trivedi ve ark. (2003), standardize edilmiĢ 14 allerjen aĢının endotoksin
içeriğini LAL testi ile incelemiĢler ve aĢıların endotoksin içeriklerinin çok farklı
olduğunu bulmuĢlardır.
Geier ve Geier (2002), ticari aĢılarda endotoksin tespitine yönelik yaptıkları bir
çalıĢmada endotoksin düzeylerini LAL testi ile tespit etmiĢler ve endotoksin düzeyi
ile yan etkilerin korelasyonunu incelemiĢlerdir. Sonuç olarak, aĢılardaki endotoksin
miktarları ile oluĢan yan etkilerin insidensi arasında doğru orantı olduğunu
göstermiĢlerdir.
Sonuç olarak; ticari aĢılarda ve biyolojik maddelerde endotoksinlerin varlığını
takip etmek ve bunları bildirmek, bu ürünleri kullanan bireylerde oluĢabilecek yan
etkilerin kaynağını daha iyi anlamak açısından yararlı olacağı düĢünülmektedir.
Bunun yanı sıra, endotoksin içeriği az olan aĢıların tercih edilmesi, oluĢabilecek yan
etkilerin önüne geçmeye yardımcı olacaktır (Bilgehan, 2000).
Biyolojik maddelerdeki kabul edilebilir endotoksin yoğunlukları
de gösterilmiĢtir (Hoffmann ve ark., 2005).
Çizelge 1.
12
Çizelge 1. ÇeĢitli maddelerde kabul edilebilir endotoksin miktarları.
Madde
Plastik kültür ekstraktları
Ticari hücre kültürü vasatı
Makrofaj kültürleri
Endotelyal hücre kültürleri
1.6.
EU / ml
0,5
˂ 1,0
0,8
˂ 0,5
Hücre Hatları ve Bakteri Suşları
1.6.1. Vero Epitelyal Hücre Hattı
Japonya‟da 1962 yılında Yasumura ve Kawakika tarafından normal, yetiĢkin Afrika
yeĢil maymununun böbrek hücrelerinden türetilmiĢtir. Epitelyal hücre hattıdır.
Mikroskopta genellikle düz, kübik Ģekilli, tek nükleuslu, hücre boyunca uzamıĢ
sitoplazmik görüntüye sahip, düzgün hatlı hücreler Ģeklinde görülür (Montagnon,
1989; Hay, 1991; Govorkova ve ark., 1995; Lindl ve Steubing, 2013).
Bu hücre hattı pek çok amaçla kullanılmaktadır. Vero hücrelerinin diğer hücre
hatlarına göre daha sık kullanılmasının ana nedenlerinden biri kolay depolanabilmesi
ve karakterize edilebilmesidir. Bu da üretimin partiler halinde üretilmesi sırasında
primer hücre kültürlerinin taze olarak hazırlanıp kullanılmasından kaynaklanabilecek
kontaminasyonların önüne geçer. Diploid hücre kültürlerine göre daha fazla
kullanılırlar. Bunun sebebi ise Vero hücreleri biyoreaktörler içerisinde üretilmeleri
sırasında kolay adapte olurlar ve bunun sonucunda daha fazla virüs elde edilir. Daha
fazla virüs elde edilmesi de aĢının daha saf olmasına neden olur (hücre atıkları daha
az olur). AĢının üretim partileri büyür, sonuç olarak da aĢı ekonomik olarak üretilir.
Tüm bu anlatılanlar göz önüne alındığında Vero hücreleri virüs üretimi için konak
hücresi konumundadır. Bunlara ek olarak, E. coli toksinlerinin taranmasında
kullanılmaktadır (Montagnon, 1989; Geier ve ark., 2002).
13
Konowalchuk ve ark., (1977), E. coli sitotoksinine karĢı Vero hücresinin
yanıtını incelemiĢler ve Vero hücresinde oluĢan önemli değiĢiklikleri göstermiĢlerdir.
Carbonell ve ark., (1997), Serratia marcescens‟in klinik izolatlarının Vero
hücresinde sitotoksik aktivitenin etkilerini araĢtırmıĢlar ve Vero hücrelerinde
büzüĢme olmadan yuvarlaklaĢma, birbirinden ayrılma gibi sitotoksik etkiler
saptamıĢlardır.
1.6.2. Baby Hamster Kidney (BHK-21) Fibroblast Hücre Hattı
Macpherson ve Staker tarafından 1962‟de geliĢtirilen fibroblast karakterde bir hücre
hattıdır. Mikroskopta genellikle düz, oval Ģekilli bir nükleuslu, hücre boyunca uzamıĢ
stoplazmik görünüme sahip, mekik Ģekilli hücreler Ģeklinde görülür (Drexlor ve ark.,
1998; Lindl ve Steubing, 2013).
1.6.3. Madin-Darby Bovine Kidney (MDBK) Epitelyal Hücre Hattı
YetiĢkin bir sığırın (Bos Taurus) böbrek dokusundan 1957 yılında geliĢtirilen
epitelyal hücre hattıdır. Özellikle viral kontaminantların tespitinde kullanılan bir
hücre hattıdır.
Bu epitel hücre hattı dünya çapında çok değiĢik uygulamalar için
laboratuvarlarda kullanılmaktadır. Fakat belki de bunlar içerisinde en belirgin olanı
aĢı üretimi için attenue virusları çoğaltmak için kullanılmasıdır (Hay, 1991; Forrester
ve ark., 1992; Erdem, 1999).
14
1.6.4. Pseudomonas aeruginosa
Pseudomonas
aeruginosa
Gama
protobacteria
sınıfının
bir
üyesidir.
Pseudomonadaceae familyasının Pseudomonas cinsinin en iyi tanımlanan türüdür
(Sears ve Kaper, 1996; Vahapoğlu ve Akhan, 2002).
P. aeruginosa, Gram negatif, zorunlu aerobik, çomak Ģeklinde (Koneman ve
ark., 2006), düz veya hafif kıvrık yapıda, sporsuz, 0,5-0,8×1,5-3,0 μm boyutlarında,
uçlarında tek nadiren 2-3 adet flagellası olan hareketli bir organizmadır (Berker ve
Hold, 1983; Dawson, 1998; Akalın, 2004). Adi besiyerinde kolayca üreyebilen
P. aeruginosa‟nın kültürdeki aromatik meyve kokusu karakteristiktir (Dawson,
1998). Nötral pH da mavi veya yeĢilimsi mavi görülür. Bu pigmentten dolayı
aeruginosa adı verilmiĢtir (Berker ve Hold, 1983; Hoffmann ve ark. 2005).
P. aeruginosa, MacConkey agarda laktoz negatif koloniler oluĢturur (Dawson,
1998). Ġzolasyonu için 24-48 saat yeterlidir.
P. aeruginosa su, toprak ve bitkiler üzerinde bulunan çevresel kaynaklı
saprofitik bir etkendir (Hoadley ve McCoy, 1968; Akalın, 2004; Esendal, 2006).
P. aeruginosa enfeksiyonları, etkenin oportunistik olması nedeniyle, genellikle yara
(yaralarda mavi yeĢil irin), yanık, kornea zedelenmesi, deride oluĢan paraziter ve
mikotik enfeksiyonlar, özellikle koyunlarda yapağının aĢırı ıslanması, kötü hijyenik
koĢullar gibi faktörlerin varlığında ortaya çıkmaktadır (Akalın, 2004; Freshney,
2005).
Endotoksin sentezleyerek sığır, koyun, keçi, domuz, at, kedi ve köpeklerde
hastalık oluĢturur. Özellikle sığırlarda mastitis, endotoksemi ve bazen ölüm;
infertilite, sporadik abort görülür (Johne ve ark., 1987). Koyun ve keçilerde ise
yapağı çürüdüğünde tel tel ayrılır, dermatit geliĢir ve kötü koku oluĢur.
P. aeruginosa‟nın yaĢam skalasının geniĢ olması ve oluĢturduğu infertilite ve
ölümler sebebiyle ciddi ekonomik kayıplara neden olmaktadır (Hay, 1991).
15
Mushin ve Ziv (1973), sığırlar ve diğer hayvanlar üzerinde yaptıkları
çalıĢmada, hastalıkların hayvanlarda meydana gelme nedeninin P. aeruginosa ile
kontamine olmuĢ suların sebep olduğunu bildirmiĢlerdir.
1.6.5. Escherichia coli
E. coli, Enterobacteriaceae ailesi içinde yer alan Escherichia cinsinin en önemli
türüdür. Gram negatif, çomak Ģeklinde, sporsuz, 1-2 × 0,1-0,5 µm boyutlarında,
peritrik flagellaya sahip olması sebebiyle hareketli, bazen hareketsiz, fakültatif
anaerob bir bakteridir. Optimum üreme ısısı 37°C‟dir. Özellikle 44°C‟de üremesiyle
diğer bakterilerden ayrılmasını sağlarlar.
Peng ve ark., (2013), E. coli‟nin çeĢitli suĢlarının özellikle çiğ sütlerde ısı ile
inaktivasyon derecelerini incelemiĢlerdir. Bu araĢtırıcılar, araĢtırmaların sonucunda
E. coli‟nin çoğu suĢunun 67.5°C ve bunun üzerindeki sıcaklıklarda inaktive
olduğunu göstermiĢlerdir.
Endotoksinler E. coli‟nin bütün suĢlarında bulunur. E. coli‟nin antijenik yapısı
çok komplike olup, patojen suĢlarda bu yapılar önem taĢımaktadır. Bu yapılardan biri
somatik “O” antijenidir. Bu antijen lipopolisakkarit özelliğinde olup, ısıya dirençli
yüzey antijenleridir. Protein – fosfolipit – polisakkarit yapısında olan “O” somatik
antijeninin polisakkarit fraksiyonları antijeniteyi belirlerken, lipoproteinler toksisiteyi
belirlerler (Ġzgür, 2006).
E. coli, normal bağırsak florası olarak memeli ve kanatlıların kalın
bağırsaklarında bulunurlar. Fakat canlı savunma gücünün azaldığı durumlarda doku
ve kana yayılarak enfeksiyon etkeni özelliği taĢırlar Canlı vücudunda ve doğada
yaygın
bulunması
sebebiyle
suları
kontamine
etme
riski
yüksektir.
Bu
mikroorganizmanın çevresel sularda tespit edilmesi dıĢkı kirlenmesinin bir belirtisi
olarak kabul edilir (Bekar, 1997).
16
E. coli ve P. aeruginosa, doğada çok yaygın bulunmaları ve zayıf besi yeri
koĢullarında
bile
kolayca
üreyebilmeleri
sebebiyle
baĢlıca
laboratuvar
kontaminantları olarak kabul edilmektedir. Hele ki bu özelliklerini hücre kültürü
çalıĢmalarının yürütüldüğü laboratuvar koĢullarında gösterdiklerinde, gerek araĢtırma
ve gerekse hücre kültürü kökenli biyolojik ürünlerin üretilmesi sırasında ciddi
problemlere yol açmaktadır. Özellikle sterilizasyon, dezenfeksiyon ve sanitasyon
koĢullarının yetersiz olduğu laboratuvar koĢullarında kolayca üreyerek hücre
hatlarının kontamine olmasına yol açmakta ve bu da ciddi maliyet ve iĢ gücü kaybına
yol açabilmektedir.
Bu çalıĢmada, bakteri endotoksinlerinin varlıkları Jel klot LAL testi ile tespit
edilerek, aĢı üretiminde kullanılan Vero, MDBK, BHK-21 gibi hücre hatlarına
etkilerinin deneysel olarak araĢtırılması ve bunun yanı sıra, çalıĢma süresince hücre
hatlarında meydana gelen sayısal ve morfolojik değiĢikliklerin belirlenmesi ve
kıyaslanması hedeflenmiĢtir.
17
2. GEREÇ VE YÖNTEM
2.1. GEREÇ
2.1.1. Bakteri Suşları
2.1.1.1. P. aeruginosa Suşu
Ankara Üniversitesi Veteriner Fakültesi Mikrobiyoloji Anabilim Dalı Kültür
Koleksiyonu'ndan Pseudomonas aeruginosa ATCC 27853 suĢu olarak temin edildi.
2.1.1.2. E. coli Suşu
E. coli O55:B5 suĢu Etlik Veteriner Kontrol Merkez AraĢtırma Enstitüsü
Bakteriyoloji Laboratuvarı Kültür Koleksiyonu'ndan saf kültür olarak temin edildi.
P. aeruginosa ve E. coli suĢlarının saflığının gösterilmesi amacıyla Mikro API
cihazı, P. aeruginosa 32 GN (Kat. no: 32100) (BIOMERIEUX) ve E. coli ID 32 E
(Kat no: 32400) kiti (BIOMERIEUX) kullanıldı.
18
2.1.2. Hücre Hatları
2.1.2.1.Vero Epitelyal Hücre Hattı
Etlik Veteriner Kontrol Merkez AraĢtırma Enstitüsü Viral AĢı Üretim Laboratuvarı
Hücre Koleksiyonu'ndan Vero CIRAD-EMVT-Fransa (174. pasaj) temin edildi.
2.1.2.2. Baby Hamster Kidney (BHK-21) Fibroblast Hücre Hattı
Etlik Veteriner Kontrol Merkez AraĢtırma Enstitüsü Viral AĢı Üretim Laboratuvarı
Hücre Koleksiyonu'ndan BHK-21 ATCC (Kat no: CCL-10) (60. pasaj) temin edildi.
2.1.2.3. Madin-Darby Bovine Kidney (MDBK) Epitelyal Hücre Hattı
Etlik Veteriner Kontrol Merkez AraĢtırma Enstitüsü Viral AĢı Üretim Laboratuvarı
Hücre Koleksiyonu'ndan MDBK ATCC (Kat no: CCL-22) (11. pasaj) temin edildi.
2.1.3. Besiyerleri
2.1.3.1. Nutrient Agar
P. aeruginosa ve E. coli suĢlarının üretimi amacıyla genel besiyeri olarak OXOID
CM003 kullanıldı. Besiyeri 28 gr / 1000 ml olacak Ģekilde hazırlandı. PH 7.4±0,2‟ye
ayarlandı. Otoklavda 121°C‟de 15 dk sterilize edildi. Besiyeri sıcaklığı 56ºC‟ye
gelince petrilere dağıtıldı. Hazırlanan petrilerin sterilite kontrolü için 37°C etüvde 24
saat inkübasyondan sonra kullanılıncaya kadar +4°C‟de buzdolabında muhafaza
edildi.
19
2.1.3.2. Nutrient Broth
P. aeruginosa ve E. coli suĢlarının üretimi amacıyla genel besiyeri olarak OXOID
CM001 kullanıldı. Besiyeri 13 gr / 1000 ml olacak Ģekilde hazırlandı. pH 7.4±0,2‟ye
ayarlandı. Tüplere eĢit miktarda dağıtıldı. Otoklavda 121°C‟de 15 dk sterilize edildi.
Hazırlanan broth'ların sterilite kontrolü için 37°C etüvde 24 saat inkübasyondan
sonra kullanana kadar +4°C‟de buzdolabında muhafaza edildi.
2.1.3.3. Kanlı Agar
E. coli suĢunun üretimi amacıyla genel besiyeri olarak nutrient agar (OXOID
CM003) kullanıldı. Besiyeri 28 g / 1000 ml olacak Ģekilde hazırlanarak ve pH‟ı
7.3‟e ayarlandı ve 121ºC‟de 15 dk sterilize edildi. Besiyeri sıcaklığı 45–50ºC‟ye
gelince içerisine %25‟lik glikozdan %5 oranında ilave edildi. Benmaride 10 dk
bekledikten sonra %7 oranında defibrine taze koyun kanı eklendi. Petrilere eĢit
Ģekilde dağıtıldı. Etüvde 24 saat inkübasyona bırakılarak kontaminasyon kontrolü
yapıldı. +4°C‟de buzdolabında saklandı.
2.1.3.4. Hücre Üretme Vasatı
Hücrelerin çoğalmasını desteklemek amacıyla vasat olarak %10 fötal dana serumu
(FCS) (BIOCHROM AG) destekli Eagle Minimal Essential Medium (EMEM)
(SIGMA – ALDRICH) kullanıldı.
20
2.1.4. Tripsin ve EDTA
Hücre hatlarının çoğaltılması iĢlemlerinde flask içinde üremiĢ hücrelerin, üreme
yüzeyinden
kaldırılmasını
sağlamak
amacıyla
%0,4
EDTA‟lı
(Ethylenediaminetetraacetic acid) tripsin (SIGMA–ALDRICH) kullanıldı. BHK-21
hücre hattının çoğaltma iĢlemlerinde ise EDTA içermeyen tripsin kullanıldı.
2.1.5. Trypan Blue Boyası
Endotoksinlerin hücre sayısına etkisinin tespiti amacıyla trypan blue boyası (BDH
stains) 25 g / 1000 ml olacak Ģekilde hazırlandı.
2.1.6. LAL Test Kiti
Bu çalıĢmada endotoksin varlığının tespiti için ġap Enstitüsü Müdürlüğü‟nden temin
edilen LAL test (Pyrotell) kiti ve non pirojen su (Pyrotell) kullanıldı. Kit kullanım
aĢamasına kadar -20°C‟de saklandı.
2.1.7. ELISA Reader Cihazı
Hücre kültürü tabletlerin her bir gözündeki hücrelerin canlılığının belirlenmesi için
ELISA reader cihazı (OLYMPUS IX71) kullanıldı. Pleytler 630 nm‟de okutuldu.
21
2.1.8. Sarf Malzemeleri
ÇalıĢma sırasında kullanılan tüm sarf malzemeler (su, serum, vasat, pipet, pipet ucu,
dilüsyon tüpleri, konteynerlar vs.) non pirojen özellikte kullanıldı.
2.2. YÖNTEM
2.2.1. P. aeruginosa ve E. coli Suşlarının Çoğaltılması
Ankara Üniversitesi Veteriner Fakültesi Mikrobiyoloji Anabilim Dalı Kültür
Koleksiyonu'ndan temin edilen P. aeruginosa suĢunun Macconkey agara ve Nutrient
agara ekimi yapıldı. Etlik Veteriner Kontrol Merkez AraĢtırma Enstitüsü
Bakteriyoloji Laboratuvarı Kültür Koleksiyonu'ndan temin edilen E. coli suĢunun
EMB agara ve Nutrient agara ekimi yapıldı. Etüvde 24 saat inkübasyona bırakıldı.
2.2.2. Mikro API Cihazı ile Suşların Saflığının Gösterilmesi
Çoğaltılan bakteri kültürlerinin saflığının gösterilmesi amacıyla Mikro API cihazı
kullanıldı. Bakteri kültürleri kit prosedürüne uygun olarak iĢleme alındı. Buna göre
aĢağıdaki adımlar uygulandı.
Nutrient agarda üreyen P. aeruginosa olduğu düĢünülen bakteri öze ile
alınarak özel solüsyonunda, Mc Farland 0,5 yoğunluğuna göre ayarlandı.
KarıĢım vortexlendi.
Kitteki her bir göze ayarı yapılmıĢ sıvıdan (Mc Farland) 135 µl hacminde
konuldu.
24 ± 2°C‟de etüvde 24 saat inkübe edildi.
Mikro API cihazı ile sonuçlandırıldı.
Çıkan özellikler olması gereken özelliklerle kıyaslanarak sağlaması yapıldı.
22
2.2.3. Suşların Çoğaltılması
Mikro API cihazı ile saflığı gösterilen E. coli ve P. aeruginosa suĢlarını çoğaltmak
için nutrient agarlara ekimleri yapıldı. Ekimi yapılan petriler 37°C etüvde 24 saat
inkübe edildi ve çoğaltma iĢlemi tamamlandı.
2.2.4. Koloni Sayım Yöntemi ile Bakteri Sayımı
P. aeruginosa ve E. coli‟nin stok kültüründe 1 ml'de ortalama ne kadar bakteri
olduğunu hesaplamak için P. aeruginosa ve E. coli suĢları nutrient broth'da çoğaltıldı
ve orijinal kültür olarak kabul edildi ve 1 ml nutrient broth içindeki yaklaĢık bakteri
sayısı, koloni sayım tekniğine göre hesaplandı. Bu tekniğe göre 9 ml nutrient broth
bulunan dilüsyon tüpleri hazırlandı. Birinci dilüsyon tüpüne 1 ml bakteri üremiĢ
nutrient brothdan eklendi ve her bir bakteri için 10-1‟den 10-9‟a kadar 10 katlı
sulandırmalar yapılarak dilüsyon iĢlemi tamamlandı ve her iki bakteri için iĢlem
tekrar edildi. Yapılan 10 katlı dilüsyonlar iyice karıĢtırıldı. 10-1‟den 10-7 dilüsyona
kadar her dilüsyon 0,1 ml nutrient agara ekildi. Son üç dilüsyonun (10-7, 10-8, 10-9)
her birinden ayrı ayrı pipet ucu kullanmak kaydıyla 3‟er adet nutrient agara 0,1 ml
miktarında ekimler yapıldı ve besiyeri üzerine yüzeyi kaplayacak Ģekilde yayıldı.
ĠĢlem gören petri kutuları 37°C‟de 24 saat inkubasyona bırakıldı. Yirmidört saat
sonunda her dilüsyon için yapılan 3 petri kutusundaki bakteriler sayıldı ve ortalaması
alındı. Orijinal kültürdeki P. aeruginosa ve E. coli sayısını hesaplamada aĢağıdaki
formülden yararlanıldı (Arda, 2011).
Burada;
= Orijinal stok kültürdeki (sulandırılmamıĢ) bakteri sayısı
= Petri kutularına ekilen inokulum miktarı (0,1 ml)
= Ortalama bakteri sayısı
= Dilüsyonunun ters logaritması
23
Her dilüsyonun 1 ml‟sinde koloni miktarı bulunduktan sonra sonuçların
ortalaması alındı. Böylece, P. aeruginosa ve E. coli‟nin stok kültüründe 1 ml'de
ortalama ne kadar bakteri olduğu belirlendi.
2.2.5. Endotoksinlerin Açığa Çıkarılması
Nutrient agarda çoğaltılan P. aeruginosa ve E. coli suĢlarının her biri öze yardımıyla
agar üzerinden tamamen toplandı. Her bir bakteri birer tüp içerisindeki 50 ml non
pirojen su içinde süspanse edildi. Önceden 95°C‟de ısıtılmıĢ benmari içerisine bu iki
tüp yerleĢtirildi. Benmaride 95°C‟de 30 dk bekletildi ve sonunda tüpler benmariden
çıkartıldı. Soğumaya bırakıldı (Ludwig ve Avis, 1988).
2.2.6. Sterilite Kontrolü
Vasat üretme suyunda parçalanmadan kalan bakteriler hazırlanan hücrede
kontaminasyona sebep olacağından dilüsyon iĢleminden önce bakteri kontrolü
yapılması gerekmektedir. Endotoksin çıkartma iĢlemi tamamlandıktan sonra soğuyan
P. aeruginosa ve E. coli endotoksinlerine sahip stok solüsyonlarından öze yardımıyla
nutrient agara ekim yapıldı. 37°C etüvde 24 saat inkübe edildi. Ġnkübasyon sonunda
üreme olup olmadığına bakıldı.
2.2.7. Jel Klot LAL Testi ile Stok Solüsyonlarında Endotoksinlerin Tespiti
Bu çalıĢmada, P. aeruginosa ve E. coli stok solüsyonu içindeki açığa çıkan
endotoksini tespit etmek için stok solüsyonlarına Jel Klot LAL testi uygulandı. ĠĢlem,
kit prosedüründe belirtilen talimatlara uygun olarak yapıldı.
24
2.2.8. Jel klot LAL Testi ile Endotoksin Yoğunluğunun Saptanması
Bu amaçla, stok solüsyonlarından non pirojen tüpler içerisine, non pirojen su ile 10
katlı seri dilüsyonlar hazırlandı. Dilüsyon iĢlemi boyunca non pirojen pipet ucu
kullanıldı ve 900 µl non pirojen su içinde 100 µl bakteri endotoksinli stok dilüe
edildi. Böylelikle her bir bakteri suĢu endotoksini için 10 katlı seri dilüsyonlar
hazırlanmıĢ oldu. Daha sonra, hazırlanan bu endotoksin dilüsyonlarında endotoksin
yoğunluğunu tespit etmek amacıyla Limulus amebocyte lysate (LAL) testi kullanıldı.
Test, kit protokolüne uygun Ģekilde yapıldı. Buna göre aĢağıdaki adımlar uygulandı.
Limulus amebocyte lizatı içine 2 ml non pirojen su eklendi.
0.1 ml test örneği veya kontrol içeren her bir reaksiyon tüpüne 0.1 µl LAL
lizatı eklendi. Ekleme sırasında iyi bir karıĢımın olması için tüpler 20-30 sn boyunca
çalkalandı.
Reaksiyon tüpleri 37°C±1°C‟de bir su banyosu veya etüvde 1 saat bekletildi.
Test numunesine LAL lizatı eklendiği anda reaksiyon baĢladı. Fakat karıĢımın
optimum orana ulaĢabilmesi için 37°C‟ye gelmesi beklendi.
60 dk'nın sonunda tüpler alındı.
OluĢan jel görünümüne göre endotoksin değerlendirildi (Çizelge 2).
Çizelge 2. Jel Klot LAL test protokolüne göre testin değerlendirmesi
Endotoksin miktarı
0.5 EU/mL
0.25 EU/mL
0.125 EU/mL
0.06 EU/mL
Endotoksin varlığı
+
+
-
2.2.9. Hücre Kültürlerinin Çoğaltılması
Vero, MDBK ve BHK-21 hücreleri %10 FCS içeren EMEM vasatı içerisinde 75
cm2‟lik hücre kültürü kaplarına konuldu. Monolayer hücre üremesi sağlandı.
25
2.2.10. Hücre Üretme Vasatları İçerisinde Stok Solüsyonlardan Endotoksinli
Seri Dilüsyonların Hazırlanması
Jel Klot LAL testi ile belirlenen endotoksin varlığının olmadığı son dilüsyon
basamağının bir üstünü de kapsayacak Ģekilde (10-1, 10-2, 10-3, 10-4) hücre üretme
vasatı ile logaritma 10 tabanına göre endotoksin dilüsyonları her kullanımdan önce
hazırlandı.
2.2.11. Hücre Kültürlerinin 96 Gözlü Pleytlere ve Hücre Kültürü Flasklarına
Aktarılması
Daha önceden 75 cm2‟lik flasklarda monolayer üremesi tamamlanmıĢ hücre
hatlarının, endotoksinli vasatlarla subkültürleri yapılarak 96 gözlü pleytlere ve
25 cm2 lik flasklara dağıtılması sağlandı. Bu amaçla, her bir bakteri endotoksini için,
endotoksin varlığının olmadığı son dilüsyon basamağının bir üstünü de içerecek
Ģekilde 96 gözlü pleyt ve 25 cm2'lik flask sayısı belirlendi. Hücrelerin hücre üretme
vasatıyla subkültürü yapılarak pleyt ve flasklara pay edilmesi sağlandı. Prosedür Ģu
metodolojiye göre gerçekleĢtirildi.
Monolayer durumda bulunan ve 75 cm2‟lik flasklarda üretilmiĢ hücre
kültürlerinin (Vero, MDBK, BHK-21) içerisindeki hücre üretme vasatı döküldü.
Vasat ile hücrelerin yüzeyleri yıkandı.
Hücrelerin tripsin ile flask yüzeyinden ayrılması sağlandıktan sonra EMEM
ile pipetasyonu yapılarak birbirlerinden ayrılması sağlandı.
Daha sonra hemositometrik yöntem ile Thoma lamında sayılan hücreler,
(MDBK, BHK-21 ve Vero için ayrı ayrı) 125.000 hücre/ml olacak Ģekilde EMEM ve
%10 FCS‟li hücre üretme vasatı içinde sulandırıldı. Hazırlanan hücreler 96 gözlü
pleytlerin her bir gözüne 0,1 ml hacminde ve 25 cm2 lik flasklara ise 10 ml hacminde
dağıtıldı (Freshney, 2005).
26
2.2.12. 96 Gözlü Pleytler ve Flasklardaki Vasatların Endotoksinli Vasatlar ile
Değiştirilmesi
Hücre hatlarının E. coli ve P. aeruginosa endotoksinlerine sürekli maruz kalmasını
sağlamak amacıyla pleyt ve flasklardaki hücreler hergün endotoksinli taze vasatlarla
değiĢtirildi. ĠĢlem, Pöllänen ve ark. (2000)'nın belirttiği yönteme göre yapıldı. Bu
amaçla; öncelikle flask ve pleytlere dağıtılan hücrelerin (MDBK,
BHK-21 ve
Vero için ayrı ayrı) pleyt ve flask yüzeyine yapıĢmasını sağlamak amacıyla 24 saat
boyunca 37°C ve %5 CO2‟li etüvde inkübe edildi. Ġnkübasyon sonunda pleyt ve
flasklardaki hücre üretme vasatları steril bir pipet ile çekildi ve bunların yerine, her
bir bakteri endotoksini için % 2 FCS içeren 10-1, 10-2, 10-3 ve 10-4 oranlarında
endotoksin ihtiva eden vasatlar ilave edildi. Endotoksinli vasatlar ile yapılan bu
değiĢim iĢlemi 5 gün boyunca devam etti.
2.2.13. Morfolojik Değişikliklerin Saptanması
Endotoksinli vasatlarla vasat değiĢimi yapılan hücre hatları hergün doku kültürü
mikroskobunda
morfolojik
değiĢiklikler
yönünden
kontrol
hücreleriyle
karĢılaĢtırılarak incelendi ve değiĢiklikler kaydedildi. Hücrelerde meydana gelen
toksik etkiler, Brown‟ın (1982) bildirdiği yönteme göre değerlendirildi. Bu yönteme
göre;
0 = Negatif yanıt. Normal hücre morfolojisi.
+1 = Kontrolle kıyaslanabilir görüntü mevcut fakat granülasyonda azalma veya
%25‟den daha az hücrelerin azalması (hafif ĢiĢme veya krenasyon), granüllerin
varlıkları yokken tek tek hücrelerin morfolojik değiĢimi.
+2 = YaklaĢık bütün Monolayer hücrelerde büzüĢme ve krenasyon, genellikle
hücrelere granülasyon eĢlik eder; yüzen ölmüĢ hücreler mevcut olabilir.
+3 = AĢırı granülasyon veya büzüĢme veya krenasyon. Her durumda da
%50-75 hücre kaybı
27
+4 = Hücrelerde %75‟den daha fazla kayıp ve ciddi morfolojik değiĢim (bu
kültür hala metabolik aktivite sergileyebilir)
2.2.14. Kristal Viyole Boyama Yöntemi ile Endotoksinlerin Hücre Canlılığına
Etkisinin Tespiti
Canlı
hücrelerin
tespiti
ve
bunların
kantitatif
miktarsal
olarak
tayinini
gerçekleĢtirmek amacıyla 96 gözlü pleytlerde üretilen hücreler boyandı ve her bir
gözdeki boya miktarı ELISA okuyucu ile Optik Dansite (OD) birimi olarak
belirlendi. Deney prosedürü Pöllänen ve ark. (2000) belirttiği yönteme göre
yapılmıĢtır.
Hücre kültürü tabletlerindeki hücre üretme vasatı döküldü.
96 gözlü pleytlerin her bir gözüne 100 µl %5 sükroz içeren PBS içerisinde
hazırlanmıĢ %4‟lük formaldehit solüsyonu içerisinde 1 gece boyunca fikzasyona
bırakıldı.
Fikzasyon sonunda pleytlerin içerisindeki solüsyon boĢaltıldı.
4 kez distile su ile yıkandı, durulandı ve kurutuldu.
96 gözlü pleytlerin her bir gözü, %0,1 borik asit içeren 100 µl hacmindeki
kristal viyole ( 200mM, pH 6,0 ) ile boyandı.
Oda sıcaklığında 30 dk bekletildi.
Süre sonunda gözlerdeki boya boĢaltıldı.
4 kez distile su ile yıkandı, durulandı ve kurutuldu.
Pleytlerin her bir gözüne konulan boya miktarı kadar (100µl) %10 asetik asit
konularak boya almıĢ canlı hücrelerdeki boya çözdürüldü.
Çözünen boya miktarı ELISA reader ile 630 nm‟de okutuldu.
Değerlendirme; Boya alan hücre sayısı ile orantılı olarak OD değerleri yüksek
olan gözlerde canlı hücre miktarının daha yüksek olduğu kabul edildi.
28
2.2.15. Trypan Blue Boyama Yöntemi ile Endotoksinlerin Hücre Sayısına
Etkisinin Tespiti
25
cm2‟lik
flasklarda
üretilen
monolayer
hücre
kültürlerinin
endotoksin
uygulanmadan önceki ve uygulamadan sonraki canlı/ölü hücre sayısının belirlenmesi
ve karĢılaĢtırması için hücreler trypan blue boyama yöntemiyle sayıldı. Test
prosedürü Altman ve ark. (1993) bildirdiği yönteme göre yapıldı. Prosedüre göre;
Trypan blue boyası (BDH stains) 25 g / 1000 ml olacak Ģekilde hazırlandı.
25 cm2‟lik flasklarda monolayer hücre kültürü olarak çoğaltılan hücrelerin
yüzeyinden vasat yavaĢça boĢaltıldı.
Vasat ile yüzeyi yıkandı ve yıkama vasatı boĢaltıldı.
Yüzeye 4 ml tripsin eklendi ve 37°C‟de 2 dk etüvde inkübe edildi.
Flask içerisine 2 ml vasat eklendi ve hücrelerin birbirinden ayrılması için
pipetasyon yapıldı.
500 µl hücre ve 500 µl trypan blue boyası ile bir tüp içerinde karıĢtırıldı.
5 dk oda sıcaklığında bekletildi. (Canlı hücreler boya almazken ölü hücreler
boya alır).
Hemositometre üzerine 1‟er damla damlatıldı.
Doku kültürü mikroskobunda 100X‟lük objektifle ölü ve canlı hücrelerin
sayımı gerçekleĢtirildi.
1 ml‟deki canlı ve ölü hücre sayısı aĢağıda verilen formüle göre hesaplandı.
Canlı/ölü hücre sayısı = Sayılan canlı/ölü hücre x Dilüsyon faktörü x Toplam
hacim
29
3. BULGULAR
3.1. Bakterilerin Çoğaltılması
Nutrient agara ekilen ve inkübasyona bıraklan P. aeruginosa ve E. coli O55:B5
suĢları 24 saat sonunda koloni oluĢumları gösterdi.
3.2. Mikro API Cihazı ile Suşların Saflığının Gösterilmesi
Üreyen kolonilerin saflığını göstermek için Mikro API cihazı kullanıldı. SuĢların P.
aeruginosa suĢu ve E. coli suĢu olduğu tespit edildi.
3.3. Koloni Sayım Yöntemi ile Bakteri Sayımı
Koloni Sayım Yöntemi ile gerçekleĢtirilen bakteri sayımı sonucunda;
P. aeruginosa için mililitredeki bakteri sayısı;
10-9 dilüsyonun 0,1 ml sinde yaklaĢık olarak ortalama koloni 270 sayıldı.
Orijinal süspansiyonun 1 ml sinde, ortalama;
göre
109= 270 x 1010 = 2700 x 109 cfu bakteri /ml
E. coli için mililitredeki bakteri sayısı ise;
10-9 dilüsyonun 0,1 ml sinde yaklaĢık olarak ortalama koloni 53 olarak
sayıldı. Orijinal süspansiyonun 1 ml sinde, ortalama;
30
109= 53 x 1010 = 530 x 109 cfu bakteri / ml
göre
olarak bulundu.
Gerek P. aeruginosa ve gerekse E. coli için bakteri sayım sonuçları
Çigelge 3. de özetlenmiĢtir.
Çizelge 3. P. aeruginosa ve E. coli için bakteri sayım sonuçları
Bakteri
P. aeruginosa
E. coli
Diüsyon
-9
1. petri
2. petri
3. petri
Toplam
Ortalama
Koloni
Koloni
Bakteri sayısı
(cfu
bakteri/ml)
10
248
164
400
812
270,6
2700x109
10-9
56
60
44
160
53,3
530x109
3.4. Endotoksinli Stok Solüsyonlarının Sterilite Testleri
Endotoksinlerin açığa çıkartılması sırasında parçalanmadan kalan bakteriler,
hazırlanan hücre sistemlerinde kontaminasyona sebep olabileceğinden, tekrar
nutrient agara ekimleri sonucunda; her iki suĢa ait besiyerlerinde 24 saat sonunda
üreme olmadığı, bütün bakterilerin parçalanmıĢ olduğu ve süspansiyonların steril
olduğu saptandı.
3.5. Jel Klot LAL testi ile Endotoksin Kontrolü
Testin sonucu pozitif olarak bulundu ve stok solüsyonlarında endotoksin varlığı teyid
edildi.
31
3.6. Çalışmada Kullanılacak Dilüsyon Basamaklarının Belirlenmesi
Her bir sulandırma basamağına uygulanan Jel Klot LAL testi sonucunda; kullanılan
her bir bakteri suĢu için endotoksin tespit edilen son sulandırma basamağı 10-3 olarak
belirlendi. Bir diğer deyiĢle 10-3 dilüsyon basamağındaki endotoksin miktarı yaklaĢık
0.25 EU/mL olarak belirlendi.
Her bir hücre hattı için iĢleme alınacak endotoksin yoğunlukları ise; her iki
bakteri için endotoksin varlığının bittiği son basamak (10-1,10-2, 10-3) ve onun bir
üstü (10-4) olarak belirlendi. Bütün çalıĢmalar kontrollü deney metodolojisine uygun
olarak gerçekleĢtirildi.
3.7. Hücre Hatlarının Endotoksinle Muamele Öncesi Sayısal Değerleri
Kristal viyole boyama ve ELISA reader ile canlılığın tespit edilmesi için ayrılan 96
gözlü pleytlerde gerek Vero (174. pasajda), gerek MDBK (11. pasajda) ve gerekse
BHK-21 (60. pasajda) hücre hatlarında hücre miktarı, 125.000 hücre/ml olarak
kullanıldı.
Trypan blue boyama ve hemositometrede ölü/canlı hücre sayımı yapılması için
ayrılan 25 cm2 flasklarda ise hücre hatlarının endotoksinlere maruz bırakılmadan
önceki miktarları aĢağıdaki gibi tespit edildi:
Vero P174 hücresi 590.000 hücre/ml
MDBK P11 hücresi 670.000 hücre/ml
BHK-21 P60 hücresi 370.000 hücre/ml
32
3.8. Hücre Morfolojisindeki Değişiklikler
Bütün iĢlem görmüĢ Vero, MDBK ve BHK-21 hücreleri her gün kontrol hücresiyle
kıyaslanarak, 100X, 200X ve 400X‟lük büyütme ile doku kültürü mikroskobunda
morfolojik yönden incelendi.
Buna göre; en fazla morfolojik değiĢimin görüldüğü hücre hattının Vero (+2)
hücre hattı olduğu tespit edildi. Morfolojik değiĢikliklerin 2. günde (+1) meydana
gelmeye baĢladığı ve 5. günde en üst seviyeye ulaĢtığı gözlemlendi. P. aeruginosa
endotoksini
ile
muamele
edilen
Vero
hücrelerinde
hücre
duvarında
ve
sitoplazmasında silikleĢme, intrasitoplazmik granülasyon ve vakuol oluĢumları
gözlemlenirken (Resim 1), E. coli endotoksini ile muamele edilen hücrelerde üst üste
katlanmalar ve yine intrastoplazmik granülasyonlar gözlemlendi (Resim 2).
Resim 1: (A) P. aeruginosa (10-1 dilüsyon) endotoksini uygulanmıĢ Vero hücre
hattının görüntüsü x 100. (B) Vero hücre kontrol x 100.
A
Vakuol
Granülasyonlar
Silikleşme
B
33
Resim 2: (A) E. coli (10-1dilüsyon) endotoksini uygulanmıĢ Vero hücre
hattının görüntüsü x 100. (B) Vero hücre kontrol x 100.
A
Katlanmalar
B
Her iki bakterinin endotoksini ile muamele gören MDBK hücreleri
incelendiğinde ise; morfolojik açıdan herhangi bir değiĢiklik (0) gözlemlenmedi
(Resim 3).
Resim 3: (A) P. aeruginosa (10-1 dilüsyon) endotoksini uygulanmıĢ MDBK
hücre hattının görüntüsü x 100. (B) MDBK hücre kontrol x 100.
A
B
BHK-21 hücresi incelendiğinde ise; endotoksin uygulanan hücreler ile kontrol
hücreleri arasında morfolojik olarak belirgin bir fark görülmemekle birlikte (0),
P. aeruginosa endotoksinine maruz kalan BHK-21 hücrelerinin (10-1 dilüsyon
basamağı) kontrol hücrelerine nazaran mekik Ģekilli görüntünün kısaldığı ve flask
yüzeyini kaplama oranında farklılık olduğu gözlemlenmiĢtir.
34
3.9. Kristal Viyole Boyama Yöntemi ile Endotoksinlerin Hücre Canlılığına
Etkisinin Tespiti
Yapılan testlerin sonucunda, P. aeruginosa endotoksini uygulanmıĢ Vero, MDBK,
BHK-21 hücreleri için ELISA sonuçları ġekil 2.A, 2.B ve 2.C‟de verilmiĢtir.
Grafikler incelendiğinde OD değerlerinin Vero hücrelerinde 2,426 ile 1,772 arasında
değiĢtiği ve en belirgin farkın (0.654) 10-1 ve kontrol hücreleri arasında olduğu
belirlendi. MDBK da ise Vero‟ya benzer bir Ģekilde doğrusal bir azalma olduğu ve
yine belirgin farkın (0.166) 10-1 ve kontrol hücreleri arasında olduğu belirlendi.
Ancak BHK-21 hücrelerine ait OD değerleri incelendiğinde herhangi bir doğrusal
azalma olmadığı ve OD değerleri arasındaki farkların ve dolayısıyla hücre
canlılığının endotoksin yoğunluğundan etkilenmediği saptandı.
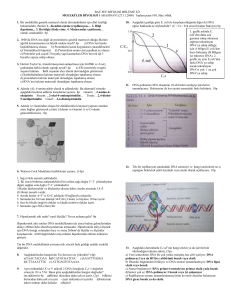
Şekil 2.A. P. aeruginosa endotoksini uygulanmıĢ Vero hücre hattında tespit
edilen ELISA sonuçları
Aktüel OD
OD Değeri
0,654
1,772
-1
Kontrol arası fark
0,401
0,157
0,077
2,025
2,269
2,349
2,426
-2
-3
-4
Kontrol
Endotoksin Konsantrasyonu
35
Şekil 2.B. P. aeruginosa endotoksini uygulanmıĢ MDBK hücre hattında tespit
edilen ELISA sonuçları
OD Değeri
Aktüel OD
Kontrol arası fark
0,015
0,014
0,006
1,909
1,91
1,918
1,924
-2
-3
-4
Kontrol
0,166
1,758
-1
Endotoksin Konsantrasyonu
Şekil 2.C. P. aeruginosa endotoksini uygulanmıĢ BHK-21 hücre hattında tespit
edilen ELISA sonuçları
OD Değeri
Aktüel OD
1,078
0,973
0,929
-1
-2
-3
0,939
0,931
-4
Kontrol
Endotoksin Konsantrasyonu
E. coli endotoksini uygulanmıĢ Vero hücrelerinde ELISA sonuçları
incelendiğinde de benzer Ģekilde, OD değerlerinde endotoksin yoğunluğu ile hücre
sayısı arasında ters orantı olduğu ve kontrol hücresiyle kıyaslandığında en az hücre
canlılığının 10-1 dilüsyon basamağında olduğu tespit edildi (ġekil 3.A). MDBK ve
BHK-21 hücre hatlarına ait OD değerleri incelendiğinde ise herhangi bir doğrusal
azalma olmadığı ve OD değerleri arasındaki farkların dilüsyondan dilüsyona
değiĢtiği saptandı (ġekil 3.B ve 3.C).
36
Şekil 3.A. E. coli endotoksini uygulanmıĢ Vero hücre hattında tespit edilen
ELISA sonuçları
OD Değeri
Aktüel OD
Kontrol arası fark
0,085
0,066
0,02
2,159
2,178
2,224
2,244
-2
-3
-4
Kontrol
0,305
1,939
-1
Endotoksin Konsantrasyonu
Şekil 3.B. E. coli endotoksini uygulanmıĢ MDBK hücre hattında tespit edilen
ELISA sonuçları
Aktüel OD
OD Değeri
0,026
Kontrol arası fark
0,031
0,057
0,049
1,885
1,859
-1
1,854
-2
1,828
1,836
-3
-4
Endotoksin Konsantrasyonu
Kontrol
37
Şekil 3.C. E. coli endotoksini uygulanmıĢ BHK-21 hücre hattında tespit edilen
ELISA sonuçları
OD Değeri
Aktüel OD
0,966
1,002
0,934
0,906
0,833
-1
-2
-3
-4
Kontrol
Endotoksin Konsantrasyonu
3.10. Trypan Blue Boyama Yöntemi ile Endotoksinlerin Hücre Sayısına
Etkisinin Tespiti
Trypan Blue Boyama yöntemiyle boyanan ve Thoma lamında hemositometrik
yöntemle sayılan Vero, MDBK, BHK-21 hücre hatlarına ait canlı/ölü hücre sayıları
ve bunların toplam hücre sayısına göre yüzdeleri Çizelge 4, 5 ve 6‟te verilmiĢtir.
Çizelge 4. Vero hücre hattında canlı/ölü hücre sayıları ve toplam hücre sayısına
göre yüzdesi
Ġnokulum
Vero Hücre Sayısı
Sulandırma
Canlı hücre
P. aeruginosa
Stok Solüsyonu
Sulandırmaları
Stok Solüsyonu
Sulandırmaları
hücre
10
-1
36 (%92)
3 (%8)
10
-2
41 (%93)
3 (%7)
10
-3
48 (%96)
2 (%4)
10-4
60 (%95)
3 (%5)
-1
37 (%93)
3 (%7)
10-2
45 (%94)
3 (%6)
-3
50 (%96)
2 (%4)
10-4
63 (%94)
4 (%6)
10
E. coli
Ölü
10
Kontrol
Canlı hücre
Ölü hücre
65 (%98)
1 (%2)
65 (%98)
1 (%2)
38
Bunun yanı sıra, Thoma lamında sayılan canlı ve ölü hücre sayısı her iki
bakteri suĢuna ait endotoksinler ile muamele edilmiĢ Vero, MDBK ve BHK-21 hücre
hatlarına ait mililitredeki canlı ve ölü hücre sayıları herbir dilüsyon basamağı için
ayrı ayrı hesaplanmıĢtır. Buna göre her iki endotoksine ait Vero hücre hattındaki
veriler Çizelge 4, ġekil 4.A ve B de verilmiĢtir.
Şekil 4.A. P. aeruginosa endotoksini uygulanmıĢ Vero hücre hattının
1 ml‟sinde tespit edilen canlı ve ölü hücre sayıları
Endotoksin konsantrasyonu
-1
Canlı hücre sayısı
Ölü hücre sayısı
360.000
30.000
410.000
-2
30.000
480.000
-3
20.000
600.000
-4
30.000
650.000
Kontrol
10
1 ml'deki canlı ve ölü hücre sayısı
Şekil 4.B. E. coli endotoksini uygulanmıĢ Vero hücre hattının 1 ml‟sinde tespit
edilen canlı ve ölü hücre sayıları
Endotoksin konsantrasyonu
Canlı hücre sayısı
-1
-2
-3
-4
Kontrol
Ölü hücre sayısı
370.000
30.000
450.000
30.000
500.000
20.000
630.000
650.000
1 ml'deki canlı ve ölü hücre sayısı
40.000
30.000
39
Çizelge 5. MDBK hücre hattında canlı/ölü hücre sayıları ve toplam hücre
sayısına göre yüzdesi
Ġnokulum
Vero Hücre Sayısı
Sulandırma
Canlı hücre
Ölü hücre
10-1
26 (%93)
2 (%7)
Stok
10
-2
35 (%97)
1 (%3)
Solüsyonu
10-3
43 (%93)
3 (%7)
10
-4
44 (%88)
6 (%12)
10
-1
33 (%97)
1 (%3)
10
-2
31 (%94)
2 (%6)
Solüsyonu
10
-3
30 (%97)
1 (%3)
Sulandırmaları
10-4
33 (%97)
1 (%3)
P. aeruginosa
Sulandırmaları
E. coli
Stok
Kontrol
Canlı hücre
Ölü hücre
44 (%100)
0
33 (%100)
0
Yukarıdaki tablo sonuçları ele alınarak 25 cm2 flask içerisinde monolayer
üretilen P. aeruginosa ve E. coli endotoksini uygulanmıĢ MDBK hücresinin
1 ml'deki canlı ve ölü hücreleri ġekil 5.A, 5.B gösterilmiĢtir.
Şekil 5.A. P. aeruginosa endotoksini uygulanmıĢ MDBK hücre hattının
1 ml‟sinde tespit edilen canlı ve ölü hücre sayıları
Endotoksin konsantrasyonu
Canlı hücre sayısı
-1
-2
260.000
Ölü hücre sayısı
20.000
350.000
-3
430.000
-4
440.000
Kontrol
440.000
10.000
1 ml'deki canlı/ölü hücre sayısı
30.000
60.000
40
Şekil 5.B. E. coli endotoksini uygulanmıĢ MDBK hücre hattının 1 ml‟sinde
tespit edilen canlı ve ölü hücre sayıları
Endotoksin konsatrasyonu
Canlı hücre sayısı
330.000
-1
310.000
-2
-3
Ölü hücre sayısı
300.000
10.000
20.000
10.000
-4
330.000
10.000
Kontrol
330.000
10.000
1 ml'deki canlı/ölü hücre sayısı
Çizelge 6. BHK-21 hücre hattında canlı/ölü hücre sayıları ve toplam hücre
sayısına göre yüzdesi
Vero Hücre Sayısı
Ġnokulum
P. aeruginosa
Stok Solüsyonu
Sulandırmaları
E. coli
Stok Solüsyonu
Sulandırmaları
Sulandırma
Canlı hücre
Ölü hücre
10-1
9 (%92)
2 (%8)
-2
7 (%70)
3 (%30)
10-3
12 (%71)
5 (%29)
10
-4
23 (%79)
6 (%21)
10
-1
17 (%81)
4 (%19)
10
-2
16 (%80)
4 (%20)
10
-3
9 (%69)
4 (%31)
19 (%83)
4 (%17)
10
10-4
Kontrol
Canlı hücre
Ölü hücre
28 (%100)
0
11 (%92)
1 (%8)
Yukarıdaki çizelgeye göre P. aeruginosa ve E. coli endotoksini uygulanmıĢ
BHK-21 hücresinin 1 ml'deki canlı ve ölü hücrelere ait veriler ġekil 6.A ve B de
gösterilmiĢtir.
41
Şekil 6.A. P. aeruginosa endotoksini uygulanmıĢ BHK-21 hücre hattının
1 ml‟sinde tespit edilen canlı ve ölü hücre sayıları
Endotoksin konsantrasyonu
Canlı hücre sayısı
-1
-2
-3
90.000
70.000
Ölü hücre sayısı
20.000
30.000
120.000
50.000
230.000
-4
60.000
280.000
Kontrol
1 ml'deki canlı/ölü hücre sayısı
Şekil 6.B. E. coli endotoksini uygulanmıĢ BHK-21 hücre hattının 1 ml‟sinde
tespit edilen canlı ve ölü hücre sayıları
Endotoksin konsantrasyonu
Canlı hücre sayısı
170.000
-1
90.000
40.000
40.000
190.000
-4
Kontrol
40.000
160.000
-2
-3
Ölü hücre sayısı
110.000
10.000
1 ml'deki canlı/ölü hücre sayısı
40.000
42
4. TARTIŞMA
Bakteriyal endotoksinler hücre kültürlerinde kullanılan ana materyallerin sıkça
rastlanan kontaminantlarıdır. Bu endotoksinler çeĢitli sebeplerle su, serum ve
vasatlara karıĢtığında biyolojik maddelerin kalitesini olumsuz etkileyebildiği bilinen
bir gerçektir (Geier ve Geier, 2002). Özellikle oluĢabilecek ürün kayıpları
neticesinde ciddi ekonomik kayıplar meydana gelebileceği gibi iĢ gücü kaybına da
yol açabilmektedir. Bu maddelerin organizmadaki varlığı ise, yoğunluğuna bağlı
olarak hafifden ağıra kadar değiĢen fizyopatolojik sonuçlar doğurur (Bui, 2012). Bu
fizyopatolojilerin
ana
sebebini
endotoksinlerin
immün
sisteminden
çeĢitli
medyatörlerin salınmasına sebep olması oluĢturur (Forehand ve ark., 1989; Rietschel
ve ark., 1994).
Bu çalıĢmada, bakteri endotoksin varlıkları jel klot LAL testi ile tespit edilerek,
aĢı üretiminde kullanılan Vero, MDBK, BHK-21 gibi hücre hatlarına etkisinin
deneysel olarak araĢtırılması ve bunun yanı sıra çalıĢma süresince hücre hatlarında
meydana gelen sayısal ve morfolojik değiĢikliklerin belirlenmesi ve kıyaslanması da
amaçlanmıĢtır.
Günümüzde gerek biyolojik materyallerde ve gerekse biyolojik araĢtırmalarda
kullanılan maddelerde endotoksinlerin varlığını tespit etmek için birçok test
kullanılmakta ve var olanların üzerine yenileri geliĢtirilmektedir. Bunların baĢında
ELISA prensibini kullanılarak geliĢtirilen endotoksin testleri ve organizmada
pirojenlere verilen yanıtı taklit eden monosit aktivasyon testleri yer almaktadır.
Ancak bu tip testler spesifik ve hassas olmakla birlikte maliyetleri yüksektir.
Endotoksinleri ve diğer pirojenleri tespit etmek için kullanılan bu teknikler birçok
araĢtırmanın konusunu oluĢturmuĢ ve testlerin kendi aralarında karĢılaĢtırmaları
yapılmıĢtır. Yapılan bu bilimsel araĢtırmalar ve bunlardan elde edilen veriler
değerlendirildiğinde, biyolojik materyallarde endotoksin tespiti için jel klot LAL
testinin gerek spesifik ve hassas olması ve gerekse kısa sürede yanıt alınarak gözle
değerlendirilebilmesi ve maliyetinin düĢük olması sebebiyle halen en değerli araç
43
olduğu anlaĢılmaktadır (Asakawa ve ark. 1994; Joiner ve ark., 2002; Park ve ark.,
2005; Schindler ve ark., 2009). Bu gerçek, araĢtırmamızda endotoksinlerin tespiti
için jel klot LAL testinin kullanılmasında belirleyici faktör olmuĢtur.
ÇalıĢmamızda endotoksinlerini kullandığımız P. aeruginosa ve E. coli
suĢlarının nutrient agarda çoğaltılması sonucunda stok kültürde bakteri sayıları
mililitrede sırasıyla
2700x109 ve 530x109 cfu bakteri/ml olarak hesaplandı.
Çoğaltılan bu bakterilerin inaktive edilerek endotoksinlerinin açığa çıkarılması
sonucunda gerçekleĢtirilen jel klot LAL testi, hazırlanan süspansiyonlarda 10-3
dilüsyon basamağına kadar endotoksin varlığını tespit etmiĢtir. Dolayısı ile jel klot
LAL testinin hassasiyetine bağlı olarak, 10-3 dilüsyon basamağındaki endotoksin
miktarı yaklaĢık 0.25 EU/mL olarak kabul edilmiĢtir. ÇalıĢmamızda toksik etkilerini
araĢtırdığımız endotoksinlerin tüm sulandırmalarının (10-1, 10-2 ve 10-3) uluslararası
kabul edilebilir limitlerin üzerinde endotoksin içerdiği ve yukarıda sayısal değerleri
verilen bakteri yoğunluklarının Hoffmann ve ark. (2005)'nın belirttiği kabul edilebilir
limitlerin çok üzerinde endotoksin içerdiği sonucuna varılmıĢtır.
AraĢtırmamızda Vero hücre hattının
P. aeruginosa ve E. coli‟nin
endotoksinlerinin farklı yoğunluklarına karĢı verdiği morfolojik ve fizyolojik cevaba
iliĢkin bulgular değerlendirildiğinde;
Vero hücre hattında morfolojik olarak, 1. gün hücre morfolojisinde gözle
görülür bir değiĢiklik saptanmamakla birlikte, 2. günden itibaren kontrol hücreleri ile
kıyaslandığında, endotoksin uygulanmıĢ hücrelerde, endotoksinin yoğunluğu ile
doğru orantılı olarak hücre stoplazmasında vakuol oluĢumları ve granülasyonlar
gözlemlenmiĢtir (Resim 1). Ayrıca P. aeruginosa endotoksini Vero hücrelerinde
silikleĢme Ģeklinde etki gösterirken, E. coli endotoksini uygulanan hücrelerde ise üst
üste katlanmalar gözlemlenmiĢtir (Resim 2). Elde edilen bu bulgular Konowalchuk
ve ark. (1977)'nın bulduğu sonuçlarla paralellik göstermektedir. Bu araĢtırıcılar
E. coli sitotoksinine karĢı Vero hücre hattının yanıtını incelemiĢler ve Vero
hücrelerinde benzer değiĢikliklerin olduğunu göstermiĢlerdir. Dawson (1998) ise
44
hücre membranları ile endotoksinlerin etkileĢimleri sonucunda hücrede meydana
gelebilecek değiĢimleri, özellikle hücre membranında dalgalanma, sitoplazmada
büyük vakuol oluĢumları ve hücre membranında ciddi hasarlar meydana geldiğini
göstererek vurgulamıĢtır. Benzer Ģekilde, Carbonell ve ark. (1997), Serratia
marcescens‟in klinik izolatlarının Vero hücresinde sitotoksik aktivitesinin etkilerini
araĢtırmıĢlar ve Vero hücrelerinde büzüĢme olmadan yuvarlaklaĢma, birbirinden
ayrılma gibi sitotoksik etkiler saptamıĢlardır.
Vero hücre hattının E. coli ve P. aeruginosa endotoksinine verdiği fizyolojik
yanıtı belirlemek için kullanılan kristal viyole ve trypan blue boyama teknikleriyle
elde edilen veriler incelendiğinde; Kristal viyole testinde ortaya çıkan OD değerleri
(ġekil 2.A ve 3.A); endotoksin yoğunlukları ile canlı hücre yoğunluğunun arasında
ters
orantı
olduğunu
ortaya
koymuĢtur.
Dolayısıyla,
kontrol
hücreleriyle
kıyaslandığında en az hücre yoğunluğunun yoğun endotoksin konsantrasyonuna
maruz bırakılmıĢ hücrelerde olduğu gözlenmiĢtir. Bu veriler doğrultusunda kontrol
gözlerindeki canlı hücre yoğunluğunun, yüksek endotoksin konsantrasyonu
uygulanmıĢ hücrelere göre daha fazla olduğu sonucuna varılmıĢtır.
Diğer taraftan, endotoksinlerin Vero hücre hattında trypan blue boyama ile
hemositometrik canlı/ölü hücre sayımı sonucunda meydana gelen ölüm ve canlılık
oranlarına ait veriler, E. coli ve P. aeruginosa endotoksini uygulanmıĢ Vero
hücrelerinde en az canlı hücre sayısının 10-1 dilüsyon basamağında olduğu tespit
edilmiĢtir. Bununla birlikte, ilginç olarak, değiĢik endotoksin yoğunluklarında ölü
hücre sayısında herhangi bir değiĢim meydana gelmediği gözlenmiĢtir (ġekil 4.A ve
4.B).
Vero hücrelerinin endotoksin varlığına verdiği bu yanıtlar göz önüne
alındığında, özellikle hücre sayısının azalmasına rağmen ölü hücre oranın
değiĢmemesi, endotoksinlerin bu hücre hattında hücre ölümüne değil de, hücre
mitozuna olumsuz etki ettiğini düĢündürmektedir.
45
AraĢtırmamızda MDBK hücre hattının P. aeruginosa ve E. coli‟nin
endotoksinlerinin farklı yoğunluklarına karĢı verdiği morfolojik ve fizyolojik cevaba
iliĢkin bulgular değerlendirildiğinde; Morfolojik olarak endotoksinlerin farklı
yoğunluğuna maruz bırakılmıĢ MDBK hücre hatlarında mikroskobik olarak hücre
morfolojisinde gözle görülür bir değiĢiklik saptanmamıĢtır (Resim 3).
MDBK hücre hattının E. coli ve P. aeruginosa endotoksinine verdiği fizyolojik
yanıtı belirlemek için kullanılan kristal viyole ve trypan blue boyama teknikleriyle
elde edilen veriler incelendiğinde ise, gerek hücre yoğunlukları ve gerekse canlı/ölü
hücre oranları baz alındığında, bu iki endotoksinin MDBK hücreleri üzerine olan
etkisinin farklı olduğu tespit edilmiĢtir (ġekil 2.B, 3.B, ġekil 5.A, 5.B). Buna göre,
P. aeruginosa endotoksinine maruz bırakılan MDBK hücrelerinin, dilüsyon
basamakları arasındaki OD değerlerinin birbirine yakın olduğu tespit edilmekle
birlikte, hücre yoğunluklarının Vero‟ya benzer bir Ģekilde doğrusal bir azalma
gösterdiği ve yine belirgin farkın 10-1 ve kontrol hücreleri arasında olduğu
belirlenmiĢtir (ġekil 2B). Yine P. aeruginosa endotoksinlerinin aynı hücre hattında
meydana getirdiği ölüm ve canlılık oranının saptanması amacıyla yapılan trypan blue
boyama yöntemi ile sayılan canlı hücre sayısının, endotoksin yoğunluğunun
artmasıyla birlikte azaldığı saptanmıĢtır. Ölü hücre sayısının değiĢmemesi ise yine
dikkat çekici bir bulgu olarak kaydedilmiĢtir (ġekil 5A). Bu verilere paralel olarak
Fujioka ve Akema (2010) çalıĢmalarında, lipopolisakkaritlerin, olgun sıçanların
dental gyruslarındaki nöral öncü hücrelerin ölümünü artırmadığını, fakat çoğalmasını
engelleyerek
akut
olarak
baskıladığını
göstermiĢlerdir.
Forbes
(1965),
endotoksinlerin makrofajların mitoz bölünmesine etkisini araĢtırdığı çalıĢmasında,
endotoksinlerin veya bunların metabolizması sonucu oluĢan ürünlerin makrofajlarda
geri dönüĢümsüz hasara yol açtığını öne sürmüĢtür.
Malik ve ark. (1995)'nın Salmonella serovarlarının sitotoksik etkisini
araĢtırdığı çalıĢmalarında ise, MDBK ve Vero hücre hatlarında farklı serovarların
farklı sitotoksik etki gösterdiğini ve hücrelerdeki bu etkilerin doza bağlı olduğunu
gözlemlemiĢlerdir.
46
Aynı hücre hattının E. coli endotoksinin değiĢik yoğunluklarına verdiği
cevabın değiĢken olduğu gözlenmiĢtir. Yapılan testler sonucunda gerek kristal viyole
ve gerekse trypan blue boyama yöntemi sonucunda canlı hücre yoğunluklarının ve
ölü/canlı hücre sayısının endotoksin yoğunluklarına bağlı olmaksızın değiĢken
olduğu belirlenmiĢtir (ġekil 4B, 6B). Buna göre, MDBK hücre hattının E. coli
endotoksinine karĢı daha dirençli olduğu düĢünülmüĢtür. Varılan bu sonucu destekler
nitelikte, yapılan araĢtırmalarda çeĢitli bakteri endotoksinlerinin farklı hücre
hatlarında etki derecesinin değiĢken olduğu bildirilmiĢtir. (Harlan ve ark. 1983;
Reitmeyer ve Peterson, 1988; Dawson, 1998). Bunlara ek olarak, Berjis ve Green
(1986) tümorojenik MDCK (Madin-Darby canine kidney) T1 hücrelerinde
L- canavin‟in seçici sitotoksitite çalıĢmalarında, toksin uygulanan tumorojenik
MDCK T1 hücrelerinin büyüme oranlarında herhangi farklılık olmadığını
bildirilmiĢtir.
ÇalıĢmada BHK-21 hücre hattının endotoksine verdiği morfolojik ve fizyolojik
cevap diğer iki hücre hattına göre daha değiĢken olmuĢtur. Bu hücre hattının her gün
doku kültürü mikroskobunda yapılan incelemelerinde morfolojik olarak kontrol
hücrelerine nazaran mekik Ģekilli görüntünün kısaldığı ve normalde olması gereken
baĢak tarlası görünümünün yerine hücrelerde kısalmaya bağlı olarak flask yüzeyini
kaplama oranında farklılık olduğu gözlemlendi.
Aynı hücre hattının endotoksinlere verdiği fizyolojik cevap incelendiğinde,
Hücre canlılığınına ait OD değerlerinin endotoksin yoğunluğuna bağlı olmaksızın
test gözleri arasında değiĢkenlik gösterdiği saptanmıĢtır. Dolayısıyla hücre
canlılığının endotoksin yoğunluğundan etkilenmediği saptandı (ġekil 2C, 3C).
Yine BHK-21 hücre hattının trypan blue boyama yöntemi ile canlı/ölü hücre
sayısına bakıldığında da dilüsyon flaskları ve kontrol flaskı dahil olmak üzere canlı
ve ölü hücre sayısı endotoksin miktarına bağlı olmaksızın birbirinden farklı olduğu
belirlendi. Bu bulgu da, endotoksinlerin BHK-21 hücre hattı üzerinde hücre ölümü
veya canlılığına etki etmediğini düĢündürmüĢtür. Masuzawa ve ark. (1990),
in vitro
olarak 500 µg/ ml dozunda PAgslar‟ın (koruyucu antijenler), fare makrofajlarının
peritonal eksudatları üzerine zayıf bir sitotoksik etki gösterdiği, ancak BHK-21
47
hücreleri üzerine herhangi bir toksik etki göstermediği tespit etmiĢtir. Bu çalıĢmada
BHK-21 hücrelerine ait elde edilen veriler çalıĢmamızda elde ettiğimiz bulguları
destekler niteliktedir.
TartıĢılan tüm bu veriler, sonuç olarak Vero, MDBK ve BHK-21 hücre
hatlarının E. coli ve P. aeruginosa endotoksinine karĢı değiĢken cevaplar verdiğini
göstermiĢtir. Vero hücre hattı, her iki endotoksine karĢı gerek morfolojik ve gerekse
fizyolojik olarak en duyarlı hücre hattı olarak bulunmuĢ iken, bu endotoksinlerin
MDBK hücre hattında morfolojik bir değiĢikliğe yol açmamakla birlikte,
P. aeruginosa endotoksininin hücre yoğunluğunda azalmaya sebep olduğunu,
E. coli'nin ise hücre yoğunluğunu etkilemediğini göstermiĢtir. BHK-21 hücre
hattında ise morfolojik değiĢiklikler gözlemlenmesine karĢın, yapılan diğer testlerin
sonucunda her iki endotoksine karĢı anlamlı sonuçlar elde edilememesi, bu hücre
hattının E. coli ve P. aeruginosa endotoksinine daha dirençli olduğunu
düĢündürmüĢtür.
Morrisson ve ark. (1994) ve Ryan (2004) endotoksinlerin tüm hücre hatlarını
aynı Ģekilde etkilemediğini, bazı hücre hatlarını daha çok etkilerken bazılarını daha
az etkilediğini bilmiĢlerdir. Bunun sebebi olarak da bazı hücre hatlarının endotoksin
reseptörlerinden yoksun olabileceğini ve bunun sonucunda da endotoksinlerden daha
az etkilenebileceğini öne sürmüĢlerdir. Diğer bir sebep olarak da uzun yıllar boyunca
seri pasajları yapılan hücre hatlarının bu uzun süreç içerisinde endotoksinlere karĢı
doğal direnç kazanmıĢ olabileceklerini öne sürmüĢlerdir.
Adı geçen endotoksinlere ait BHK-21, MDBK, Vero hücre hatlarında yapılan
tüm testlerin sonucunda, tüm parametreler Ģu veya bu Ģekilde değiĢmiĢ iken,
değiĢmeyen tek parametre kullanılan tüm hücre hatlarında meydana gelen ölü hücre
sayısının değiĢmemesi dikkat çekici bir bulgu olarak karĢımıza çıkmıĢtır. Bu dikkat
çekici bulgu, endotoksinlerin hücre hatlarında özellikle mitoz bölünme sürecine
etki ettiğini düĢündürmektedir.
48
Gelecekte bu verilerin, endotoksinlerin değiĢik hücre hatlarında hücre
mitozuna etkisinin araĢtırılacağı ve bunlara iliĢkin süreçlerin inceleneceği daha
detaylı çalıĢmalara ıĢık tutacağı düĢünülmektedir.
49
5. SONUÇ
AraĢtırmada, bakteri endotoksinlerinin aĢı üretiminde kullanılan Vero, MDBK,
BHK-21 gibi hücre hatlarına etkisinin deneysel olarak araĢtırılması amaçlanmıĢtır.
Bu amaçla, çalıĢma süresince hücre hatlarında meydana gelen sayısal ve morfolojik
değiĢikliklerin belirlenmesi ve birbiriyle kıyaslanması gerçekleĢtirilmiĢtir. Yapılan
çalıĢma sonucunda elde edilen veriler değerlendirildiğinde Ģu sonuçlara varılmıĢtır.
1)
Vero, MDBK ve BHK-21 hücre hatlarında üzerine endotoksinlerin
değiĢken etki gösterdiği ve aynı zamanda farklı endotoksinlerin farklı hücre hatları
üzerine etkisinin de değiĢiklik gösterdiği saptanmıĢtır.
2)
Hücre morfolojisi ve in vitro ortamda hücre sayısal değerleri baz
alındığında: Vero, MDBK, BHK-21 hücre hatları içerisinde gerek P. aeruginosa
gerek E. coli endotoksininin değiĢik yoğunluklarından en çok etkilenen hücre
hattının Vero hücre hattı olduğu tespit edilmiĢtir.
3)
BHK-21 hücre hattında ise hücre canlılığı ve canlı/ölü sayısının
endotoksin yoğunluğuna bağlı olmaksızın değiĢenlik gösterdiği saptanmıĢtır.
4)
MDBK hücre hattının ise, her iki bakteri endotoksinin değiĢik
yoğunluklarına karĢı cevabı değiĢken olmuĢtur. Buna göre P. aeruginosa
endotoksinine maruz kalmıĢ hücrelerin yoğunluğu ile endotoksin konsantrasyonu
arasında ters orantı olduğu sonucuna varılmıĢtır. Aynı hücre hattı E. coli
endotoksinin farklı yoğunluklarına yine değiĢken yanıt vermiĢtir.
Yukarıda anlatılan sonuçlar tek tek değerlendiğinde; adı geçen üç hücre hattı
içerisinde endotoksine en fazla duyarlı hücre hattının Vero olduğu anlaĢılmıĢtır. Bu
da endotoksinlerin hücrelere etkisinin araĢtırıldığı çalıĢmaların büyük bir kısmının
neden Vero hücreleriyle yapıldığını açıklamaktadır. Bunun yanı sıra diğer hücre
hatları belirli endotoksin yoğunluklarına maruz kaldıklarında, verilen cevabın
50
yoğunluk oranı ile iliĢkili olmaksızın değiĢken olması, bu hücre hatlarının
endotoksinlere daha dirençli olduğunu düĢündürmektedir.
Ancak, Vero hattının her iki endotoksinin farklı yoğunluklarına verdiği cevap
incelendiğinde; özellikle hücrenin ölüm oranında bir değiĢiklik meydana
gelmemesine karĢın sayısal bir azalma meydana gelmesi, endotoksinlerin Vero
hücrelerinin özellikle mitoz bölünme sürecine etki ettiğini düĢündürmektedir.
Gelecekte bu verilerin, endotoksinlerin hücre mitozuna etkisinin araĢtırılacağı
ve bunlara iliĢkin süreçlerin inceleneceği daha detaylı çalıĢmalara ıĢık tutacağı
düĢünülmektedir.
51
ÖZET
Bakteri Endotoksinlerinin Aşı Üretiminde Kullanılan Devamlı Hücre Hatlarına
Etkisinin Araştırılması
Bu çalıĢmada, bakteri endotoksinlerinin aĢı üretiminde kullanılan devamlı
hücre hatlarına etkisi deneysel olarak araĢtırılmıĢtır. Bu amaçla, çalıĢma süresince
hücre hatlarında meydana gelen sayısal ve morfolojik değiĢiklikler belirlenmiĢ ve
hücre hatları arasındaki farklar kıyaslanmıĢtır.
Devamlı hücre hatları olarak Vero, MDBK ve BHK-21 hücre hatları tercih
edilmiĢtir. Aynı zamanda endotoksin elde edilecek bakteriler olarak, doğada yaygın
bulunması sebebiyle P. aeruginosa ve E. coli tercih edilmiĢtir.
AraĢtırmada kullanılan P. aeruginosa ve E. coli'ye ait endotoksinlerin varlıkları
tüm stok solüsynlarında ve dilüsyon oranlarında jel klot LAL testi ile teyid edilmiĢtir.
Endotoksinlerin bu hücre hatları üzerine morfolojik etkisini incelemek
amacıyla Vero, MDBK ve BHK-21 hücreleri doku mikroskobunda hergün incelendi.
Vero hücresinde vakuol ve granülasyon oluĢumları tespit edildi.
Endotoksine maruz kalan hücrelerin hücre canlılığını tespit etmek amacıyla
yapılan ELISA testi sonucunda Vero, MDBK ve BHK-21 hücrelerinin değiĢen
miktarlarda endotoksinden etkilendiği tespit edilmiĢtir. En fazla etkilenen hücre
hattının da Vero hücre hattı olduğu tespit edilmiĢtir.
Endotoksinlerin hücre hatlarında hücre sayısına etkisinin belirlenmesi için
yapılan trypan blue boyama yönteminde ise hücre hatlarında farklı veriler elde
edilmiĢtir. En belirgin olarak Vero hücre hattında canlı hücre sayısı endotoksin
52
miktarı ile ters orantılı olarak azalıĢ göstermiĢtir. Diğer hücre hatlarında ise canlı
hücre oranı değiĢkenlik göstermiĢtir.
Elde edilen verilere göre bu üç hücre hattı içerisinde endotoksine en fazla
duyarlı hücre hattının Vero hücre hattı olduğu ortaya çıkarılmıĢtır. Bunun yanı sıra
diğer hücre hatları belirli endotoksin yoğunluklarına maruz kaldıklarında verilen
cevabın yoğunluk oranı ile iliĢkili olmaksızın değiĢken olması endotoksinlere karĢı
daha dirençli olduğunu düĢündürmektedir. Ayrıca hücre hatlarında endotoksinlerin
hücre ölüm oranına etki etmediği sonucuna varılmıĢtır.
Anahtar Kelimeler: BHK-21, Endotoksin, Escherichia coli, Jel klot LAL
testi, MDBK, Pseudomonas aeruginosa, Vero.
53
SUMMARY
The aim of this study was to determine the effects of bacterial endotoxins on various
cell lines used in vaccine production and other biyological products. For this purpose
quantitative and morphlogical changes at various cell lines had been determined and
compared.
Vero, MDBK and BHK-21 cell lines was prefered as continous cell lines. On
the other hand, P. aeruginosa and E. coli was prefered as bacteria to derive
endotoxins since they have been found abundantly in nature.
Existance of P. aeruginosa and E. coli endotoxins used in this research were
confirmed by gel clot LAL test in all stock solutions and dilutions.
Vero, MDBK and BHK-21 cell cultures were daily examined microscopically
in order to detect the morphological effects of endotoxins on cell cultures.
Granulation and vacuolisation has been detected on Vero cell line.
The results of the ELISA technique which was used for detection of cell
viabiliy on cell lines objected to bacterial endotoxines revealed that, all the cell lines
were effected from endotoxines at varying levels. The most effected cell line was
found to be the Vero among others.
In order to determine the effect of endotoxins on over all cell number in culture
enviroment, trypan blue staining method was performed. Although data achieved
from these studies exhibit inconsistancy, live cell numbers in Vero cell line had
declined as endotoxin concentration increased. On the contrary, in other cell lines,
live cell ratio exhibit inconsistancy.
54
According to these data achieved, it is concluded that the most susceptible cell
line against endotoxins among tested was Vero. On the other hand, it seems that
other cell lines were more resistant to endotoxins since they exhibit various response
to endotoxins regardless the concentration of endotoxin. Furthermore it is concluded
that endotoxins do not effect the overall cell death ratio in these cell lines.
Key Words: BHK-21, Endotoksin, Escherichia coli, Gel clot LAL test,
MDBK, Pseudomonas aeruginosa, Vero.
55
KAYNAKLAR
AKALIN, H. (2004). Pseudomonas infeksiyonları. 6. Antimikrobik Kemoterapi
Günleri, Program ve Özet kitabı, Ġstanbul., 124-130.
ALTMAN, S.A., RANDERS, L., RAO, G. (1993). Comparison of trypan blue dye
exclusion and fluorometric assays for mammalian cell viability determinations.
Biotechnol. Prog, 9:671-74.
ANSPACH, F.B. (2001). Endotoxin removal by affinity sorbents. J. Biochem. and
Biophy. Met., 49:665-681.
ARDA, M. (2011). Temel Mikrobiyoloji Kitabı. 4.Baskı Medisan Yayınları71/Ankara. 218-220.
ASAKAWA, S., FUJIWARA, H., NAITO, S., HOMMA, R., ISHIDA, S., CHINO,
F., TSUCHIYA, M., MATSUURA, S., TANAKA, S., OHKI, M. (1994).
Application of the Limulus test for practical quality control on endotoxin
content in commercial human serum albumin (HSA) products. In comparison
with the rabbit pyrogen test.Yakugaku Zasshi., 114(11):888-93.
BATES, D.W, PARSONNET, J., KETCHUM, P.A., MILLER, E.B., NOVITSKY,
T.J., SANDS, K., HIBBERD, P.L., GRAMAN, P.S., LANKEN, P.N.,
SCHWARTZ, J.S., KAHN, K., SNYDMAN, D.R., MOORE, R., BLACK, E.
VE PLATT, R. for the AMCC Sepsis Project Working Group (1998). Limulus
amebocyte lysate assay for detection of endotoxin in patients with sepsis
syndrome. Clin Infect Dis. 27(3): 582-591.
BEKAR, M. (1997). Enterobacteriaceae familyası mikroorganizmaları genel
karakterleri ve tanı yöntemleri. Vet. Kont. ve ArĢ. Enst. Müd. Etlik-Ankara
Yayın No. 97-1, P:17,53.
BERKER, K.A. ve HOLD, S.A. (1983). The invitro effect of actinobacillus
actinomycetemcomitans strain Y4 lypopolisaccaride on murine peritoneal
macraphages. Can. J. Microbiol., 29:1552-1563.
BERJIS, M. ve GREEN, M.H. (1986). Selective cytotoxicity of L-canavanine in
tumorigenic Madin-Darby canine kidney T1 cells. Chem. Biol. Interact.
60(3): 305-15.
56
BERTHOLD, W., WALTER, J. (1994). Protein purification: aspects of processes for
pharmaceutical products. Biologicals 22:135-150.
BILGEHAN, H. (2000). Fermentasyon yapmayan gram olumsuz bakteriler
"Bilgehan, H., (ed): Klinik Mikrobiyoloji Özel Bakteriyoloji ve Bakteri
Ġnfeksiyonları" kitabı, Fakülteler Kitapevi, Ġzmir, 422.
BROWN, S.A. (1982). Cell culture the methods: A symposium. American Society
for Testing and Metarials. Library of Congress Catalog Card Number : 8370421.
BRUNN, G.J., PLATT, J.L. (2006). The etiology of sepsis: turned inside out. Trends
in Mol. Med. 12:10-16.
BUI, A. (2012). Structual characteristics of bacterial endotoxins. Doktora tezi.
University of PECS. Doctoral School of Chemistry PECS / Denmark.
CASE-GOULD, M.J. (1984). Endotoxin in Vertebrate Cell Culture: Its Measurement
and Significance in Uses and Standardization of Vertebrate Cell Lines, (Tissue
Culture Association, Gaithersburg, MD,) 125-136.
CARBONELL G.V. ALFIERI A.F., ALFIERI A.A., VIDOTTO M.C., LEVY C.E.,
DARINI A.L., YANAGUITA R.M. (1997). Detection of cytotoxic activity on
Vero cells in clinical isolates of Serratia marcescens. Brazilian J. Med. Biol.
Res., 30:1291-1298.
CO, T.U.I., HOPE, D., SCRĠFT, M.H. VE POWERS, J., (1944). Purified pyrogen
from Eber thella typhosa. A preliminary report on its preparation and its
chemical and biologic characterization. J. Lab. Clin. Med., 29:58-62.
DARKOW, R., GROTH, T., ALBRECHT, W., LÜTZOW, K., PAUL, D. (1999).
Functionalized nanoparticles for endotoxin binding in aqueous solutions.
Biomaterials. 20(14):1277-83.
DAVID, A.G, MARK, R.G. (2002). Clinical implications of endotoxin
concentrations in vaccines. Ann Pharmacother; 36:776-780.
DAWSON, M.E. (1998). The significance of endotoxin to cell culture and
biotechnology. Associates of cape cod incorporated. Vol. 16, No.1.
DREXLOR, I., HELLER, K., WAHREN, B., ERFLE, V., SUTTER, G. (1998).
Higly attenuated modified vaccinia virus Ankara replicates in Baby Hamster
57
Kidney cells, a potential host for virus propagation, but not in various human
transformed and primary cells. J. Gen. Virol. 79:347-352.
ERDEM, B. (1999). Pseudomonaslar, " Ustaçelebi ġ. (ed): Temel ve Klinik
Mikrobiyoloji" kitabı, GündeĢ Kitapevi, Ankara, 551-557.
ESENDAL Ö.M. (2006). Pseudomonas Enfeksiyonları. "Aydın N. ve Paracıklıoğlu
J., (eds): Veteriner mikrobiyoloji (Bakteriyel Hastalıklar)" kitabı, Ġlke emek
yayınları. 129-133.
FISKE,
J.M.,
ROSS,
A.,
VANDERMEID,
R.K.,
MCMICHAEL,
J.C.,
ARUMUGHAM, (2001). Method for reducing endotoxin in Moraxella
catarrhalis Usp A2 protein preparations. J. Chrom. B., 753:269-278.
FORBES, I.J., (1965). Induction of mitosis in macrophages by endotoxin.
J. Immunol., 94:37-9.
FOREHAND, J.R., PABST, M.J., PHILLIPS, W.A., JOHNSTON, J.R.B., (1989).
Lipopolysaccharide priming of human neutrophils for an enhanced respiratory
burst. Role of intracellular free calcium. J. Clin. Invest., 83:74-83.
FORRESTER, A., FARRELL, H., WILKINSON, G., KAYE, J., DAVISPOYNTER, N., MINSON, T. (1992). "Construction and properties of a mutant
of herpes simplex virus type 1 with glycoprotein H coding sequences deleted".
J. Virol., 66(1):341–8.
FRESHNEY, R.I. (2005). Culture of Animal Cells: a Manual of Basic Technique,
5th edition, Wiley-Liss.
FREUDENBERG, M.A., MEIER-DIETER, U., STAEHELIN, T., GALANOS, C.
(1991). Analysis of LPS released from Salmonella abortus equi in human.
Microb. Pathogen., 10:93-104.
FUJIOKA, H., AKEMA, T. (2010). Lipopolysaccharide acutely inhibits proliferation
of neural precursor cells in the dentate gyrus in adult rats. Brain Res. 1352:3542.
GALANOS, C., FREUDENBERG, M.A., (1993). Mechanisms of endotoxin shock
and endotoxin hypersensitivity. Review. Immunobiol., 187(3-5):346-56.
GEIER, D. ve GEIER, M. (2002). Clinical implications of endotoxin concentrations
in vaccines. Ann Pharmacother; 36:776-780.
58
GEIER, M.R., STANBRO, H., MERRIL, C.R. (1978). Endotoxins in commercial
vaccines. App. Env. Microbiol., 36(3):445-449.
GOLENBOCK, D.T., HAMPTON, R.Y., QURESHI, N., TAKAYAMA, K.,
RAETZ, C.R.H. (1991). Lipid A-like molecules that antagonize the effects of
endotoxins on human monocytes. J. Biol. Chem., 266:19490-19498.
GORBET, M.B., SEFTON, M.V. (2006). Endotoxin: The uninvited guest.
Biomaterials, 26:6811-6817.
GOVORKOVA, E.A., KAVERIN, N.V., GUBOREVA, L.V., MEIGNIER, B.,
WEBSTER, R.G. (1995). Replication of Influenza A viruses in a Green
Monkey Kidney continious cell line (Vero). J. Infect. Dis., 172(1):250-253.
HARLAN, J.M., HARKER, L.A., STRIKER, G.E., WEAVER, L.J. (1983). Effects
of lipopolysaccharide on human endothelial cells in culture. Thromb Res.,
29(1):15-26.
HAY, R.J. (1991). Cell line preservation and characterisation. In Masters, J.R.W.
(Ed.). Animal Culture, A practical approach. Oxford, U.K, IRL Press at Oxford
University Press., 95-148.
HECKER, W., WITTHAUER, D., STAERK, A. (1994). Validation of dry heat
inactivation of bacterial endotoxins. PDA J. Pharm. Sci. Technol., 48(4):197204.
HEILMAN, D.H. (1965). In vitro studies on changes in the reticuloendothelial
system of rabbits after an injection of endotoxin. J. Reticuloendothel. Soc.,
2(2):89-104.
HEILMAN, D.H. (1968). In vitro toxicity of endotoxin for macrophages of young
guinea pigs and rabbits. Int. Arch. Allergy Appl. Immunol., 33(5):501-10.
HEUMANN, D., ROGER, T. (2002). Initial responses to endotoxinas and Gramnegative bacteria. Clin. Chim. Acta, 323:59-72.
HIRAYAMA, C., SAKATA, M. (2002). Chromatographic removal of endotoxin
from protein solutions by polymer particles. J. Chrom. B., 781:419-432.
HOADLEY, A.W. ve MCCOY, E. (1968). Some observations on the ecology of
Pseudomonas aeruginosa and its occurrence in the intestinal tract of animals.
Cornell Vet., 58:354.
59
HOFFMANN, S., PETERBAUERE, A., SCHINDLERA, S., FENNRICHA, S.,
POOLEB, S., MISTRYB, Y., MONTAG-LESSINGC, T., SPREITZERC, I.,
LOSCHNERC, B., AALDEREND, M.V., BOSD, R., GOMMERD, M.,
NIBBELINGD, R., WERNER-FELMAYERE, G., LOITZLE, P., JUNGIF, T.,
BRCICF, M., BRUGGERG, P., FREYG, E., BOWEH, G., CASADOH, J.,
COECKEH, S., LANGEH, J., MOGSTERI, B., NÆSSI, L.M., AABERGEI,
I.S., WENDELA, A., HARTUNGA, T. (2005). International validation of
novel pyrogen tests based on human monocytoid cells. J. Immunol. Methods.
298(1-2):161-73.
HOU, K.C. ve ZANIEWSKI, R. (1990). Depyrigenation by endotoxin removal with
positively charged depth filter cartridge. J. Parent. Sci. Tech., 44:204-209.
HUSSAINI, S.N. ve READY, R.A. (1981). Studies on Escherichia coli vaccines:
estimation of endotoxins in veterinary vaccines. Vet. Res. Commun., 5(2):1715.
IZGUR M. (2006). Enterobakteri infeksiyonları. " Aydın N. ve Paracıklıoğlu J.,
(eds): Veteriner mikrobiyoloji (Bakteriyel Hastalıklar)" kitabı, Ġlke emek
yayınları. 110,112.
JAFFE, E.A., NACHMAN, R.L., BECKER, G.C., NININCK, C.R. (1973). Culture
of human endothelial cells derived from umblical veins. J. Clin. Invest.,
53:2745-2756.
JOHN D.L. ve KENNETH E.A. (1988). Validation of a heating cell for precisely
controlled studies on the thermal destruction of endotoxin in glass. J. Parenteral
Sci. Technol., 42:9-14.
JOHNE, B., GAUDERNACK, G. ve MORLAND, B. (1987). Effect of endotoxins
from Bacteriodes intermedius and Escherichia coli on human monocytes
invitro. Acta Pathol. Microbiol. Immunol. Scand., 95(Sec C):241-250.
JOINER, T.J., KRAUS, P.F., PHD KUPIEC, T.C. (2002). Comparison of endotoxin
testing methods for pharmaceutical products. Int. J. Pharm. Compound.,
6(6):408-409.
KESSEL, R.W., BRAUN, W., PLESCIA, O.J. (1966). Endotoxin cytotoxicity: role
of cell-associated antibody. Proc. Soc. Exp. Biol. Med., 121(2):449-52.
60
KIRIKAE, T., KIRIKAE, F., SAITO, S., TOMINAGA, K., TAMURA, H.,
UEMURA,
Y.,
YOKOCHI,
T.,
NAKANO,
M.
(1998).
Biological
characterization of endotoxins released from antibiotic-treated Pseudomonas
aeruginosa and Escherichia coli. Antimicrob. Agents Chemother., 42(5):101521.
KONEMAN, E., STEPHAN, D.A., WILLIAM, M.J., SCHRECKENBERGER, P.C.,
WINN, C.W. J.R. (2006). The nonfermentative Gram-negative bacilli.
Konoman‟s Colour Atlas and Textbook of Diagnostic Microbiology 6th
Edition. Philadelphia, Lippincott: 303-391.
KONOWALCHUK J., SPEIRS J. I. VE STAVRIC S. (1977). Vero Response to a
Cytotoxın of Escherichia coli. Infect. and Ġmmun., 18:775-779.
LIN, M.F., WILLIAMS, C., MURRAY, M.V., ROPP, P.A. (2005). Removal of
lipopolysaccharides
from
protein-lipopolysaccharide
complex
by
nonflammable solvents. J. Chrom. B., 816:167-174.
LINDL, T., STEUBING, R. (2013). Animal cell lines. 328-472. "Atlas of Living cell
cultures" kitabı. John Wiley & Sons. West Sussex England. ISBN:
3527769930.
LOPPNOW,
H.,
BRADE,
H.,
DUÈRRBAUM,
I.,
DINARELLO,
C.A.,
KUSUMOTO, S. RIETSCHEL, E.Th. (1989). IL-1 induction-capacity of
defined lipopolysaccharide partial structures. J. Immunol., 142:3229-3238.
MAGALHÃES, P.O., LOPES, A.M., MAZZOLA, P.G., RANGEL-YAGUI, C.,
PENNA, T.C., PESSOA, A.JR. (2007). Methods of endotoxin removal from
biological preparations: a Review. J. Pharm. Pharmaceut. Sci. (www.
cspsCanada.org), 10(3):388-404.
MALIK, P., SHARMA, V.D., CHANDRA, R. (1995). Cytotoxigenicity in
Salmonella serovars. Indian J. Exp. Biol., 33(3):177-81.
MASUZAWA, T., NAKAMURA, R., SHIMIZU, T., YANAGIHARA, Y. (1990).
Biological activities and endotoxic activities of protective antigens (PAgs) of
Leptospira interrogans. Zentralbl. Bakteriol., 274(1):109-17.
MONTAGNON, B.J. (1989). Polio rabies vaccines produced in continious cell lines:
a reality for Vero cell line. dev. Biol. Stand., 70:27-47.
61
MORRISON, D.C., DINARELLO, C.A., MUNFORD, R.S., NATANSON, C.,
DANNER, R., POLLACK, M., SPITZER, J.J., ULEVITCH, R.J., VOGEL,
S.N. ve MCSWEEGAN, E. (1994). Current status of bacterial endotoxins.
ASM News, 60:479-484.
MUSHIN, R. ve ZIV, G. (1973). An epidemiological study of Pseudomonas
aeruginosa in cattle and other animals by pyocine typing. J. Hyg. (Lond).
71(1):113-22.
OGIKUBO, Y., OGIKUBO, Y., NORIMATSU, M., NODA, K., TAKAHASHI, J.,
INOTSUME, M., TSUCHIYA, M., TAMURA, Y. (2004). Evaluation of the
bacterial endotoxin test for quantification of endotoxin contamination of
porcine vaccines. Biologicals. 32:88-93.
PARK, C.Y., JUNG, S.H., BAK, J.P., LEE, S.S., RHEE, D.K. (2005). Comparison
of the rabbit pyrogen test and Limulus amoebocyte lysate (LAL) assay for
endotoxin in hepatitis B vaccines and the effect of aluminum hydroxide.
Biologicals. 33(3):145-51.
PENG, S., HUMMERJOHANN, J., STEPHAN, R., HAMMER, P. (2013). Short
communication: Heat resistance of Escherichia coli strains in raw milk at
different subpasteurization conditions. J. Dairy. Sci., 96(6):3543-6.
PETSCH, D., ANSPACH, F.B. (2000). Endotoxin removal from protein solutions. J.
Biotech., 76:97-119.
POLLANEN, M.T., SALONEN, J.I., GRAINER,D., VITTO, V.J. (2000). Epithelial
cell
responce
to
challange
of
bacterial
lipoteichoic
acids
and
lipopolysaccharides in vitro. J. Med. Microbiol., 49:245-252.
PROBEY, T.F. ve PITTMAN, M. (1945). The pyrogenicity of bacterial
contaminants found in biologic products. J. Bacteriol., 50:397-411.
PUGIN, J., ULEVITCH, R.J., TOBIAS, P.S. (1995). Mechanism of cellular
activation by endotoxin. Prog. Surg. 20, 8-17
RAETZ, C.R., ULEVITCH, R.J., WRIGHT, S.D., SIBLEY, C.H., DING, A.,
NATHAN, C.F. (1991). Gram-negative endotoxin: an extraordinary lipid with
profound effects on eukaryotic signal transduction. The FASEB J., 5(12):26522660.
62
REITMEYER, J.C. ve PETERSON, J.W. (1988). Invitro cytotoxicity of
lipopolysaccharides for chineese hamster ovary cells. FEMS Microbiol. Lett.,
49:393-396.
RIETSCHEL, E.T., KIRIKAE, T., SCHADE, F.U., MAMAT, U., SCHMIDT, G.,
LOPPNOW, H., ULMER, A.J., ZÄHRINGER, U., SEYDEL, U., DI
PADOVA, F., SCHREIER, M., BRADE, H. (1994). Bacterial endotoxin:
molecular relationships of structure to activity and function. Review. FASEB
J., 8(2):217-25.
RYAN, J.A. (2002). Understanding and Managing Cell Culture contamination.
Corning, Inc. Technical Publication, CLS-AN-020. (Corning Life Sciences
web site at www.corning.com/lifesciences.)
RYAN, J.A. (2004). Endotoxins and cell culture. Corning, Inc. Technical Bulletin. 18. (Corning Life Sciences web site at www.corning.com/lifesciences.)
SARGENT, W. (2002). Crab wars: a tale of horseshoe crabs, bioterrorism, and
human health. Unıversity Press of New England. P:108-114.
SCHROMM A.B., BRANDENBURG K., LOPPNOW H., MORAN A.P., KOCH
M.H.J., RIETSCHEL E.T., SEYDEL U. (2000). Biological activities of
lipopolysaccharides are determined by the shape of their lipid A portion.
European J. Biochem., 267:2008-2013.
SEARS, C.L. ve KAPER, J.B. (1996). Enteric bacterial toxins: mechanisms of action
and linkage to intestinal secretion. Microbiol. Rev., 60:167-215.
SCHINDLER, S., VON AULOCK, S., DANESHIAN, M., HARTUNG, T. (2009).
Development, validation and applications of the monocyte activation test for
pyrogens based on human whole blood. ALTEX., 26(4):265-77.
SCHUHMANN, R.R., LEONG, S.R., FLAGGS, G.W., GRAY, P.W., WRIGHT,
S.D., MATHISON, J.C. (1990). Structure and function of lipopolysaccharidebinding protein. Science; 249:1429-1431.
STANISLAVSKY,
E.S.,MAKARENKO,
T.A.,
KHOLODKOVA,
E.V.,
LUGOLSKI, C. (1997). R-form lipopolysaccharides (LPS) of Gram-negative
bacteria as possiblevaccineantigens. FEMS Immun. Med. Microbiol.,
18:139:145.
63
TAKIGUCHI, S. ve KOGA, A. (1988). Effect of bile acids and endotoxin on the
function and morphology of cultured hamster Kupffer cells. Virchows Arch. B.
Cell Pathol., 54:303-311.
TRIVEDI, B., VALERIO, C., SLATER, J.E., (2003). Endotoxin content of
standardized allergen vaccines. J, Allergy Clin, Immunol., 111(4):777-83.
TSUJI, K. ve HARRISON, S.J. (1978). Dry-heat destruction of lipopolysaccharide:
dry-heat destruction kinetics. Appl. Environ. Microbiol., 36(5):710-4.
VAARA, M., NURMINEN, M. (1999). Outer membrane permeability barrier in
Escherichia coli mutants that are defective in the late acyltransferases of lipid
A biosynthesis. Antimicrob. Agents and Chemother., 43:1459-1462.
VAHAPOĞLU, H., AKHAN, S.Ç. (2002). Pseudomonas aeruginosa ve diğer
Pseudomonas türleri. " Topçu AW., Söyletir G., Doğanay M. (eds): Ġnfeksiyon
Hastalıkları ve Mikrobiyolojisi " kitabı, Nobel Tıp Kitapevleri, Ġstanbul.
VOGEL, S.N., ve HOGAN, M.M. (1990). The role of cytokines in endotoxinmediated host responses. " Oppenheim, J.J., and Shevack, E.M., (eds): In
Immunopharmacology-the Role of Cells and Cytokines in Immunity and
Inflammation. " 238-258, Oxford University Press, New York.
WESTPHAL, O. (1975). Bacterial endotoxins. Int. Arch. Allergy Appl. Immunol.,
49:1-43.
WESTPHAL, O., ve JANN, K. (1965). Bacterial lipopolysaccharide. Extraction with
phenol-water and further applications of the procedure. Methods Carbohydr.
Chem., 5:83-91.
64
ÖZGEÇMİŞ
I-
Bireysel Bilgiler
Adı
: Züleyha
Soyadı
: Ergün
Doğum yeri ve tarihi
: Ankara, 28.06.1986
Uyruğu
: TC
Medeni durumu
: Bekar
ĠletiĢim adresi ve telefonu
: Keklikpınarı mah. 900. cad. 897.sok.
No:13/11 Dikmen / Ankara
(0312) 426 79 29
ll-
Eğitimi
2011-2013 AÜ. Veteriner Fakültesi, Mikrobiyoloji A.B.D. Yüksek Lisans
2007-2010 Kırıkkale Üniversitesi Biyoloji Bölümü
2004-2006 Hacettepe Üniversitesi Laboratuvar Teknikerliği Bölümü
2000-2004 Ankara Mustafa Kemal Sağlık Meslek Lisesi
1992-2000 Nedred Arif Ġlköğretim Okulu
Yabancı Dili Ġngilizce
lll-
Ünvanları
Biyolog
lV-
Mesleki Deneyimi
2006 yılından itibaren Veteriner Kontrol Merkez AraĢtırma Enstitüsü'nde
Biyolog
65
2011 yılından itibaren A.Ü. Veteriner Fakültesi, Mikrobiyoloji A.B.D. Yüksek
Lisans öğrencisi
V-
Bilimsel Etkinlikleri
Seminerler
1.Taylorella equigenitalis'in Laboratuvar Tanısı (2012).
Sempozyum
1. Bati Nil Virüsü Sempozyumu
Yer Aldığı Projeler
Veteriner Kontrol Merkez AraĢtırma Enstitüsü Viral AĢı Üretim Laboratuvarı
tarafından yürütülen "Attenüe BT-9 ve BT16 SuĢlarının Orjini Olan Saha SuĢları Ġle VP2
Gen Segmenti Düzeyinde KarĢılaĢtırılması" isimli proje (Yardımcı araĢtırıcı), (Proje Ocak
2014 itibari ile baĢlayacak).
Veteriner Kontrol Merkez AraĢtırma Enstitüsü Viral AĢı Üretim Laboratuvarı
tarafından yürütülen TAGEM/HSGYAD/13/A07/P02/25 no'lu " Isıya Dirençli Küçük
Ruminant Vebası AĢısı (PPR) Üretimi " isimli proje (Yardımcı araĢtırıcı), 2012.