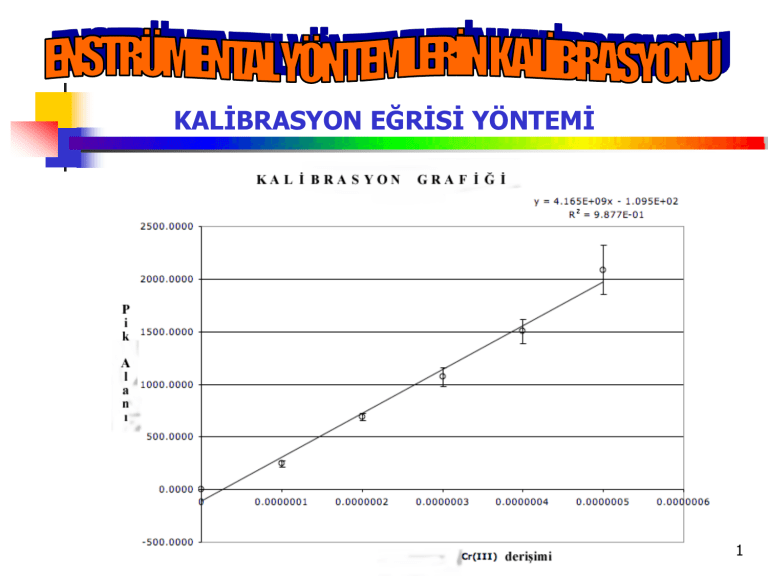
KALİBRASYON EĞRİSİ YÖNTEMİ
1
STANDART EKLEME YÖNTEMİ
Örnek matriks kompozisyonunun değişken olduğu veya bilinmediği
durumlarda kalibrasyon grafiği hazırlamak için kullanılan bir tekniktir.
Çözücü numune matriksinin blank değerinin güvenilir bir şekilde
ayrılamadığı durumlarda daha çok kullanılır.
2
İÇ STANDART YÖNTEMİ
Standart ekleme yöntemine göre hazırlanan çözeltiler
kalibrasyon eğrisinde analit derişimine karşı analit
sinyali/iç standart sinyali oranına karşı grafiğe
geçirilir.
Numune hazırlama aşamasında analit kaybından
kaynaklanabilecek hatayı düzeltmek için kullanılır.
Örnek: Kan serumunda Na, K tayininde Li sıklıkla
kullanılan bir iç standarttır.
3
SİNYAL VE GÜRÜLTÜ
Sinyal Nedir?
Gürültü Nedir?
Deneysel Çalışma ve Sinyal/Gürültü Oranı?
Gürültü Kaynakları ve Giderme Yolları?
4
Sinyal: Cihaz ile numune arasında bilgi alışverişi sağlayan
bir araç.
Gürültü: Analitik cihazlardan elde edilen sinyal, kontrolü
mümkün olmayan pek çok değişkenin etkisiyle rasgele
şekilde dalgalanır. Cihazın duyarlığını azaltan bu
dalgalanmalara gürültü denir.
5
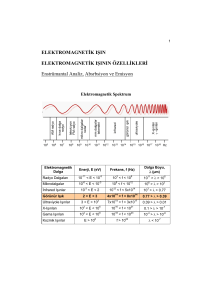
SPEKTROMETRİK YÖNTEMLERE GİRİŞ
ELEKTROMANYETİK IŞIN
Elektromanyetik ışın, boşlukta çok büyük hızla
hareket edebilen bir enerji türüdür.
Elektromanyetik dalgalar, elektrik yüklü
parçacıkların hareketiyle oluşur. Bu
dalgalara elektromanyetik ışın da denir.
6
Elektromanyetik ışının en çok karşılaşılan türleri, gözle algıladığımız
görünür ışık ve ısı şeklinde algıladığımız infrared (kızılötesi)
ışınlarıdır.
7
Elektromanyetik ışın, hem dalga hem parçacık
özelliğine sahiptir.
Girişim ve Kırınım davranışları dalga özelliğiyle
açıklanır.
Aynı dalga boylarındaki ışınlar aralarındaki faz
farkına göre birbirlerini kuvvetlendirir veya
söndürürler.
Farklı dalga boylarındaki ışınlar girişim
yapmazlar. Bu olay ışığın parçacık özelliği ile
açıklanabilir.
8
•Bir metal yüzeyinden ışın ile elektronların koparılması (fotoelektrik
olay), ışın enerjisinin bir madde tarafından absorpsiyonu
(soğurulması) ve emisyonu (yayınımı) olayları, ışının parçacık
özelliği (foton) ile açıklanır. (örnek;dedektörler)
9
Fotoelektrik Etki
Işığın parçacık özelliği bu olayla açıklanmaya çalışılmıştır. Buna
göre;
Bir metal yüzeyinden elektron koparabilmek için gelen ışınların
enerjisi yeterince yüksek yani kısa dalga boylu olmalıdır.
(örneğin;UV)
Yüzeyi parlatılmış, negatif yüklü Zn plaka
10
Fotoelektrik Olay
Işığın tanecik özelliklerindendir.
Metal yüzeyine gelen ışık elektron koparır.
Gelen ışığın frekansı arttıkça kopan elektronların kinetik enerjisi artar.
Gelen ışığın frekansı belirli bir eşik değerin (o ) altında ise elektron
koparamaz, elektronların kopması ışığın şiddetine bağlı değildir.
E=E0+Ek
h= h 0 +1/2 mV2 Ek=h(- 0 )
e- ların kinetik enerjisi
Gelen ışık enerjisi
İş fonksiyonu
veya
eşik enerjisi
11
12
ELEKTROMANYETİK SPEKTRUMDA BÖLGELER
VE ELEKTRONİK GEÇİŞLER
MaLıM YaSTıK
13
Elektronik Geçişler
Gözlerimiz; güneşten gelen görünür ışığa karşı duyarlıdır. Oysa bazı yılanlar IR
ışınlarına karşı, bazı böcekler de UV ışınlarına karşı duyarlıdır.
Öyleyse; ışınlar enerji taşır, elektronlar ışınları soğurur ve sonra yayar.
İnsan gözü; katı yüzeyinden yansıyan veya bir sıvıdan geçen ışını analiz
eden bir spektrometre gibi çalışır.
14
En sık gözlenen geçişler;
* ve n *
Elektronik spektroskopide 200-800 nm arasında çalışıldığından bu
bölgedeki ışın enerjileri ancak nπ* ve ππ* geçişlerini sağlayacak
enerjiye sahiptir.
15
Madde-Işın Etkileşmesi
1-Işının
2-Işının
3-Işının
4-Işının
5-Işının
6-Işının
geçmesi ve kırılması (refraksiyonu)
dağılması (dispersiyonu)
yansıması (reflection)
saçılması (scattering)
polarizasyonu
absorpsiyonu
16
Işının geçmesi ve kırılması
Işın bir ortamdan ikinci bir ortama geçtiğinde
kısmen yansır, kısmen de ikinci ortama geçer.
İkinci ortamda ilerleyen ışının frekansı değişmez,
ilerleme yönü ve hızı değişir. Bu değişim, ışının
10-15 sn gibi bir süre maddenin bağ
elektronlarınca alıkonulmasından ileri gelir.
Işın, maddenin atom veya molekülleri ile etkileşir.
Bu etkileşim, ışının elektriksel alanı ile maddenin
bağ elektronları arasında olur.
17
Işın demetinin bir ortamdan yoğunluğu farklı başka bir
ortama geçerken yön değiştirmesine kırılma (refraksiyon)
adı verilir.
Kritik açının ölçülmesiyle her madde için farklı kırılma indisi
belirlenmiştir.
18
Kırılma indisi değerleri, maddelerin belirgin
özelliklerinden biri olarak tanımlanmıştır.
Kırılma indisinin ölçülmesine dayanan
Refraktometri yöntemi:
Kırılma İndisi değerleri;
maddenin nitel ve nicel analizinde,
saflık derecesinin belirlenmesinde kullanılır.
Kırılma indisi ölçümü yapan düzeneğe
refraktometre adı verilir.
Refraktometre, idrar dansitesi ölçümünde sıklıkla kullanılır.
19
Işının dispersiyonu
İçinden geçen ışının dalga boyu veya frekansına göre bir maddenin
kırma indisinin değişmesi olayına dispersiyon denir.
Normal Dispersiyon gösteren maddeler beyaz ışığı
renklerine ayırmadan geçirir. (Mercek)
Anormal Dispersiyon gösteren maddeler ışın demetini
renklerine ayırır. (Ör.Prizma)
20
Işının yansıması (reflection)
Işın, bir ortamdan başka bir ortama
geçerken yansır. Yansımayı iki faktör
etkiler:
Gelen ışının normalle yaptığı açının
büyümesi
Işının içinden geçtiği ortamların
kırma indisleri arasındaki fark
Havadan dik olarak cama gelen (normalle
yaptığı açı 0° olan) bir ışın demetinin ~
%4 ü yansır. 90° de %100 ü yansır.
21
Işının saçılması (scattering)
Işın madde içinden geçerken çok kısa bir süre
alıkonulur. Bu sırada maddenin atom veya
moleküllerinde polarizlenmeler (yük
dağılımında geçici değişmeler) olur ve sonra
madde tuttuğu ışını geri salar.
Bu ise bir sonraki sayfadaki gibi olur:
Sisli havada ışık
saçılması
22
Fotonun örnekteki parçacıklara çarparak yön
değiştirmesine saçılma adı verilir.
-Görünür bölge ışıması kullanıldığında, kolloidal ve
bulanık çözeltilerde gözlenen saçılma, Tyndall
saçılmasıdır.
-Çözünmüş moleküller veya çok atomlu iyonlardan
saçılma Rayleigh saçılmasıdır.
?Gökyüzü neden mavi görünür?
-Parçacıklarla etkileşen dalga boyunun, ışığı saçan
moleküllerin titreşim enerji düzeylerine göre değiştiği
saçılma türü Raman saçılmasıdır.
23
Sisli havada Neden Sarı Sis Farları Kullanılır?
Bunun nedeni;
•Daha rahat bir görüş sağlamasıdır. Göz, en kısa dalga boylu
mavi ve mor renkleri algılamada zorlanır.
•Normal far ışığı, sarı ışığa (550nm) göre daha kısa dalga
boyuna sahiptir.
Işının saçılması ile oluşan Rayleigh Dağılması olduğu
düşünülebilir. Ancak ortalama su damlası veya kar tanesinin
boyutunun (8000 nm) ışığın dalga boyuna (400-700 nm) eşit
veya küçük olduğu durumlarda bu dağılma olayı gözlenebilir.
Burada ise tanecikler bu kadar küçük boyutta değildir.
Dolayısıyla Rayleigh dağılması gerçekleşmez.
24
Işının polarizasyonu
Işık dalgası, genellikle her düzlemde
ilerleyen dalgaların karışımıdır. Tek bir
düzlemde ilerleyen ışık dalgasına
düzlemsel polarize ışık denir.
Düzlemsel polarize ışık ile asimetrik ve
ışığı absorplamayan maddeler etkileştiği
zaman, polarize ışığın düzlemi sağa (+)
veya sola (-) açı değiştirir.
25
Işının absorpsiyonu (soğurumu)
Kuantum kuramına göre atomlar, ancak elektron
konfigürasyonuna ve dış elektronlarının belirli
enerji düzeyleri arasındaki geçişlerine bağlı
belirli potansiyel enerji düzeylerinde
bulunabilirler. Elektronların bir enerji
düzeyinden diğerine geçişleri ile ilgili atomik
spektrumlar belirlenmiştir.
Atomlar, elektromanyetik ışını absorbe ederek en
düşük enerji düzeyinden (temel düzey)
uyarılmış düzeylere geçerler; bu geçişlerle ilgili
olarak söz konusu atomun absorpsiyon
spektrumları da belirlenmiştir.
26
Elektromanyetik ışımayı absorbe ederek en düşük
enerji düzeyinden (temel düzey) uyarılmış düzeylere
geçmiş olan atomlar, temel düzeye dönüş sırasında
ultraviyole veya görünür bölge sınırları içinde ışıma
yaparlar (emisyon). Her atom için emisyon spektrumu
da belirlenir.
Moleküller de atomlarda olduğu gibi uygun enerjideki
fotonlarla etkileştiklerinde bu fotonları absorplayarak
uyarılmış hale geçerler. Uyarılmış moleküller, bu
kararsız durumdan fazla enerjilerini yayarak
kurtulurlar (moleküler emisyon). Atom
spektrumlarından daha karmaşık olan moleküler
spektrumlar da belirlenir.
27
Geçici Dipol Moment
ve Absorpsiyon
Bir maddenin soğurum yapabilmesi için dipol momentinin
ışının elektrik alanıyla etkileşmesi gerekir Bunun sonucu dipol
moment büyür. HCl, H2O gibi maddeler Daimi Dipol Momente
sahiptir.
Cl2, H2 gibi maddelerin durumu Geçici Dipol Moment ile
açıklanabilir.
Ömrü: 10-15 sn
28
Absorplanan fotonların sayısı, ortamda absorpsiyon
yapan türlerin sayısı ile orantılıdır. Monokromatik ve I0
şiddetinde bir ışın demeti, ortamı daha küçük olan I
şiddetinde terk eder.
M + hv M*
M* M + ısı
I0 = I + Ia + Id + Iy
İhmal edilir
Lambert-Beer kanunu: Bir çözeltiden geçen ışık
miktarı, ışığın çözelti içinde aldığı yol ve çözelti
derişimi ile logaritmik olarak ters orantılı,
soğurulan ışık miktarı ise doğru orantılıdır.
29
Beer Kanunu
Lambert Kanunu
30
A = εlc
%Geçirgenlik (T)= 100(I/I0)
Absorbans (A)= -logT = I/I0 = εlc
c çözelti derişimi (mol/L)
l ışığın çözelti içinde aldığı yol (cm)
ε molar soğurum katsayısı (L/mol/cm)
Formüldeki ε değeri denel olarak bulunur. Bunun için
standart çözeltilerden absorbans-derişim grafiği çizilir.
Doğrunun eğimi ε değerini verir.
31
Madde ve Renk
Bir maddenin rengi, o maddeden gözümüze
ulaşan görünür bölgedeki elektromanyetik
ışınlardır. Bu ışınlar, saydam maddeler için
maddenin içinden geçip gelen, saydam
olmayanlar için ise yansıyan ışınlardır.
Maddelerin rengi, maddelerin tuttuğu ışının
tamamlayıcısı olan ışının rengidir.
32
konjugasyon
Ana Renkler: Kırmızı, Yeşil, Mavi.
Görünen renk Soğurulan renk Işık (nm)
Mavi-yeşil
Kırmızı
620-700
Yeşil-mavi
Portakal
600-620
Sarı
575-600
Sarı-yeşil
555-575
Yeşil
505-555
Mavi-yeşil
495-505
Yeşil-mavi
475-495
Sarı
Mavi
440-475
Sarı-yeşil
Menekşe
380-440
Mavi
Renk Çarkı
Menekşe
Mor
Kırmızı
Portakal
UV Alanı
220-380
MaLıM YaSTıK
33
Çözelti içindeki madde miktarını çözeltinin
renginden faydalanarak ölçme işlemine
kolorimetri, bu tip ölçümde kullanılan
cihazlara da kolorimetre denir.
Kolorimetrik ölçümde, konsantrasyonu
ölçülecek çözeltinin rengi değişik
konsantrasyonlardaki standartların rengiyle
karşılaştırılarak değerlendirilir.
34
Organik Maddelerin Absorpsiyonu
ve Renklilik
Organik maddelerin yapısında bulunan her grup kendine
has dalga boyunu soğurur. Bu gruplara bağlı yan
grupların değişimiyle soğurum veya dalga boyu azalır
veya artar.
C=O (Karbonil Grubu): Yan gruplar, -OH, -NH2, -Cl,
alken gibi olabilir. Bu gibi gruplar %30’a varan
kaymalara neden olurlar.
C=O, NO2, N=N Bu grupların varlığında madde 400800 nm arasında soğurum yapar. Böyle gruplara
Kromofor gruplar denir.
Bunların bulunduğu her madde renkli değildir. Ancak her renkli
madde de bu gruplardan vardır.
35
-NH2, -OH Kendileri renkli değildir ancak
bulundukları maddenin renk tonunu artırırlar. Bu tür
gruplara ise Oksokrom Gruplar denir.
Renkli ve renksiz maddeler arasında fark var mıdır?
Yoktur. Çünkü renkliler görünür bölgede, renksizler ise bu
bölgenin dışında soğurum yaparlar.
36