MADDENİN HALLERİ VE ISI
8.SINIF
6.ÜNİTE
KONU
NO: 21
*ÖZ ISI - ISI ALIŞVERİŞİ VE SICAKLIK DEĞİŞİMİ*
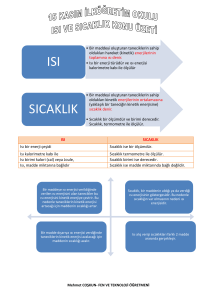
Bir gram maddenin sıcaklığını 1 C arttırmak için gerekli ısı miktarına
öz ısı denir.
Öz Isı;
Küçük "c" ile gösterilir.
O
O
Birimi, Cal/g C ya da J/g C olarak ifade edilir.
Öz ısı, madde miktarına bağlı olmayıp maddenin cinsine (türüne)
bağlıdır.
Saf maddeler için ayırt edici bir özelliktir. Yani her maddenin
kendine özgü bir öz ısısı vardır.
Öz ısısı büyük olan madde geç ısınıp, geç soğurken; öz ısısı küçük
olan madde erken ısınıp, erken soğur.
Günlük Hayatta Kullandığımız Bazı Maddelerin Öz Isıları
Madde
Öz Isı (J/gOC)
Öz Isı (Cal/gOC)
Su
4,18
1
Cıva
0,12
0,03
Alkol
2,40
0,57
Demir
0,45
0,11
Alüminyum
0,91
0,22
*** Yukarıdaki tabloda görüldüğü gibi suyun öz ısısı 1 kalori ya da
4,18 joule'dür. Bu durumda;
1 Kalori (Cal) = 4,18 Joule (J)
O
O
Örnek: 10 C sıcaklığındaki 100 gram demirin sıcaklığını 11 C'ye
çıkarmak için gereken ısı miktarını kalori ve joule cinsinden
hesaplayınız.
Çözüm: Yukarıdaki tabloda verildiği gibi demirin Öz ısısı (yani 1
O
gramının sıcaklığını 1 C arttırmak için gerekli olan ısı miktarı) 0,11
kaloridir.
O halde;
100 gram x 0,11 kalori = 11 Kalori
11 kalori ise, 11 x 4,18 = 45,98 Joule
O
O
Sonuç olarak 100 gram demirin sıcaklığını 1 derece (10 C 'den 11 C
'ye) arttırmak için gereken ısı miktarı 11 Kalori ya da 45,98
Joule'dür.
www.fensepeti.com
O
::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::
ÖZ ISI
::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::
Bu konu anlatımı seti Metin GÖKTÜRK tarafından hazırlanmıştır. Konu anlatım seti ve diğer setler için www.fensepeti.com sitesini ziyaret edebilirsiniz. 2017 ©
Suyun öz ısısı 1 kalori (4,18 joule) 'dir. Öz ısı madde
miktarına bağlı olarak değişmez.
Yukarıdaki görselde verildiği gibi bir damla suyun da bir okyanus
dolusu suyunda öz ısısı 1 kalori ya da 4,18 joule 'dür.
Öz ısı maddeler için ayırt edici bir özelliktir. Her
maddenin kendine özgü öz ısısı vardır.
Demir
Bakır
Alüminyum
Yukarıda görselleri sırasıyla verilen demir, bakır ve alüminyum
maddelerinin öz ısıları 0,45 , 0,37 ve 0,91 joule' dür.
Öz ısısı büyük olan madde geç ısınıp, geç soğurken; öz
ısısı küçük olan madde erken ısınıp, erken soğur.
Suyun öz ısısı karadan fazla olduğundan sonbaharda, kışa
girerken karalar denizlerden daha erken soğurken; kıştan
ilkbahara geçişte ise karalar denizlerden daha erken ısınır.
Hatırlatma ..!
Günlük yaşantımızda ısı ile sıcaklık kavramları
genelde karıştırılmaktadır. Oysa ki ısı, bir maddenin
taneciklerinin kinetik (hareket) enerjilerinin toplamı
iken; sıcaklık, bir maddenin taneciklerinin ortalama
kinetik (hareket) enerjisinin bir göstergesidir.
Benzetme: Bir öğrencinin Fen Bilimleri dersi notlarının
toplamı ısı ise bu notların ortalaması sıcaklıktır.
Sıcaklığı yüksek tanecikler
Madde taneciklerinin hareketi maddenin sıcaklığı ile doğru
orantılıdır. Bu nedenle bir maddenin sıcaklığı arttığında maddenin
taneciklerinin hareketi de o oranda artar.
Aşağıda ısı - öz ısı ilişkisi, ısı - kütle ilişkisi ve ısı - sıcaklık ilişkisi ele
alınacaktır.
ISI - ÖZ ISI İLİŞKİSİ
Daha önce bahsettiğimiz gibi öz ısısı büyük olan madde geç ısınıp,
geç soğurken; öz ısısı küçük olan madde erken ısınıp, erken soğur.
Bu durumu örnekleyecek olursak;
A
B
Kütlesi: 50 g
Sıcaklık: 40 0C
Öz Isı: 1,50
Kütlesi: 50 g
Sıcaklık: 40 0C
Öz Isı: 3,50
Yukarıda verilen kütleleri ve ilk sıcakları eşit A ve B maddelerinin
0
sıcaklıklarını 60 C 'ye çıkarabilmek için verilmesi gereken ısı miktarı
aynı olmaz. Bunun nedeni B maddesinin öz ısısının A maddesinin öz
ısısından büyük olmasıdır. Bu durumda öz ısısı küçük olan A
maddesi hemen ısınırken, öz ısısı büyük olan B maddesi hemen
ısınmaz ve ısı almaya devam eder.
0
Sonuç olarak; B maddesinin 60 C 'ye ulaşması için alması gereken
0
ısı miktarı, A maddesinin 60 C ' ye ulaşması için alması gereken ısı
miktarından fazladır.
ISI - KÜTLE İLİŞKİSİ
Isı, madde taneciklerinin kinetik enerjisinin toplamıdır. O halde iki
aynı tür maddeden kütlesi büyük olan madde daha yavaş ısınır,
daha yavaş soğur.
A
Kütlesi: 50 g
Sıcaklık: 10 0C
Öz Isı: 1,50
A
Kütlesi: 100 g
Sıcaklık: 10 0C
Öz Isı: 1,50
::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::
Sıcaklığı düşük tanecikler
www.fensepeti.com
Maddeler atomlardan dolayısıyla taneciklerden meydana
gelmişlerdir. İster katı ister sıvı ister gaz olsun tüm maddelerin
tanecikleri hareket halindedir.
::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::
ISI ALIŞ VERİŞİ VE SICAKLIK DEĞİŞİMİ
O
O
Yukarıda ilk sıcaklıkları 10 C olan A maddelerinin sıcaklıkları 40 C
'ye çıkarılmak istendiğinde kütlesi 100 g olan maddeye, kütlesi 50 g
olan maddeye göre daha fazla ısı verilmelidir. Bu durum kütle
arttıkça maddeye verilmesi gereken ısının arttığını göstermektedir.
Günlük hayattan örnek: Özdeş iki ocak üstünde bir
bardak su mu bir çaydanlık su mu daha erken kaynar?
ISI - SICAKLIK İLİŞKİSİ
Aşağıda içerisinde 20'şer gram ve ilk sıcaklıkları eşit su bulunan
kaplar verilmiştir. Bu kaplardan birini 1, diğerini 2 özdeş
ısıtıcıyla ısıttığımızda Y kabındaki suyun daha yüksek sıcaklığa
sahip olduğu görülmektedir. Bu durumda maddeye verilen ısı
arttıkça maddenin sıcaklığı artar sonucuna ulaşılır.
X
Y
Kütlesi: 20 g
Sıcaklık: 10 0C
Öz Isı: 1
Kütlesi: 20 g
Sıcaklık: 10 0C
Öz Isı: 1
Yukarıda verilen başlıklar incelendiğinde ısı ile öz ısı, kütle ve sıcaklık
arasında bir ilişkinin olduğu görülecektir. Bu ilişki aşağıda verilmiştir.
Q=m.c.
Q: Isı
m: Kütle
t
c: Öz ısı
t: Sıcaklık Farkı
Verilen formülden de anlaşılacağı gibi bir maddeye verilen ısı; o
maddenin kütlesi, öz ısısı ve maddenin son sıcaklığı ile ilk sıcaklığı
arasındaki farkın (sıcaklık farkı) çarpımına eşittir.
0
0
Örnek : 200 gram suyun sıcaklığını 10 C' dan 20 C'a çıkarmak için
O
verilmesi gereken ısı miktarı kaçtır? (csu = 4,18 J/g C)
Çözüm : Yukarıdaki soruda bir maddenin yani suyun sıcaklığını
arttırmak için verilmesi gereken ısı miktarı (Q) istenmiştir. O halde;
Q=m.c.
t
formülünü kullanırız. Soruda verilenlerden yola çıkarak,
m = 200 gram
O
0
csu = 4,18 J/g C
t = 20 - 10 = 10 C
Bu durumda,
Q = 200 . 4,18 . 10 = 8.360 Joule
0
0
Sonuç: 200 gram suyun sıcaklığını 10 C arttırmak için (10 C 'dan
0
20 C 'a) gerekli olan ısı miktarı 8.360 joule 'dür.