ALTINCI HAFTA
Deney No: 6
Reaksiyon Isısının Hesaplanması
Deney No:6
Reaksiyon Isısının Hesaplanması
Teori:
Deneyde reaksiyon ısısı, molar ısı kapasite, spesifik ısı ve
kalorimetre kavramlarını irdelenecek ve bir reaksiyon ısısı
hesaplanacaktır. Termodinamik, fiziksel ve kimyasal olaylara
eşlik eden enerji değişimlerini inceler. Kimyasal termodinamiğin
yasaları, belirli koşullarla belirli bir kimyasal tepkimenin
kuramsal olarak oluşup oluşmayacağını önceden tahmin
etmemizi sağlar. Tepkime ısısı, sabit sıcaklık ve sabit basınçta
yürüyen bir kimyasal tepkimede sistem ile çevresi arasında
alınıp verilen ısı miktarıdır. Tepkime ısıları deneysel olarak
kalorimetre denilen ve ısı miktarını ölçen aletlerle belirlenir. Bir
tepkime yalıtılmış bir sistemde gerçekleşirse yani çevresi ile
madde ve enerji alışverişinde bulunmazsa, tepkime sistemin
ısısal enerjisinde değişme meydana getirir ve sıcaklık artar
yada azalır.
Deney No:6
Yaratılmış bir sistemde sıcaklık artışına neden olan yada
yalıtılmamış bir sistemde çevreye ısı veren bir tepkimeye
ekzotermik tepkime denir. Ekzotermik bir tepkimede, tepkime
ısısı negatif (qtep<0) bir büyüklüktür. Yalıtılmış bir sistemde
sıcaklığın azalmasına neden olan yada yalıtılmamış bir
sistemde çevreden ısı alan bir tepkimeye de endotermik
tepkime denir. Bu durumda tepkime ısısı pozitif (qtep>0) bir
büyüklüktür. Isı, sıcaklık farkından ileri gelen enerji alışverişidir.
Sıcak bir cisimden soğuk bir cisme enerji aktarımı ısı şeklinde
olur. Bir sistemin sıcaklığını bir derece değiştirmek için gerekli
ısı miktarına o sistemin ısı kapasitesi denir. Sıcaklık değişimi:
Burada Ts son sıcaklık, Ti ilk sıcaklıktır.
Deney No:6
Sistemin sıcaklığı artarsa Ts>Ti dir ve ΔT pozitiftir. q nun pozitif
olması ısısın soğurulduğunu, ada sistem tarafından
kazanıldığını belirtir. Sistemin sıcaklığı azalırsa (Ts<Ti) ΔT
negatiftir. Negatif q ısı açığa çıktığını yada ısı kaybedildiğini
gösterir.
Termodinamiğin birinci yasası enerjinin korunumu yasasıdır.
Sistem ve çevresi arasındaki etkileşimlerde toplam enerji sabit
kalır. Diğer bir deyişle evrenin toplam enerjisi sabittir. Bu yasa
aşağıdaki gibi formülle edilebilir.
qsistem + qçevre = 0
Buna göre, sistemin kaybettiği ısı çevresi tarafından kazanılır,
çevrenin kaybettiği ısı sistem tarafından kazanılır.
Yani:
qsistem = - qçevre
Deney No:6
Reaksiyon Isılarının Ölçülmesi:
Isı miktarını hesaplayabilmek için ısı kapasitesinin bilinmesi
gerekir. Isı kapasitesi faz geçişlerinin olmadığı sıcaklık
aralıklarında iki türlü tanımlanır.
1) Molar ısı kapasitesi: Bir mol maddenin sıcaklığını 1 K veya
1ºC yükseltmek için gerekli olan ısı miktarıdır. Birimi J/Kmol
dür.
2) Spesifik ısı: Bir gram maddeyi 1 K veya 1ºC yükseltmek
için gerekli olan ısı miktarıdır. Birimi J/Kg dır.
ΔT=Ts-Ti (1)
Bu durumda bir cismin aldığı veya verdiği ısı iki farklı şekilde
hesaplanabilir.
Isı(q) = mol sayısı × molar ısı kapasitesi × ΔT (2)
Isı(q) = kütle × spesifik ısı × ΔT (3)
Deney No:6
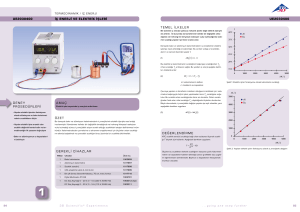
Kalorimetreler:
Reaksiyon ısıları ölçmek için kullanılan aletlerdir. Gerek sabit
hacimde (kapalı kaplarda), gerek sabit basınçta (açık kaplarda,
atmosfer basıncında) reaksiyon ısıları ölçülerek ΔE (iki halin iç
enerjileri arasındaki fark) veya ΔH (entalpi değişimi) deneysel
olarak hesaplanabilir. Her iki halde de önce kalorimetrenin ısı
kapasitesi deneysel olarak belirlenmelidir. Kalorimetrenin
kazandığı ısı:q(J) = kalorimetre ısı kapasitesi (J/K) ×ΔT(K) (4)
bağıntısı kullanılarak kalorimetrenin ısı kapasitesi hesaplanır.
Bu hesap yapıldıktan sonra kalorimetre ısı kapasitesi yerine
konarak reaksiyon ısıları sadece kalorimetre içindeki sıcaklık
yükselmesi (veya azalması) okunarak bulunur. Çözelti
kalorimetre laboratuarda bir termos yada alüminyum yaprakla
ağzı örtülmüş beherlerden yapılabilir.
Deney No:6
Deneyin Yapılışı:
1.Isı kapasitesi tayini: Kalorimetrenin ısı kapasitesi tayini için
beher tipi kalorimetre kullanılır. (ağzı alüminyum folyo ile
kapatılmış 250mL’lik beher içinde beher) Önceden tartılan Cu
parçası(mCu) 30 dakika 100ºC deki etüvde ısıtılır. 250mL lik
behere 100gram saf su (msu) konyulur. Bu suyun sıcaklığı bir
termometre yardımı ile okunur ve kaydedilir (t1). 30 dakika
sonra bakır parçası etüvden alınır ve bakırın ısısını
kaybetmemesi için hemen kalorimetre kabına yerleştirilip son
sıcaklığı kaydedilir (t2). (7) nolu bağıntıyı kullanılarak ısı
kapasitesi hesaplanır.
2.Reaksiyon ısısının hesabı: 1. kısımda kullanılan beher
boşaltılır ve kurutulur. Bu defa reaksiyon ısısı ölçülecek
karışımlar koyulur. Behere 100 gram seyreltik HCl çözeltisi
koyulur ve çözeltinin sıcaklığı okunarak kaydedilir (t1).
Deney No:6
Önceden tarttılan magnezyum parçası çözeltiye atılarak
reaksiyon tamamlanınca sıcaklık okunur (t2). (8) nolu bağıntı
kullanılarak reaksiyon ısısı hesaplanır.
Aşağıdaki reaksiyonun reaksiyon ısısı hesaplanacaktır:
Hesaplamalar:
1) Termodinamiğin birinci kanununa göre kaybedilen ısı
kazanılan ısıya eşit olmalıdır. Bir başka değişle kazanılan ve
kaybedilen ısıların toplamı sıfır olmalıdır.
q bakırın kaybettiği = q suyun kazandığı + q kalorimetrenin kazandığı (6)
mCu × CCu* × (100-t2) = msu × Csu*(t2-t1) + Isı kapasitesi*(t2-t1) (7)
* : CCu = 0,385 J/Kg
* : Csu = 4,18 J/Kg
Deney No:6
Reaksiyon ısısı = Isı kapasitesi × (t2-t1) + çözeltinin kütlesi × Cçözelti × (t2-t1) (8)
Cçözelti = 4,21 J/Kg
Sonuçlar:
Beherin ısı kapasitesi:.........................................................
Reaksiyon ısısı: ................................................................