• Dünya belli bir düzen ve uyum içerisinde kurulmuştur ve
bu durumu devam ettirmektedir.
Biyolojik Süreçler ve
Denge
• Bu işleyiş içerisinde bütün canlılar hayat aktivitelerini
sürdürebilmek için çevre ve diğer canlılarla etkileşim
halindedir.
• Bu etkileşime yaşamsal denge denir.
Denge (Homeostasi)
• İnsanda kan hücreleri, insanda homeostasi oluşmasını
sağlar.
• Homeostasi değişen dış koşullara rağmen nispeten sabit
bir iç fizyolojik ortamı sürdürme sürecidir.
• Böylece vücut organlarının, normal sınırlarda verimli bir
şekilde çalışmasını sağlar.
• Tek hücreli ya da çok hücreli tüm organizmalarda denge
(homeostasi) görülmektedir. Bu sürece bazı örnekler;
• Hücresel düzeyde pH değerinin ayarlanması
• Organizma düzeyinde vücut sıcaklığının sabit tutulması
• Ekosistem düzeyinde bitkilerin karbondioksit fazlalığında
daha hızlı büyümesi
Denge (Homeostasi)
Denge (Homeostasi)
• Canlı vücudunda gerçekleşen denge sistemleri:
• Yaşamak için gerekli olan tüm fizyolojik ve kimyasal
işlemler (metabolizma) su ile gerçekleşir.
• Sıvı – elektrolit dengesi
• Asit – baz dengesi
• Vücut ısısının değişmesi
• Kanda karbondioksit taşınması
Denge (Homeostasi)
• O yüzden suyun olmadığı bir ortamda canlılıktan söz
edilemez.
• Canlıların metabolizmasında sadece sudan bahsedilemez.
• Hem su hem de su içerisinde yer alan elektrolit ve
elektrolit olamayan maddeler içerir
Sıvı-Elektrolit Dengesi
1
• Suyun vücudumuzdaki fonksiyonları;
• Maddelerin hücre içine ve dışına taşınmasını sağlar
• Hücredeki faaliyetler için gerekli olan katı madddeleri çözer
• Vücut sıvılarının fizyolojik ve kimyasal işlemlerinin
devamlılığını sağlar
• Besinlerin en küçük birimlerine bölünmesini ve
sindirilmesini sağlar
• Kan hacmini ayarlar. Metabolizma sonucu oluşan atıkların
vücuttan atılmasını sağlar
• Vücut ısısını düzenler
Sıvı-Elektrolit Dengesi
• Bir yetişkinin ağırlığının yaklaşık %60’ı sudur
• Yeni doğan bebeklerde bu oran %75’tir
• Normal koşullarda 24 saat içinde, vücudumuza alınan ve vücuttan atılankaybedilen sıvı miktarları dengededir.
• Bu denge, ateşli hastalıklar, ishal-kusma gibi durumlarda bozulabilmektedir.
• Bazen de alınan çıkandan fazla olabilmektedir.
• Bu durumda vücudun dengeleme sistemi devreye girerek herhangi bir sorunun
oluşmasını engeller.
Sıvı-Elektrolit Dengesi
• Su kaybında vücudun tepkileri:
• Toplam vücut ağırlığına göre;
• %1: susama hissi oluşur
• Hücre içindeki (intrasellüler) sıvı= %45
• %5-8: halsizlik, nabızda ve vücut ısısında artma
• Hücre dışındaki (ekstrasellüler) sıvı= %15
• %11-15 (Deliryum): genellikle bilinç durumunda oluşan
bozukluklarla ortaya çıkan akut organik beyin sendromudur.
• %20 (Ağır dehidrasyon): deri buruşur, vücuttan terle karışık kan
sızar, gözyaşı yerine kan gelir.
Sıvı-elektrolit Dengesi
Sıvı-Elektrolit Dengesi
• Normal bir kişinin günlük su ihtiyacı:
• Az su tüketimi
• Yaşa
• Cinsiyete
• Vücut yapısına
• Vücut metabolizmasına
• Ne is yaptığına (fiziksel aktivitesine)
• Hava sıcaklığına
• Sağlık durumuna (mide bozulması, ishal vb.)
değişkenlerine bağlıdır
Sıvı-Elektrolit Dengesi
• Depolanan yağ miktarında artış gözlenir
• Vücut kendinde bulunan suyu tutmaya çalışır
• Metabolizmanın yavaş çalışmasına sebep olur
• Besinlerin sindirilmesinde ve emilmesinde problemler
meydana gelir
Sıvı-Elektrolit Dengesi
2
• Aşırı su tüketimi
• Kandaki sodyum miktarının düşmesine (hiponatremi)
• Hücrelerin su alarak şişmesine
• Ciddi fiziksel sorunlara
• Beyin ödemine ve ölümüne neden olabilmektedir
Sıvı-Elektrolit Dengesi
• Elektrolitler, vücut sıvılarında çözünmüş olarak bulunan
yüklü taneciklerdir.
• Vücut sıvısında bulunan eriyik halindeki maddelerin
çoğunu elektrolitler oluşturur.
• Elektrolitlerin görevleri şunlardır:
• Vücut sıvılarının ozmolaritesini (bir litre suda çözünen
toplam partikül sayısı) sağlar
• Nöromuskular (sinir-kas) uyarımını sağlar
• Vücut sıvılarının olması gerektiği oranlarda dağılımını
sağlar
Elektrolitler
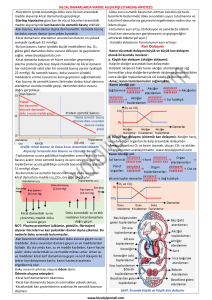
• Sıvı ve Elektrolitlerin Hareketi
Sıvı – Hücre
Etkileşimi
• Ozmolarite: Bir litre suda çözünen toplam partikül sayısıdır.
Yoğun olarak adlandırılan sıvının ozmolaritesi fazladır.
• Ozmoz: Yarı geçirgen zarla ayrılmış farklı ozmolariteleri olan iki
sıvı söz konusu olduğunda, su ozmolaritesi fazla olan tarafa
geçmeye çalışır. Diğer bir ifadeyle, ozmoz, suyun düşük
yoğunluklu ortamdan yüksek yoğunluklu ortama geçme isteğidir.
Hipertonik Sıvı
ve Hücre
Hipotonik Sıvı
ve Hücre
• Ozmotik basınç: Ozmozu engellemek üzere gereken basınç
miktarıdır.
Elektrolitler
• Hipertonik Sıvı ve Hücre
• Hücre dışındaki ortamın ozmotik basıncının hücre içi ozmotik
basıncından daha yüksek olduğu ortamlara hipertonik ortam denir
• Hipertonik ortamdaki hücreler dış ortamdan daha yoğun oldukları
için su kaybederek büzüşürler
• Hücrenin su kaybetmesi olayına plazmoliz denir
• Hipotonik Sıvı ve Hücre
• Hücre içindeki ortamın ozmotik basıncının hücre dışı ozmotik
basıncından daha yüksek olduğu ortamlara hipotonik ortam denir.
• Hipotonik ortamdaki hücrelerde iç ortam daha yoğun olduğu içi
su alarak şişerler.
• Hücrenin su alarak şişmesi olayına deplazmoliz denir.
Elektrolitler
Elektrolitler
• Canlıların metabolizmasındaki reaksiyonların hemen
hepsi optimum bir pH ortamında gerçekleşir.
• Ortamın pH değerinin değişmesi, önemli bozukluklara
hatta ölümlere bile sebep olabilir.
• Asit-baz dengesini koruyan ve sürdüren sistemler:
• Tampon sistemler
• Solunum sistemleri
• Boşaltım sistemleri
Asit-Baz Dengesi
3
• Asit-baz dengesini koruyan ve sürdüren sistemler
• Tampon sistemler: Asit-baz dengesi bozulduğu anda
hemen tepkime verir
• Solunum sistemi: Biraz geç tepkime verir. Soluk alıp
vermeyi hızlandırarak ya da yavaşlatarak CO2 atılımını
dengelemeye çalışır
• Boşaltım sistemi: Oldukça geç tepki verir.
Asit-Baz Dengesi
4