Hazırlayan: Ebru KOYUNCU
Yenişehir Y.İ.B.Okulu
UŞAK
Fen ve Teknoloji 8
www.fenokulu.net
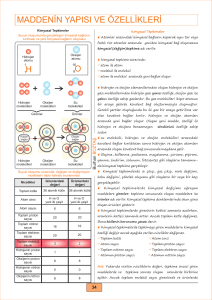
KİMYASAL TEPKİMELER
Elementlerin kaç tane e-alacakları ya
da verecekleri bulunur.
Anahtar Kavramlar
İyonlar yazılır.(Mg+2
Son olarak çaprazlama yapılır.
Kimyasal Tepkime
Kimyasal Denklem
Cl-1)
*Kalsiyum ve Flor atomlarının oluşturacağı
bileşiğin formülünü bulalım.
Yanma Tepkimesi
2 e12Ca
KAZANIM 3.1
= 2) 8) 8) 2)
Ca
1 e-
Yükü bilinen iyonların
oluşturduğu
9F
bileşiklerin
F-1
= 2) 7)
formüllerini yazar.
KAZANIM 3.2
+2
Çok
yaygın
Ca Atomlu
F-1
iyonların oluşturduğu
element atomlarının
formülünü bulalım.
sayısını hesaplar.
-
2e
Mg+2
=2) 8) 2)
1e17Cl
= 2) 8) 7)
Mg+2
Çok Atomlu İyonlar
Cl-1
Cl-1
MgCl2
Bileşik formülü bulunurken;
CaF2
bileşiklerin formüllerinde
*Mg ve Cl atomlarının oluşturacağı bileşiğin
12Mg
+2
Verilen elementlerin e- dizilimleri
yapılır.
1
İyonun Adı
İyonun Formülü
Hidronyum
H 3O
Amonyum
NH4-
Nitrat
NO3-
Hidroksit
OH-
Karbonat
CO3-2
+
Hazırlayan: Ebru KOYUNCU
Yenişehir Y.İ.B.Okulu
UŞAK
Fen ve Teknoloji 8
www.fenokulu.net
Sülfat
SO4-2
Al2(CO3)3
Fosfat
PO4-3
Ca(NO2)2
siyanür
CNMg(NO3)2 =
(NH4)PO4
KAZANIM 3.3
Mg 1
N 2
Kimyasal bir tepkimenin
9
gerçekleştiğini deneyle
O 6
Na3PO4
=
gösterir.
Na 3
P 1
8
O 4
Dün okuldan eve giderken karnım
çok açıkmıştı adeta zil
çalıyordu.Sokak kapısını açıp
merdivenleri çıkmaya başladığımda
İyon
Formüldeki
burnuma harika kokular
geliyordu.Annem akşam yemeği için
Katyon
toplam
Anyon
İçerdiği
Formülü
Elementler
Bileşik
patates kızartması yapıyordu.
atom
Üzerimi değiştirip hemen mutfağa
sayısı
geçtim.Annem kendisine yardım
edebileceğimi söyledi.Annemin
NaOH
soyduğu patatesleri ben
kesiyordum.Sonra da kızartma
(NH4)SO4
tenceresine koyup kızarmış
Be(OH)2
patatesleri alıyorduk. Tabii
kızarmış patatesler bir taraftan
NaHCO3
eksiliyordu çünkü ben
Ca3(PO4)2
atıştırıyordum. Sonra Aklıma fen
ve teknoloji öğretmenimizin derste
AlPO4
anlattıkları aklıma geldi. Kızarmış
patates KİMYASAL DEĞİŞİM’ e
PB3(PO4)4
uğruyor. Çünkü kızarmış patates
tekrar çiğ patates olamaz
2
Hazırlayan: Ebru KOYUNCU
Yenişehir Y.İ.B.Okulu
UŞAK
Fen ve Teknoloji 8
www.fenokulu.net
KİMYASAL TEPKİME= Element ya da bileşiklerin
KİMYASAL DEĞİŞİM= Maddelerin iç yapısında
kimyasal değişime uğrayarak yeni maddeler
meydana gelen değişimlerdir.
oluşturduğu olaylara KİMYASAL TEPKİME denir.
Kibritin yanması
Kimyasal Tepkimelerde atomların tür ve
sayısı değişmez dolayısıyla;
Kağıdın Yanması
Mumun Yanması
-Toplam Kütle,
Yumurtanın Pişmesi
-Toplam proton ve nötron sayıları,
Yemeğin pişmesi…
-Toplam elektron sayısı,
KAZANIM 3.4
-Toplam yük;
Kimyasal Değişimi atomlar
DEĞİŞMEZ!!!!
arası bağların kopması ve
yeni bağların oluşması
Hidrojen
temelinde açıklar.
Kimyasal Değişimlerde maddeyi oluşturan
atomlar arasındaki bağlar kopar ve yeni bağlar
+
Oksijen
2H2
+
O2
4 gram
+
32 gram
Su
2H2O
36 gram
[H=1 gram, O= 16 gram]
oluşur.
N2 + 3H2
Kimyasal Değişimlerde atomların proton ve
2NH3
nötron sayılarında herhangi bir değişim olmaz.
Tepkime denklemine göre; 112 gram N2
Sadece elektron sayıları değişir.( Elektron alış-
gazı yeterince H2 gazı ile tepkimeye
verişi ya da ortaklaşması ile)
giriyor.Sonuçta 136 gram NH3 gazı oluşuyor.
Buna göre; harcanan H2 gazı kaç gramdır?
Kimyasal Değişimler sonunda atomların cinsi
değişmez.Sadece aralarındaki bağların yeri ve
N2
sayısı değişir.
112 g.
KAZANIM 3.5
atomların yok olmadığını
ve yeni atomların
korunduğunu açıklar.
2NH3
+
136 g.
?
136-112= 24 gram. H2 gazı oluşur.
Kimyasal Değişimlerde
oluşmadığını, Kütlenin
+ 3H2
3
Hazırlayan: Ebru KOYUNCU
Yenişehir Y.İ.B.Okulu
UŞAK
Fen ve Teknoloji 8
www.fenokulu.net
Mg= 1
KAZANIM 3.6
1H
2
H= 2
1/2 O
+
O= 2
1H O
2
2
_____
2
H= 2
Cl= 2
1
Al= 1
yöntemi ile denkleştirir.
Cl= 1
______
2
denklemlerini sayma
Mg= 1
______
2Al + 3H SO
Basit Kimyasal Tepkime
H= 1
4
_______
1Al (SO )
2
4 3
Al= 2
S=1
S= 3
O= 4
O=12
1
______
3*
H= 2
_______
H=2
2
+
2
H= 2
__________
7
3H
_______
17*
2
O= 1
______
________
_______
1Fe S
2
2
2
3 *
3
+
4O
Fe= 2
Tepkimeye giren ve çıkan bileşiklerdeki
2
O= 2
S= 3
atom sayıları bulunur.
________
En fazla atom sayısına sahip olan bileşik
bulunur.
Fe2O3 +
3SO
Fe = 2
O = 3
________
5*
2
_______
2
S=1
O = 3
_______
5*
4
En fazla atom sayısına sahip bileşiğin
önüne 1 yazılır.
Eğer girenler ve ürünlerde en fazla atoma sahip
“Girenler ve ürünlerin atom sayıları eşit
iki tane bileşik varsa ; bunlardan içinde H ve O
olması gerekir.” Kuralına göre
atomları olmayan ya da en az olan bileşiğin
denkleştirme yapılır.
başına 1 yazılır.
Denkleştirme yapılırken H ve O atomları
en sona bırakılır.
1 Mg + 2 HCl
1 MgCl
2
+
1H
2
4
Hazırlayan: Ebru KOYUNCU
Yenişehir Y.İ.B.Okulu
UŞAK
Fen ve Teknoloji 8
www.fenokulu.net
(propan)
B) YAVAŞ YANMA= Yanma olayı uzun sürede
Ve alev,ateş olmadan gerçekleşiyorsa Yavaş
Yanma olarak adlandırılır.
KAZANIM 3.7
Demirin paslanması,oksitlenme,Besinlerin
hücrelerimizde yakılması……
Yanma Tepkimelerini
tanımlayarak basit yanma
2Fe + 3/2 O2
tepkimelerini formüllerle
C6H12O6
gösterir.
(Besin)
YANMA TEPKİMELERİ= Bir maddenin oksijen ile
Tepkimeye girmesi olayına YANMA TEPKİMESİ
Denir.
Yanma Olayının gerçekleşebilmesi için
ortamda; - Yanıcı Madde
- Oksijen Gazı
- Yeterli Sıcaklık
Olması gerekir.
A) HIZLI YANMA= Gözle görülür alev ve ateş
İle gerçekleşen yanma çeşidine Hızlı Yanma
Denir.
Odunun yanması, kağıdın yanması, mutfak
tüplerindeki propan(C3H8) gazının yanması,Doğal
gazın yanması……
C3H8 + 5O2
3CO2 + 4H2O
5
+
6O2
Fe2O3
6CO2
+
6H20