ANKARA ÜNİVERSİTESİ
SAĞLIK BİLİMLERİ ENSTİTÜSÜ
BİYOKİMYA
BİYOKİMYA LABORATUVARINDA KULLANILAN
CİHAZLAR VE EKİPMANLAR
DERYA ÜNAL
DOKTORA
ANKARA
2017
İÇİNDEKİLER
1. ALETLER ..................................................................................................................................................................... 3
1.1 Terazi: ....................................................................................................................................................................... 3
1.2 Işık mikroskobu: ....................................................................................................................................................... 3
1.3 Santrifüj .................................................................................................................................................................... 3
1.4 Spektrofotometre ...................................................................................................................................................... 3
1.5 Su banyosu................................................................................................................................................................ 3
1.6 Etüv........................................................................................................................................................................... 4
1.7 pHmetre .................................................................................................................................................................... 4
1.8 Saf su cihazı .............................................................................................................................................................. 4
1.9 Elektrikli karıştırıcı (vorteks) ................................................................................................................................... 4
1.10 Elektrik ocağı .......................................................................................................................................................... 4
2. CAM EŞYA.................................................................................................................................................................... 5
2.1 Kalitatif Cam Eşya: .................................................................................................................................................. 5
2.1.1 Beher...................................................................................................................................................................... 5
2.1.2 Erlenmeyer............................................................................................................................................................. 5
2.1.3 Piset ....................................................................................................................................................................... 5
2.1.4 Altı düz balon ........................................................................................................................................................ 5
2.1.5 Deney tüpleri ......................................................................................................................................................... 5
2.1.6 Santrifüj tüpleri ...................................................................................................................................................... 6
2.2
Volumetrik Cam Eşya ......................................................................................................................................... 6
2.2.1 Pipet ....................................................................................................................................................................... 6
2.2.1.1 Dereceli pipetler ................................................................................................................................................. 6
2.2.1.2 Büllü pipetler ...................................................................................................................................................... 6
2.2.1.3 Mikropipetler ...................................................................................................................................................... 6
2.2.1.4 Kapiller pipetler .................................................................................................................................................. 6
2.2.1.5 Otomatik pipetler ................................................................................................................................................ 7
2.2.2 Büret ...................................................................................................................................................................... 7
2.2.3 Ölçü silindiri (mezür) ............................................................................................................................................ 7
2.2.4 Ölçü balonu (Balon joje) ....................................................................................................................................... 8
3. DİĞER GEREÇLER ...................................................................................................................................................... 9
3.1 Bunzen beki-ispirto ocağı ......................................................................................................................................... 9
3.2 Porselen kroze........................................................................................................................................................... 9
3.3 Porselen kapsül ......................................................................................................................................................... 9
3.4 Sacayak ..................................................................................................................................................................... 9
3.5 Spatül ........................................................................................................................................................................ 9
3.6 Havan ........................................................................................................................................................................ 9
3.7 Port-tüp ..................................................................................................................................................................... 9
3.8 Baget ....................................................................................................................................................................... 10
3.9 Tahta maşa .............................................................................................................................................................. 10
3.10 Kıl fırça ................................................................................................................................................................. 10
3.11 Desikatör............................................................................................................................................................... 10
3.12 Huni ...................................................................................................................................................................... 10
3.13 Ayırma hunisi ....................................................................................................................................................... 11
3.14 Saat camı .............................................................................................................................................................. 11
3.15 Lastik puar ............................................................................................................................................................ 11
3.16 Vakumlu tüp sistemi ............................................................................................................................................. 11
4. CİHAZLAR .................................................................................................................................................................. 12
4.1 Spektrofotometre .................................................................................................................................................... 12
4.1.1 Işık spektrumu ..................................................................................................................................................... 12
4.2 Atomik Absorpsiyon Spektrofotometre Cihazı ..................................................................................................... 15
4.3 Otoanalizör ............................................................................................................................................................. 16
4.3 Kromotografi .......................................................................................................................................................... 18
4.4.1 Adsorpsiyon kromatografisi: ............................................................................................................................... 19
4.4.2 Partisyon kromatografisi ...................................................................................................................................... 19
4.5 Elektroforez ............................................................................................................................................................ 19
KAYNAKLAR ................................................................................................................................................................. 23
1. ALETLER
Soğutucu ve derin dondurucu: Bazı kimyasalların ve biyolojik materyallerin (doku, kan, vb.)
saklanmasında gereklidir.
1.1 Terazi: Tartımlarda kullanılır.
1.2 Işık mikroskobu: Biyolojik sıvılarda gözle görülemeyecek kadar küçük cisimlerin saptanması
amacıyla kullanılan, merceği çok güçlü optik aygıttır.
1.3 Santrifüj: Dönme ile sağlanan merkez çekim kuvvetinden yararlanılarak çökeltiyi çözeltiden
ayırmak için kullanılan alettir.
1.4 Spektrofotometre: Belirli dalga boyundaki bir ışığın çözelti tarafından emilimini (absorpsiyon)
veya geçirgenliğini (transmitans) ölçmekte kullanılan alettir.
1.5 Su banyosu: Belirli sıcaklıkta nemli ortam sağlanması gereken deneylerde kullanılır.
1.6 Etüv: Bazı deneylerde (hücre kültürü vb.) gerekli olan sabit basınç ve sıcaklıkta kuru ortam
sağlamak, rutin çalışmalarda maddeleri (kimyasal madde, doku vb.) ve cam eşyayı kurutmak için
kullanılır.
1.7 pHmetre: Biyolojik sıvıların, tamponların ve çözeltilerin pH’ını ölçmek ve ayarlamak için
kullanılır.
1.8 Saf su cihazı: En basit şekliyle, suyu buharlaştırarak gaz fazına geçiren ve daha sonra
yoğunlaştırarak arıtan alettir. Çok geliştirilmiş tipleri vardır.
1.9 Elektrikli karıştırıcı (vorteks): Üzerindeki küçük oyuğa yerleştirilen deney tüpünü motor
gücüyle döndürerek karıştıran alettir.
1.10 Elektrik ocağı: Isıtmalarda ilk seçenektir.
2. CAM EŞYA
Sıvıların hacim ölçümünde kullanılan volümetrik cam eşya ile sıvı ve katı maddelerin tartım,
titrasyon, ısıtma gibi işlemlerinde kullanılan, üzerinde alabileceği maksimum hacim yazılı olan
kalitatif cam eşya olarak gruplandırılır.
2.1 Kalitatif Cam Eşya:
2.1.1 Beher: Geniş ağızlı, kenarı sıvı aktarmaya uygun, silindir biçiminde cam kaplardır. Kimya
laboratuvarlarında kullanılan bardağa benzer cam eşyadır. Çözelti hazırlama, maddelerin
karıştırılması, aktarılması, ısıtma ve kristallendirme gibi birçok işlemde kullanılan silindirik biçimƖi
cam malzemelerdir. Yüksek sıcaklığa dayanıklı temper camdan üretilmiştir. Ağız kısmında sıvının
kolayca akması için oluklu bir kısım vardır. Temper cam, işlemsiz cama göre yaklaşık 5 kat daha
dayanıklı olup kırıldığında zar büyüklüğünde parçalara ayrılır. Bu özelliğinden dolayı yaralanma
riskini azaltır, güvenlik camı olarak da kullanılır.
Beher
Erlenmeyer
Piset
2.1.2 Erlenmeyer: Kalitatif işlemlere uygun, özellikle titrasyonda kullanılan, dar boyunlu, tabanı
düz, koni biçiminde cam kaplardır. Alman kimyacı Carl Emil Erlenmeyer tarafından 1861’de
oluşturulmuş ve onun adını almıştır. Özellikle analitik kimya laboratuvarlarında titrasyon
işlemƖerinde kullanılır. Çözelti hazırlamaktan çözelti saklamaya kadar, kristalizasyon işleminden ve
benzer laboratuvar işlemƖerine kadar daha birçok amaçla kullanılmaktadır.
2.1.3 Piset: Camdan veya plastikten yapılmış, saf su koymaya ve aktarmaya yarayan kaplardır
2.1.4 Altı düz balon: Çözelti hazırlamakta kullanılır. Bu balonlar açık aleve tutulduğu takdirde
amyant üzerine yerleştirilmelidir. Direkt ısıtmak için yuvarlak balonlar daha uygundur.
Düz balon
Deney tüpleri
Santrifüj tüpleri
2.1.5 Deney tüpleri: Silindir biçimindedir. Alt kısmı yuvarlak olduğundan porttüp (tüp taşıyıcı) ile
kullanılır. Çöktürme, renklendirme ve diğer laboratuvar işlemleri için gerekli temel eşyadır. İnce
uzun, bir tarafı kapalı bir tarafı açık, içine kimyasalların konulduğu 100 °C sıcaklığa dayanabilen
deney aracıdır. Maddelerin birbirleriyle etkileşimini gözlemek amacıyla kullanılan silindirik
biçimƖi, küçük çaplı cam malzemelerdir. Çeşitli ebatlarda olanları vardır. En sık kullanılanları 15 x
1,5 cm ebadında olanlarıdır. Kalitatif analizlerde basit tanıma deneylerinde kullanılır. Tüpe konacak
saf sıvılar ve çözeltiler tüpün 1/4'ünü geçmemelidir ve analizden sonra tüpler hemen yıkanmalıdır.
Altı dar ve sivri olanları santrifüj tüpü olarak adlandırılır ve küçük tanecikli çökeleklerin
çöktürülmesi için santrifüj cihazı içinde kullanılan cam tüplerdir.
2.1.6 Santrifüj tüpleri: Santrifüj aletinde kullanılır. Altları genellikle koni şeklindedir. Bazı
santrifüjlerde altı yuvarlak tüpler kullanılır. Santrifüj tüplerinin biçimi, kullanıldığı santrifüj tipine
özgüdür.
2.2 Volumetrik Cam Eşya:
2.2.1 Pipet: Bir sıvıdan belirli bir miktar çekmek ve başka bir kaba aktarmak için kullanılan cam
borulardır. Çalışmanın niteliğine göre kullanılmak üzere çeşitli tipleri vardır.
2.2.1.1 Dereceli pipetler: Bu tip pipetlerin, maksimum hacimlerinin altındaki ölçümlerde
kullanılması daha uygundur. Çünkü son damlayı uzaklaştırmak için üflemek gerekir. Örneğin 2
mL’lik bir dereceli pipetle 2 mL’den daha az hacimler ölçülür. Tam 2 mL ölçmek gerektiğinde
büllü pipet tercih edilir.
2.2.1.2 Büllü pipetler: Dereceli pipete göre daha hassas kalibre edilmiş pipetlerdir. Sıvıyı aktarırken
bül (karın) kısmı avuç içerisinde tutularak içindeki havanın genleşmesi ve uçtaki damlayı
itmesi sağlanır.
2.2.1.3 Mikropipetler: 0.005 ten 0.25 mL’ye kadar olan hacimleri ölçmekte kullanılır.
2.2.1.4 Kapiller pipetler: Çok ince cam borucuklardır. Elektroforez ve kromatografi gibi ayırma
yöntemlerinde örneği uygulamak amacıyla kullanılır.
Büllü pipet
Mikropipet
2.2.1.5 Otomatik pipetler: Sabit (tek hacimlik) ve ayarlanabilir tipleri vardır.
2.2.2 Büret: Sıfırdan başlayarak aşağıya doğru derecelendirilmiş, 1, 2, 5, 25, 50 mL’lik
kapsamlarda, altta musluğu olan cam borulardır. Metal kıskaç ile ayaklı bir çubuğa tutturulur ve
titrasyonda kullanılır.
Rodajsız Balon
Büret
Mezür
Ölçü balonu
2.2.3 Ölçü silindiri (mezür): Sıvıların ve idrar gibi biyolojik örneklerin hacim ölçümünde
kullanılan, silindir şeklinde cam borulardır. Ölçümlerdeki kesinliği çok yüksek değildir. Kabataslak
bir tanım yapmak gerekirse mezür için dereceli silindir demek yeterli olabilir. Saf sıvıların ve
çözeltilerin hacmini ölçmek için kullanılan, üzerinde mƖ cinsinden bölmeler bulunan cam kap olarak
da tanımƖayabiliriz. Genel olarak 50-1000 mƖ arası sıvıların hacimƖerini çok daha iyi ölçer.
Biyokimya laboratuvarlarında besiyeri ve boyaların hazırlanışı sırasında kullanılır. Temel kimya ve
analitik kimya laboratuvarı derslerinde ise saf su ya da tampon çözelti gibi sıvı maddelerin
ölçülerek kullanılmasını sağlayan cam malzemedir. Ancak sıvıların yaklaşık hacimƖerinin
ölçümƖerinde ve aktarılmalarında kullanılır, çok hassas ölçü kapları değildir.
2.2.4 Ölçü balonu (Balon joje): Yuvarlak karınlı ve uzun boyunlu, tek bir hacim ölçmeye uygun,
boyunlarında bu hacmi sınırlayan çizgi bulunan kaplardır. Çözelti hazırlamakta kullanılır. Ölçüm
kesinliği
yüksektir.
İçinde
bazı
kimyasal
reaksiyonların
gerçekleştirildiği,
biyokimya
laboratuvarlarında besi yeri hazırlamak için diğer laboratuvar derslerinde de bazı çözeltileri
hazırlamada, ısıtma ve kaynatma işlemƖerinde ve geri soğutucuya takılarak çeşitli deney
düzeneklerinin hazırlanmasında kullanılan cam malzemelerdir. iki veya üç ağızlı olanları da vardır.
Özellikle karıştırma, ekleme ve gaz geçirme gibi işlemƖerin aynı anda yapılması gerektiği
durumƖarda iki ya da üç ağızlı balonlara gerek duyulur. Altı yuvarlak veya düz olabilir. Düz altı
olan balonlar toplama kabı olarak yuvarlak altı olan balonlar ise daha dayanıklı olmaları sebebi ile
basınç ve sıcaklık değiĢmelerinin olduğu durumƖarda kullanılır. Bir de altı armut şeklinde olan
balonlar vardır. Bu tip balonlar ise alçak basınçta çalışıldığında kullanılır. Ağız kısımƖarı rodajlı
olan balonlar da mevcuttur. Resimde gördüğünüz balon, ağız kısmı tek ve rodajsız olan balon
türlerindendir.
3. DİĞER GEREÇLER
3.1 Bunzen beki-ispirto ocağı: Isıtma işleminde kullanılır.
3.2 Porselen kroze: Çözeltileri kuruluğa kadar buharlaştırmak için kullanılan yüksek kenarlı kaptır.
Porselen kroze
Porselen kapsül
Sacayak
3.3 Porselen kapsül: Katı maddelerin açık alevde kurutulmasında kullanılan yuvarlak ve yayvan
kaptır. Bu işlem sırasında ısınan kapsüller bir tahta maşayla alınarak amyant levhalar üzerine konur.
3.4 Sacayak: Cam eşya veya porselen kapların ısıtma işlemi sırasında üzerine konulduğu metal
ayaktır.
3.5 Spatül: Katı maddelerin aktarılmasında kullanılan metal veya plastik kaşıklardır.
Spatül
Havan
3.6 Havan: Katı maddelerin öğütülmesinde kullanılır.
3.7 Port-tüp: Üzerinde tüplerin çapına uygun delikler bulunan ve deney tüplerini taşımaya yarayan,
metal, tahta veya plastikten yapılmış desteklerdir.
3.8 Baget: Çeşitli amaçlarla sıvıları karıştırmak ve sıvıların ısıtılması sırasında sıçramaları önlemek
için kullanılan ucu yuvarlatılmış cam çubuktur. Kimyasal karışımƖarın hazırlanması sırasında
maddeleri karıştırmak için kullanılan kalın cam çubuk olarak tanımƖanabilir. Süzme işlemi sırasında
kullanılarak iri taneli çökeleklerin tutunmasını ve süzgeç kâğıdının tıkanmasını engeller.
Kristalizasyonda, beherden huniye madde aktarılırken cam baget kullanılır. Katı maddelerin ezilip
sıvıya karışması için kullanılan baget mutlaka cam olmalıdır çünkü metaller asidik sıvıyla
reaksiyona girip paslanabilir.
3.9 Tahta maşa: Sıcak cam eşyaları tutmak veya açık alevde ısıtmak için kullanılır.
3.10 Kıl fırça: Deney tüplerinin temizliğinde kullanılır.
3.11 Desikatör: Az miktardaki ayıraçları veya katı maddeleri kurutmak ve nemden korumak için
kullanılır. Desikatörün alt kısmında nem çekici maddeler (CaCl2 ve MgCl2) bulunur.
3.12 Huni: Çökeltiyi çözeltiden ayırma işleminde kullanılır.
3.13 Ayırma hunisi: Birbiriyle karışmayan (ayrı fazlar oluşturan) sıvıları ayırmak için kullanılan,
armut şeklinde veya silindirik, ağzı kapaklı cam kaplardır.
3.14 Saat camı: Bazı deneylerde ve tartımda kullanılır.
3.15 Lastik puar: Pipetlerin kullanılmasına yardımcı olan küçük yuvarlak pompalardır.
3.16 Vakumlu tüp sistemi: Adaptör, iğne ve özel vakumlu tüpten oluşan bu sistemle damar yoluyla
gereken miktarda ve özellikte kan alınır. Tüpler, örneğe uygulanacak yönteme göre gereken
antikoagülanı içerir ve kullanım kolaylığı için değişik kapak renkleriyle tanımlanır.
4. CİHAZLAR
4.1 Spektrofotometre
Fotometri, çözeltilerin emdiği ışığın şiddetini ölçerek çözeltinin içindeki madde konsantrasyonunu
saptama yöntemidir. Günümüzde bu amaçla spektrofotometre kullanıldığından bu yolla yapılan
tayinlere spektrofotometrik yöntemler adı verilir.
Prensibi: Bir elektromanyetik radyasyon türü olan ışık, dalga veya foton denilen tanecikler halinde
boşlukta yol alır. Işığın dalgalar halinde hareket ederken oluşturduğu iki tepe noktası (pik)
arasındaki uzaklık ışığın dalga boyunu verir. Dalga boyu nanometre (=10-9m) ile ifade edilir ve
lambda () ile gösterilir. Güneş ışığı veya tungsten lambadan çıkan beyaz ışık, farklı dalga
boylarındaki radyasyondan oluşan bir karışımdır. Beyaz ışığı oluşturan farklı dalga boylarındaki tek
ışıklar kümesine spektrum denir. İnsan gözü spektrumun 380-750 nm arasındaki dalga boylarına ait
radyasyonu görebilir (görünür ışık). Daha kısa dalga boyuna sahip olanlar ultraviyole (UV), daha
uzun olanlar infrared (IR) olarak adlandırılır.
UV
Görünür ışık
380
IR
750
Dalga boyu (nm)
4.1.1 Işık spektrumu
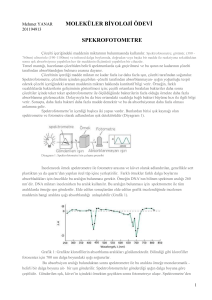
Beyaz ışık renkli bir çözeltiden geçirilirse, ışığın bazı dalga boyları çözelti tarafından seçilerek
emilir. Emilmeden geçen ışıkların bileşkesi çözeltinin görünen rengini oluşturur.
Spektrofotometrede renksiz ve saydam görünen örneklerde ise UV absorbansı ölçülerek
konsantrasyon tayini yapılabilir. Örneğin proteinler, yapılarında bulunan aromatik amino asitlerden
dolayı 260-280 nm.de UV ışığı absorbe eder. Spektrofotometrede 330 nm.den düşük dalga
boylarında ölçüm yapılırken kuartz küvetler kullanılır.
Renkli çözeltilerde görünür ışık alanında absorbans ölçümü yapılır. Renkli bir çözeltiye ışık
girdiğinde belirli bir dalga boyundaki bölümü emilir. Emilen dalga boyu, çözeltinin tam karşıt
rengindeki ışığa aittir. Örneğin sarı renkli çözelti, sarı ışığı geçirir, bunun karşıtı olan mor ışığı
maksimum oranda absorbe eder. Bu nedenle spektrofotometrede absorbans ölçülecek ise, sarı
çözeltiden geçen ışığın rengi mor olacak şekilde, 380-440 nm. dalga boyundaki ışık kullanılır.
Absorbans ölçümü için karşıt renkler Newton Çarkında görülmektedir.
Turuncu
Kırmızı
Sarı
Mor
Yeşil
Mavi
Newton Çarkı
Aşağıdaki tabloda spektrofotometrede belirli bir dalga boyu aralığında görünen ışığın rengi
verilmektedir. Örneğin spektrofotometre, 450 nm. dalga boyuna ayarlandığında deney tübüne gelen
ışık mavi renkte olur.
Işığın dalga boyu (nm)
Spektrum aralığı
<380
380-440
440-500
500-580
580-600
600-620
620-750
> 750
Işığın rengi
-
UV
Görünür
"
"
"
"
"
IR
mor
mavi
yeşil
sarı
turuncu
kırmızı
-
Spektrofotometrelerde görünür ışık kaynağı olarak tungsten lamba, UV kaynağı olarak hidrojen
veya döteryum lambası kullanılır. Basit bir spektrofotometre düzeneği aşağıda görülmektedir.
Monokromatör, tek renkli (monokromatik) ışık seçimini sağlayan bir tür ışık ayırım filtresidir.
Çıkış aralığı, dar bir ışık huzmesi eldesini sağlar. Absorbansı ölçülecek sıvıların konulduğu
küvetler, kuvartz, plastik veya camdan yapılmış, çapı 1 cm olan silindir tüp veya bir kenarı 1 cm
olan dikdörtgen prizma biçiminde haznelerdir. Küvetten çıkan ışık dedektörde elektrik enerjisine
çevrilir. Transmitans veya absorbans, göstergeden okunur.
Spektrofotometrelerde,
çözeltilerin
emdiği
ışık
şiddeti
ölçülür.
Renkli
bir
çözeltiden
monokromatik bir ışık geçirildiğinde giren, çıkan ve emilen ışık şiddetleri çözeltinin
konsantrasyonu ile ilişkilidir. Spektrofotometrede ışığın renkli çözelti tarafından emilen kısmı
absorbans, çözeltiden emilmeden geçen kısmı ise transmitans ölçümleriyle saptanır. Eğer
çözeltinin absorptivitesi yüksekse daha az ışık geçirilir, yani transmitans (geçirgenlik) azalır.
Emilen ışık miktarı (absorbans), monokromatik ışığın çözelti içerisinde kat ettiği yolla ve
maddenin konsantrasyonuyla doğru orantılıdır. Lambert-Beer Yasasının basitçe ifadesi olan bu
kural bütün spektrofotometrik yöntemlerde geçerlidir.
Spektrofotometre şeması
Giren ışığın şiddeti I0 ile gösterilir. Çözeltiden çıkan ışığın şiddeti, giriş şiddetine eşit değildir ve Is
şeklinde gösterilir. Çözeltide renk oluşturan madde, konsantrasyonu ölçülecek maddedir. Bunun
yanında bir de referans (kör=blank) çözelti kullanılır. Kör çözelti içerisinde ölçülecek madde
dışında kalan tüm ayıraçlar bulunur. Bu tübe giren ışık şiddeti I0, çıkan ışık şiddeti Ir’dir. Diğer bir
deyişle kör tübünün ışığı absorbansı, distile suyun ışığı absorbansından daha fazla, deney tübünün
absorbansından daha azdır. Spektrofotometrik tayinlerde absorbansı ölçülecek maddenin bulunduğu
ortama katılan ayıraçlar, ortama katıldıkları miktarda küvete konulup absorbans sıfır ayarı yapılır.
Böylece ayıraçların absorbansa katkıları yok edilmiş (sıfırlanmış) olur. Sıfır ayarı için distile su
kullanılırsa renkli çözeltinin geçirgenliği (transmitans=T) distile suya karşı:
T = Is / I0 (Deneyden çıkan ışık/Giren ışık) olur.
Sıfır ayarı için kör kullanıldığında deneyin transmitansı (T): Deneyden çıkan ışık / Körden çıkan
ışık (Is / Ir) olur. Transmitans değerinin 100 ile çarpımı %T i verir. %T tek renk (monokromatik)
ışığın renkli çözeltiden geçiş oranını belirtir. Renkli çözeltinin emdiği ışık miktarı ise absorbans
terimi ile ifade edilir. Absorbans (A) ile transmitans arasında şu bağıntı vardır:
A= -log T A= -log Is/Ir
Fotometrinin prensiplerini düzenleyen iki temel kanun vardır.
Lambert Kanunu: Monokromatik bir ışık, renkli bir çözeltiden geçerken ışık şddeti katedilen
yolun (b) üstel fonksiyonu olarak azalır. Renkli çözeltinin konsantrasyonu sabit tutulup küvetin çapı
iki katına çıkarılırsa, ışığı absorbe eden çözeltideki molekül sayısı da iki katına çıkar. Bu nedenle
absorbans, katedilen ışık yoluyla doğru orantılıdır.
Beer Kanunu: Çözeltinin absorbe ettiği ışık miktarı (absorbans), çözeltinin konsantrasyonunun bir
fonksiyonudur. Çözeltinin konsantrasyonu arttıkça ışığın şiddeti üstel olarak azalır. Renkli madde
ne kadar çok ışık emerse o ölçüde az ışık geçirir
4.2 Atomik Absorpsiyon Spektrofotometre Cihazı
Atomik Absorbsiyon Spektroskopisi (AAS), gaz halindeki ve temel enerji düzeyinde bulunan
atomların, UV ve görünür bölgedeki ışığı absorblaması ilkesine dayanır. Işıma şiddetindeki azalma
ortamda absorbsiyon yapan elementin derişimi ile doğru orantılıdır. Atomik absorpsiyon
spektroskopisinde metallerin çoğu ile az sayıda ametal analiz edilir. Atomik absorpsiyon
spektroskopisinde element, elementel hale dönüştürüldükten sonra buharlaştırılır ve kaynaktan
gelen ışın demetine maruz bırakılır.
Aynı elementin ışın kaynağından gelen ışınları absorplar. Sulu numune bir alev içine yükseltgen
gaz karışımı ile püskürtülür. AAS’ nin temel çalışma prensibi gaz halindeki atomların ışığı
absorplaması ilkesine dayandığı için hazırlanan çözeltinin gaz halindeki atomlarına dönüştürecek
bir atomlaştırıcıya ihtiyaç duyulmaktadır. Birimimizdeki AAS grafit yakma sistemine sahiptir.
Elektrotermal atomlaştırıcı olarak grafit fırın adı verilen 2-3 cm uzunluğunda 1 cm iç çapındaki tüp
kullanılır. Bu tüpün her iki yanına bağlanmış direnç telleri ile ısıtma yapılır. Fırın elektriksel
dirençle 3000 oC’ ye kadar istenirse kademeli olarak ısıtılabilmektedir. Alevli sistemlere göre daha
pahalı fakat daha avantajlıdır. Özellikle ağır metal elementlerinin analizinde ppb düzeyine kadar
inebildikleri için daha fazla tercih edilmektedir.
Atomik absorbsiyon spektrofotometresi, elementel analizlerde kullanılan önemli bir araçtır.
Örnekteki aranan elementler, o elemente has dalga boyundaki ışığı soğurması yardımıyla
bulunmaktadır. Katot lambada, aranan elementin dalga boyu genelde elementin kendisinin
uyarılması ile elde edildiği için, örnekteki miktarlar için keskin sonuçlar verebilmektedir. Genellikle
metaller için kullanılır.
AAS kimyasal işlem labaratuvar analizlerinde kullanıldığı gibi, günlük hayatta su kirliliği, toprak
kirliliği ve hava kirliliği oluşturan elementlerin limit miktarları doğrultusunda uyumluluk analizleri
için de kullanılmaktadır.
4.3 Otoanalizör
Otoanalizörler, klinik biokimya laboratuarlarında her türlü analiz işlemlerini tam otomatik olarak
bilgisayar kontrolü altında gerçekleştiren cihazlardır. Örnek alma, seyreltme, filtreleme, karıştırma,
ısıtma ve renk belirlenmesi gibi elle yapılan analizlerin vakit alan prosedürlerini otomatikleştirir.
Bütün işlemler mikroişlemcinin kontrolü altında gerçekleştirilir. Otoanalizör, bu prosedürleri,
otomatik olarak, doğru ve hızlı bir şekilde yapar. Analiz hızı saatte 240 test olabilmektedir.
Çoğu örneklerde, belli bir renk gelişimi ve kimyasal bir reaksiyon meydana getirmek için örnekler,
belirteçler, standartlar ile önceden belirlenmiş bir program ile kontrol altında karşılaştırılır.
Sıvının optik yoğunluğunun sıvı konsantrasyonuna bağlı olarak ifade edilmesi bir kolorimetre
içinde fotoelektrik olarak gerçekleştirilebilir. Kolorimetrenin çıkış değerleri hareketli bir grafik
kağıdı üzerinde belirlenecektir. Daha sonra, kaydedilen örneklerin değerleri grafik üzerindeki
bilgiler yardımıyla bilinen standartlar ile karşılaştırılır. Basit bir otoanalizör, plastik tüpler, cam
halkalar ve bağlantı elemanları ile birbirine bağlanmış modül olarak adlandırılan altı üniteden
meydana gelir. Modüllerin sayı ve tipleri, sadece analitik sınırlamalar ile belirlenir. Diğer birtakım
modüllere
ihtiyaç
duyulduğunda
kolayca
otoanalizör
sistemine
eklenebilir.
Otoanalizör ile glikoz, üre, ürik asit, kolestrol, trigliserit, albümin, total protein, billirubin, kreatin,
kalsiyum, fosfor, ast(sgot), alt(sagt), alkalen fosfatoz, CPK, CDH, CGT, amilaz, IgG, IgA, IgM,
transferrin C3C4, klorutr, demir testleri yapılabilir.
Otoanalizör bakımı, diğer çoğu analitik cihazda olduğu gibi, temizlik ve kalibrasyon ağırlıklıdır.
Sistemde su veya deterjanla yıkama yoktur. Reaktifler arası ve numuneler arası kontaminasyonu
önlemek için reaktif ve numune problarının iç ve dış yüzeyleri sürekli olarak invert ve hidrofob bir
sıvı ile kaplanmıştır. Bu cihazlarda elektronik devre arızası pek görülmez. Çoğunlukla mekanik
düzenlerin ayarlarının bozulması, örnek ve diğer sıvıların geçtiği ince kanalların tıkanması, cihaza
yeterli bakım yapılmaması nedeniyle oluşan sorunlar şeklindedir. Otoanalizör sisteminin her
modülünün çalışma prensibi aşağıda özetlenmiştir:
1-Örnekleyici, otoanalizör sistemine belli bir sıralama ile örnekler, standartlar verir ve eriyikler
hazırlar.
2-Pompa, manifold ile birlikte, örnekleri ve belirteçleri, belli oranlarda karıştırmak için kullanılır.
Bu modül, söz konusu sıvıları, sistemin diğer modüllerine gerekli oranlarda verir. Manifold,
pompanın üzerinde yer alır ve pompanın çalışması sırasında çeşitli sıvıları, belli oranlarda karıştırır
ve sisteme doğru iletir.
3-Dializör, karışmış maddeleri örnek materyalinden seçici bir membran yardımıyla ayırır.
4-Isıtıcı, kimyasal reaksiyonu etkilemek için sıvıları devamlı olarak ısıtır. Renk gelişmesi, enzimsel
olaylar,
ısı
ile
yumuşatma
hidroliz
ve
diğer
prosedürler
için
kullanılabilir.
5-Kolorimetre, boru şeklindeki bir akış hücresine doğru akan sıvı akımının optik yoğunluğundaki
değişmeleri belirler. Kolorimetre, optik yoğunlukların değerlerini kaydedici için, eşdeğer gerilim
işaretlerine çevirir. Bir stabilizör ünitesi, kolorimetre lambası için sabit bir gerilim üretir.
6-Kaydedici, kolorimetreden gelen elektriksel işareti, hareketli bir çizelge üzerinde grafiğe çevirir.
4.3 Kromotografi
Kromatografi geçen yüzyılın başında Rus botanikçi Mikhail Tsweet tarafından bulunmuştur.
Tsweet bitki pigmentlerini ayırmak için, çözeltileri kalsiyum karbonat içeren bir kolondan geçirerek
kolorofil ve ksantofilleri ayırmıştır. Ayrılan pigmentler kolonda renkli bantlar şeklinde görüldüğü
için, Yunanca renk anlamına gelen chroma ve yazmak anlamına gelen graphein sözcüklerini
birleştirerek, bu tekniğe kromatografi adını vermiştir.
4
Kromatografi bir ayırma tekniğidir. Örnek içerisindeki bileşenler bireysel olarak ayrılarak kantitatif
olarak belirlenir. Kromatografide ayrılacak bileşenler iki faz (sabit faz ve hareketli faz) arasında
dağılıma uğrar. Bu fazlardan birini geniş bir yüzey alanına yayılmış sabit bir yatak oluştururken,
diğer faz hareketli olup, sabit fazın üzerinden akarak ilerler.Bu iki faz birbiriyle temas halinde olup,
karışmazlar. Bir karışımdaki bileşenlerin her türlü fiziksel ve kimyasal özellikleri ne kadar farklı
olursa, söz konusu karışım o kadar iyi ayrılabilir. Sistemde en az alıkonan bileşen önce taşınır, daha
kuvvetle tutulan bileşen ise daha geç çıkar. Sabit faz katı veya sıvı olabilir. Hareketli faz da gaz
veya sıvı halde bulunabilir.
Kromatografide temel olarak iki ayrım tekniği vardır:
1. Adsorbsiyon kromatografisi
2. Partisyon kromatografisi
Sabit fazın katı olması durumunda adsorbsiyon kromatografisi; sabit fazın bir sıvı olması
durumunda ise partisyon kromatografisi söz konusudur.
4.4.1 Adsorpsiyon kromatografisi:
Adsorpsiyon kromatografisi, çözeltide bulunan maddelerin katı tanecikler üzerinde seçimli
adsorbsiyonuna dayanır. Katı sabit faz yüzeyinde absorbe edilen bileşikler bir süre burada tutulur.
Daha sonra bu maddeler tekrar hareketli faza (sıvı veya gaz) geçerler (desorbsiyon).
4.4.2 Partisyon kromatografisi:
Burada sabit faz, katı bir destek madde üzerine kaplanmış bir sıvıdır; hareketli faz ise sıvı veya gaz
olabilir. Partisyon kromatografisinde maddeler hareketli ve sabit fazlar arasında dağılmaya uğrar.
Nerst yasasına göre;
1.Birbirinde tam çözünmeyen iki sıvı faz ile dengede bulunan çözünmüş bir madde, bu iki faz
arasında sabit bir oranda dağılmaya uğrar. Dağılma oranı ideal durumlarda, çözücü sistemleri hariç,
yalnız sıcaklık ve basınca bağlı olup, genellikle çözünmüş madde konsantrasyonuna bağlı değildir.
2.İki faz içinde çeşitli maddeler çözünmüş ise, bir tür madde, sanki diğer türler yokmuş gibi
dağılmaya uğrar.
4.5 Elektroforez
Cihaz, protein ve enzimlerin ayrılmasında görevlidir. Sistem hacmi, düzgün olarak numunelere jel
dağılımını, ısı, zaman ve reaksiyon oluşumlarını ve de hızlı sonuç almayı kontrol eder. Her numune
kabına numuneler konur, reaksiyon şişesi ve rep jeli yerleştirilir. Bütün bu işlemler 20 dk. İçinde
gerçekleştirilir. 12 adet CK, LD, alkalin, fosfat izoenzimleri, serum proteinler, lipoprotein, HDL
kollesterol, hemoglobin ve CK izoformlarının analizlerini gerçekleştirir.
Elektroforezin çalışma ilkesi;
Molekül ağırlığı ve molekülde bulunun elektrik enerjisinin jel içinde bir yükten diğerine giderken
kattettiği mesafe farklılıklarını ele almaktadır. Elektroforezde kat edilen mesafe, net yük ile doğru;
molekül
büyüklüğü
ve
elektroforetik
ortamın
viskozitesi
ile
ters
orantılıdır.
Elektroforez için dört şeye ihtiyaç vardır:
İyonların hareket edebilegi uygun bir ortam (destek ortamı)
Uygun pH’da bir tampon çözelti
Elektriksel alanı oluşturmak için doğru akım sağlayacak güç kaynağı
Birbirinden
ayrılan
bantları
kantitatif
olarak
değerlendirebilen
dansitometre.
Elektroforetik destek ortamı, elektrot bölmeleri arasına yerleştirilir.
Destek ortam, tamponla doğrudan veya fitiller aracılığı ile ilişkilendirilir. Her iki tampon tankında
elektrot yer alır ve bu elektrotlar güç kaynağına bağlanmak sureti ile devre tamamlanır.
Dansitometri
absorbans
ölçümüdür
ve
destek
ortamdaki
boyanın
absorbansını
ölçer.
Dansitometrenin temel bileşenlerini; ışık kaynağı, monokromatör, tüm plağın taranması için
hareketli bir taşıyıcı, optik sistem ve fotodedektör oluşturur.
Fotodedektörle saptanan sinyaller, numunenin konsantrasyonuyla orantılı olan, destek ortamdaki
boyanın absorbansıyla ilişkilidir. Destek ortam sabit bir hızla ışık demetinden geçilir ve farklı
noktalardan alınan çoklu dansite okumalarının sunduğu bir grafik oluşur.
Elektroforez çeşitleri:
Poliakrilamid jel elektroforez
Agaroz jel elektroforez
Değişken alanlı jel elektroforez
İzoelektrik odaklama
İki boyutlu elektroforez
Kılcal (kapiller)elektroforez
İmmünfiksasyon elektroforez
İmmüno elektroforez
Elektroforez kullanım amacı
Elektroforez, patolojik durumların tamınlanmasında ve takibinde sıklıkla kullanılır. Serumda,
dokuda, hemoglobinde ve idrarda, patolojik durumlar sonucunda ortaya çıkan normal olmayan
proteinlerin varlığını, normal proteinlerin yokluğunu veya tedavi sırasında hastalığın seyrini
izlemek amacıyla kullanılır.
Son yıllarda proteomiks teknolojisinin, en önemli yöntemlerinden biri haline gelmiştir. Bu yöntem
ile protein miktarlarındaki çok küçük değişikliklerin dahi analizi yapılabilmektedir. Böylece,
patolojik durumlarda ortaya çıkan yeni proteinler kolaylıkla tanımlanabilmektedir. Otomatize
edilmiş olması nedeniyle, başta kimya, farmakoloji, biyokimya, toksikoloji, adli tıp bilimlerini
kapsayan çeşitli bilimsel alanlarda pratik ve uygun bir biçimde kullanılmaktadır.
Elektroforez kullanım alanları:
Saflaştırma Saflık kontrolü
Molekül ağırlığı saptama
Kalıtsal ve kalıtsal olmayan hastalık saptama
Enzim izoenzimlerinin saptanması (tanısal amaçlı, populasyon çalışması için, adli tipta)
İmmünolojik ve moleküler biyoloji
Elektroforez Aygıtlarında İki Temel Eşitlik Önem Taşır
1-Ohm yasasına göre elektrik alanı, akım ile direncin çarpımına eşittir. Elektroforez aygıtında
oluşan direncin hemen hemen tamamı jel tarafından oluşturulur. Direnç, akımın geçtiği bölgenin
alanının ve kullanılan tamponun iyonik kuvveti ile ters orantılıdır. Belli bir akım için, jelin
kalınlığının veya tamponun miktarının ve iyonik kuvvetinin azalması direnci arttırır; böylece jel
boyunca oluşan voltaj derecelenmesi ve jele uygulanmış molekülün elektroforetik göç hızı artar.
2-Sistemin ürettiği güç direnç ile akımın karesinin çarpımına eşittir. Üretilen güç ısı şeklinde ortaya
çıkar ve elektoforez aygıtı, jelin sıcaklığını artırmaksızın ancak belli miktarda gücü dağıtabilir. Bu
nedenle voltajın üst sınırı genellikle elektroforez aygıtının ısıyı dağıtma yeteneğine bağlıdır.
Elektroforez tamamlandıktan sonra, destek ortam boya ile Muamele edilerek ayrılmı fraksiyonlarıni
dentifikasyonu
Dansitometri
sağlanır.
absorbans
Boyanmı
ölçümüdür
ve
destek
destek
ortam
ortamdaki
dansitometride
boyanın
absorbansını
okunur.
ölçer.
Dansitometrenin temel bileşenlerini; ışık kaynağı, mono kromatör, tüm plağın taranması için
hareketli bir taşıyıcı, optik sistem ve fotodetektör oluşturur. Fotodetektörle saptanan sinyaller,
numunenin konsantrasyonuyla orantılı olan, destek ortamdaki boyanın absorbansıyla ilişkilidir.
Destek ortam sabit bir hızla ışık demetinden geçirilir ve farklı noktalardan alınan çoklu dansite
okumalarının sunduğu bir grafik oluşur.
Elektroforez cihazında örnek yüklemesi tamamlandıktan sonra aplikatör uçları otomatik olara
yıkama yapar. Aplikatörler, manyetik sistemler tarafından otomatik olarak kontrol edilir. Uygulama
zamanı, sayısı ve türü istenilen şekilde programlanabilir. Farklı deney fazlası arasında, mekanik
kollar otomatik olarak ve manyetik sistemle kontrol edilir.İşem sonucunda jel dansitometre
bölümüne gönderilir, okuması sağlandıktan sonra grafik bilgisayar ekranında görüntülenir.
Tam otomatik elektroforez cihazları ile;
Serum protein elektroforezi
İdrar protein elektroforezi
B1-b2 protein elektroforezi
İmmunofiksasyon elektroforezi
Pentavalent immünofiksasyon
Bence-jones immünofiksasyon
Yüksek çözünürlük protein elektroforezi Testleri yapılabilmektedir.
Hemoglobin elektroforezi
Lipoprotein elektroforezi
LDH izoenzim elektroforezi
Alkali fosfat izoenzin elektroforezi
CK izoenzim elektroforezi
Her test için kullanılan kitler birbirlerinden farklıdır.
KAYNAKLAR
Anonim 2011. Laboratuvar Araç Gereçleri. http://www.fenhane.com/deneyaracgerecleri.pdf.Kimya
Teknolojisi, 53.
Anonim 2014. Tıbbi biyokimya anabilim dalı laboratuvar uygulamaları (tıp fakültesi 1. sınıf
öğrencileri için) http://istanbultip.istanbul.edu.tr/ogrenci/wp-content/uploads.pdf. İstanbul
Üniversitesi Tıp Fakültesi Tıbbi Biyokimya Anabilim Dalı, 55.
Demirtaş, S., Can, M. Ve Güven B. 2014. Tıbbi Laboratuvar El Kitabı. Nobel Tıp Kitapevi, 16.