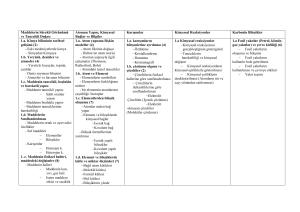
1.1 Kimya:Yirmi birinciYüzyılın Bilimi
Kimya maddenin ve uğradığı değişimlerin
araştırılmasıdır. Temel bir kimya bilgisi biyoloji, fizik,
jeoloji, ekoloji ve pek çok diğer bölüm öğrencileri
için gerekli olduğundan, kimya çoğu kez merkezi bir
bilim olarak adlandırılır. Aslında, kimya yaşam
tarzımızın merkezidir. Kimya olmadan ilkel şartları
yaşayacaktık ve otomobil, elektrik, bilgisayar, CD ya
da her günkü hayatımızı kolaylaştıran diğer pek çok
şey olmayacaktı, hatta yaşamımız daha kısa olacaktı.
Kimya için yazılan Çince karakterler”Değişimin
İncelenmesi”anlamına geliyor.
1.2 Kimyanın Çalışma Alanı
Şekil 1.1 (a) Bir otomatik DNA dizinim cihazından alınan çıktı. Farklı renklerle gösterilen her bir şerit ayrı bir DNA örneği ile elde edilen
dizinimi göstermektedir. (b) Güneş pilleri (c) Bir silisyum devre levhasının işlenişi (d) Soldaki yaprak genetik yapısı değiştirilmemiş olan bir
tütün bitkisinden alınmış olup boynuz solucanlarına maruz kalmıştır. Sağdaki yaprak ise genetiği değiştirilmiş bir tütün bitkisinden alınmış
olup, solucanların saldırısına çok az uğramıştır. Aynı teknik diğer bitki türlerinin yapraklarını korumak amacıyla da uygulanabilir.
Şekil 1.2 Demir (Fe) atomları ve oksijen (O2)
moleküllerinden pas (Fe2O3) oluşumunun basitleştirilmiş
bir moleküler görünümü. İşlem, gerçekte su gerektirir ve pas
su moleküllerini de içerir.
1.3 Bilimsel Yöntem
Sosyal bilimler de dahil olmak üzere, tüm bilim alanlarında, değişimlerin izlenmesinde araştırma için
sistematik bir yaklaşım olan bilimsel yöntem uygulanır.
Şekil 1.3 Kimya ve kimya ile ilgili konuların çalışılması üç aşamalıdır. Gözlem, makroskopik dünyadaki olaylarla ilgilidir, atomlar ve
moleküller mikroskopik dünyayı oluşturur.Temsil, Bir deneyi simgeler ve kimyasal eşitlikler yardımıyla ifade edebilmek için yapılan bir
bilimsel kısaltmadır. Kimyacılar gözlemledikleri bir olayı açıklamak için atom ve moleküllerle ilgili bilgilerini kullanırlar.
1.4 Maddenin Sınıflandırılması
Saf Maddeler ve Karışımlar
Saf madde, belirli veya sabit bir bileşimi olan ve kendine özgü özellikleri ile ayırt edilebilen maddenin bir şeklidir. Örneğin su,
amonyak, sofra şekeri (sakaroz), altın ve oksijen saf maddedir. Saf maddeler bileşim olarak birbirlerinden farklıdır ve
görünüşleri, kokuları, tatları ve diğer özellikleri ile tanınabilirler.
Karışım, her bir saf maddenin kendi özelliğini koruduğu iki ya da daha fazla saf maddenin bir araya gelmesi ile oluşur. Hava,
meşrubat, süt ve çimento aşina olduğumuz bazı örneklerdir. Karışımların sabit bir bileşimi yoktur. Bu nedenle, farklı kentlerden
alınan hava örneklerinin bileşimi, örneğin alındığı yerin yüksekliği, kirliliği vb. farklılıklardan dolayı muhtemelen farklı
olacaktır.
Karışımlar homojen ya da heterojen olabilir. Bir kaşık şeker suda çözüldüğünde, karışımın bileşimi her tarafında
aynı olan bir homojen karışım elde edilir. Diğer taraftan, kum ile demir tozları karıştırılırsa, kum taneleri ile demir tozları
görülebilir halde ayrı ayrı kalırlar (Şekil 1.4). Bu tür karışım, bileşimi her yerinde aynı olmaması nedeniyle heterojen karışım
olarak adlandırılır.
Elementler ve Bileşikler
Saf bir madde element ya da bileşik olabilir. Eğer saf madde kimyasal yöntemlerle daha basit bileşenlerine ayrılamıyorsa,
bu madde bir element’tir. Bu güne kadar 118 element tam olarak tanımlanmıştır.
Şekil 1.4 (a) Karışım, demir tozu ve kum içermektedir. (b) Mıknatıs demir tozlarını
karışımdan ayırır. Aynı teknik, alüminyum, cam ve plastik gibi manyetik özelliği olmayan
maddelerden demir ve çeliğin ayrılması amacıyla büyük ölçekli sistemlere de uygulanabilir.
Örneğin Au, aurum (altın) dan, Fe, ferrum (demir) dan ve Na, natrium (sodyum) dan türetilirken, bazı
simgelerde İngilizce isimlerinden gelmektedir
Bir Bileşik, iki ya da daha çok elementin atomlarının sabit oranlarda kimyasal olarak birleşmesiyle oluşan saf maddedir.
Karışımların aksine, bileşikler sadece kimyasal yollarla kendisini oluşturan saf bileşenlerine ayrılabilirler. Element, bileşik
ve maddenin diğer sınıfları arasındaki ilişkiler Şekil 1.5’de özetlenmiştir.
1.5 Maddenin Üç Hali
Tüm saf maddeler, en azından ilke olarak üç halde bulunabilir; katı, sıvı ve gaz. Şekil 1.6’da görüldüğü gibi,
moleküller arasındaki mesafeler bakımından gazlar, sıvı ve katılardan farklıdır. Bir katıda, moleküller çok az
serbestliğe sahiptir ve düzenli bir şekilde birbirine yakın bulunurlar. Bir sıvıdaki moleküller birbirlerine yakın
ancak sıkı sıkıya bağlı olmadan, uygun konumda bulunurlar ve birbirleri üzerinden akabilirler. Bir gazda
moleküller, büyüklükleri ile karşılaştırıldığında birbirleriyle büyük mesafelerle ayrılmış durumdadır.
Şekil 1.6 Bir katı, bir sıvı ve bir gazın mikroskopik görünümü
Şekil 1.7 Maddenin üç hali. Sıcak bir demirin, buzu
ısıtarak su ve buhara dönüştürmesi
Sıvı haldeki su molekülleri katı haldekine göre daha sıkı istiflenmiştir. Bu durumun, suyun
özelliklerini yaygın olarak bilinen maddeler arasında, benzersiz kıldığına dikkat ediniz.
1.6 Maddenin Fiziksel ve Kimyasal Özellikleri
Saf maddeler bileşimleri ile olduğu kadar kendilerine özgü özellikleri ile de ayırt edilebilirler.
Renk, erime noktası ve kaynama noktası birer fiziksel özelliktir.
Bir fiziksel özellik, maddenin kimliği veya bileşimi değiştirilmeden incelenebilir
ya da ölçülebilir. Örneğin, bir buz kütlesini ısıtıp suya dönüşmesini sağlarken
sıcaklık değişimini kaydetmek suretiyle buzun erime noktasını ölçebiliriz. Su
sadece görünüş olarak buzdan farklıdır ancak bileşim olarak bir farklılık yoktur.
Bu bir fiziksel değişimdir ve su dondurularak tekrar buz haline dönüştürülebilir. Bu
nedenle, bir maddenin erime noktası fiziksel bir özelliktir. Benzer şekilde, helyum gazının
havadan hafif olduğunu söylerken maddelerin fiziksel özelliklerini karşılaştırıyoruz demektir.
Hidrojen havada
yanarak su oluşturur.
Maddenin ölçülebilir bütün özellikleri, kapasite ve şiddet özellikleri denilen gruplardan birisinde yer
alır. Kapasite özelliği’nin ölçülen değeri, söz konusu maddenin ne kadarının dikkate alındığına, yani
miktarına bağlıdır. Kütle, bir saf maddenin söz konusu olan örneğinde bulunan miktarıdır ve bir kapasite
özelliğidir. Daha fazla madde daha fazla kütle demektir.Aynı kapasite özelliği değerleri birbiri ile toplanabilir.
Örneğin, iki tane bakır paranın kütlesi her bir bakır paranın kütleleri toplamıdır. İki tenis kortunun uzunluğu
toplamı, her bir tenis kortunun uzunluklarının toplamı kadardır. Bir küpün hacmi, uzunluğun küpü olarak
tanımlanır ve başka bir kapasite özelliğidir. Kapasite özelliğinin büyüklüğünün sayısal değeri madde miktarına
bağlıdır.
Şiddet özelliği’nin ölçülen değeri, sözkonusu maddenin miktarına bağlı değildir. Bir cismin kütlesinin
hacmine bölümü olarak tarif edilin yoğunluk bir şiddet özelliğidir. Sıcaklık da bir şiddet özelliğidir.
Aynı sıcaklıkta iki tane su dolu beher alalım. Bu iki beherdeki suyu daha büyük bir beher içinde bir araya
getirecek olursak, bir araya getirilmiş suyun sıcaklığı iki ayrı beherdeki suların sıcaklığı ile aynı olur. Kütle,
uzunluk ve hacmin aksine, sıcaklık ve diğer şiddet özellikleri toplanamaz.
1.7 Ölçme
SI Birimleri
Bilim insanları uzun yıllar ölçme sonuçlarını metrik birimlerle, ondalıklarla yani 10’ un kuvvetleri olarak
kaydetmişlerdir. Ancak, 1960 yılında Ağırlık ve Ölçüler Genel Konferansında bir araya gelen, uzmanlar, Uluslararası
Birim Sistemi (Fransızca Système Internationale d’Unites’ den SI olarak kısaltılmıştır) olarak
adlandırılan, yeniden düzenlenmiş SI metrik sistemini önermişlerdir. Çizelge 1.2’de yedi adet temel SI birimi görülmektedir.
Kütle ve Ağırlık
“Kütle” ve “ağırlık” terimleri çoğunlukla birbirinin yerine
kullanılmasına rağmen, aslında, farklı niceliklerdir. Kütle bir cismin
madde miktarının ölçüsüdür, oysa bilimsel olarak ağırlık, bir cisim
üzerine etkiyen yer çekimi kuvvetidir
Kütlenin SI temel birimi kilogramdır (kg). Kilogram, araştırmacılarca her
yerde tekrarlanabilecek doğal işlemlere dayanan uzunluk ve zaman
birimlerinin tersine, belirli bir cisim için tanımlanır (Şekil 1.9). Kimyada,
kilogramın alt birimi olan gram’ın (g) kullanımı daha uygun olmaktadır.
1 kg = 1000 g = 1 x 103 g
Sıcaklık Eşelleri
SI birim sisteminde sıcaklığın temel birimi Kelvin olup bu eşel mutlak sıcaklık eşelidir. Bu eşele mutlak denilmesinin nedeni, Kelvin
eşelinin 0 K olarak belirtilen başlangıç noktasının, kuramsal olarak ulaşılabilen en düşük sıcaklık değeri olmasıdır.
? F
9F
x(C) + 32F
5F
? K (C+273,15C)
1K
1C
Şekil 1.11 Üç sıcaklık eşelinin karşılaştırılması:
Celsius, Fahrenheit ve mutlak (Kelvin) sıcaklık eşelleri.
Görüldüğü gibi, suyun donma ve kaynama noktaları
arasında, Celsius eşelinde 100 bölme ya da 100 derece
varken aynı sıcaklık değerleri arasında Fahrenheit
eşelinde 180 bölme ya da 180 derece bulunmaktadır.
Celsius eşeli önceleri santigrat eşeli olarak da
adlandırılırdı.
Örneğin, 74,6 x100 (n = 0) sayısı 74,6’ya eşittir. İkincisi, pratikte n = 1 olduğu zaman, bunun yazılması
ihmal edilir. Buna göre 74,6 için bilimsel gösterim 7,46 x 10 şeklindedir, 7,46 x 101 değildir.
Doğruluk ve Kesinlik
Ölçmeler ve anlamlı sayılar tartışılırken, doğruluk ve kesinlik kavramlarını
birbirinden ayırmak gerekir. Doğruluk, bir ölçüm sonucunun ölçülen büyüklüğün
gerçek değerine ne kadar yakın olduğunu belirtir. Bir bilim insanı için doğruluk ile
kesinlik arasında fark vardır.
Kesinlik, aynı büyüklüğe ait, biri diğeriyle uyum içinde olan iki ya da daha çok
sayıdaki ölçme sonucunun birbirlerine ne kadar yakın olduğunu ifade eder (Şekil
1.13).
1.9 Problem Çözümünde Boyut Analizi
Boyut analizi, Einstein’a da meşhur
kütle-enerji formülü E=mc2nin
çözümünde yol göstermiş olabilir.
Dünyadaki Gerçek Problemlerin Çözümü: Bilgi, Varsayımlar ve Basitleştirmeler