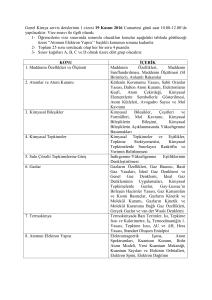
Kuantum Teorisi ve Atomların
Elektronik Yapısı
Kaynak: Fen ve Mühendislik Bilimleri için
KİMYA
Raymond CHANG
1
Dalganın Özellikleri
Dalgaboyu (l) bir dalganın ardışık iki eş noktası
arasındaki mesafedir.
Genlik dalganın tepe noktasının dalganın orta noktasına
olan dikey mesafesidir.
Frekans (n) sabit bir noktadan 1 sn de geçen dalga sayısıdır.
(Hz = 1 çevrim/s).
Dalganın Hızı (u) = l x n
2
Maxwell (1873), görünür ışığın elektromagnetik
dalgalardan oluştuğunu ileri sürmüştür.
Elektromagnetik
radyasyon enerjinin
elektromagnetik dalgalar
halinde taşınımıdır.
Işığın (vakumdaki) hızı (c) = 3.00 x 108 m/s
Tüm elektromagnetik radyasyon için
lxn=c
1nm=1x10-9 m
3
4
Bir fotonun frekansı 6.0 x 104 Hz dir. Dalgaboyunu (λ) kaç nm
dir. Bu frekans görünür bölgede midir ?
lxn=c
l = c/n
l = 3.00 x 108 m/s / 6.0 x 104 Hz
l = 5.0 x 103 m
l = 5.0 x 1012 nm
5
Gizem #1, “Isıtılan Katılar Problemi”
Planck tarafından 1900 de çözüldü
Katılar ısıtıldığında geniş bir dalgaboyu
aralığında elektromagnetik radyasyon yayar.
Belirli bir sıcaklıktaki bir cisimden yayılan radyant enerji
dalgaboyuna bağlıdır.
Enerji (ışın) kesikli birimler
halinde (kuantum)
yayılır veya absorplanır.
E=hxn
Planck sabiti (h)
h = 6.63 x 10-34 J•s
6
Bakır yüksek enerjili elektronlar ile bombardıman edildiğinde X
ışınları yayılır. X ışınlarının dalgaboyu 0,154 nm ise enerjiyi
joule cinsinden hesaplayınız.
E=hxn
E=hxc/l
E = 6.63 x 10-34 (J•s) x 3.00 x 10 8 (m/s) / 0.154 x 10-9 (m)
E = 1.29 x 10 -15 J
7
Schrodinger Dalga Denklemi
1926 da Schrodinger elektronun hem dalga hem parçacık
karakterini tanımlayan bir denklem geliştirdi.
Dalga Fonksiyonu (y) :
1. Y ile elektronun enerjisi ve
2. e- nun uzayda nerede olabileceğinin olasılığını verilir.
Schrodinger denklemi yalnızca hidrojen atomu için tam
olarak çözülebilir. Çok elektronlu sistemlerde ise en olası
çözümü verir.
8
Schrodinger Dalga Denklemi
y kuantum sayıları denen 4 sayının bir fonksiyonudur.
kuantum sayıları (n, l, ml, ms)
Baş kuantum sayısı n
n = 1, 2, 3, 4, ….
e- un çekirdeğe olan uzaklığını ifade eder.
n=1
n=2
n=3
9
e- yoğunluğunun % 90 ı
1s orbital
10
Schrodinger Dalga Denklemi
kuantum sayıları: (n, l, ml, ms)
açısal momentum kuantum sayısı l
Verilen bir n değeri için , l = 0, 1, 2, 3, … n-1
n = 1, l = 0
n = 2, l = 0 veya 1
n = 3, l = 0, 1, veya 2
l=0
l=1
l=2
l=3
s orbital
p orbital
d orbital
f orbital
e- nun kapladığı “hacmin” şeklini gösterir
11
l = 0 (s orbitalleri)
l = 1 (p orbitalleri)
12
l = 2 (d orbitalleri)
13
Schrodinger Dalga Denklemi
kuantum sayıları: (n, l, ml, ms)
Manyetik kuantum sayısı ml
l nin verilen bir değeri için
ml = -l, …., 0, …. +l
Eğer l = 1 (p orbital) ise , ml = -1, 0, veya1
Eğer l = 2 (d orbital), ml = -2, -1, 0, 1, veya 2
Orbitallerin uzaydaki yönelimi
14
ml = -1, 0, veya 1
Uzaydaki 3 farklı yönelim
15
ml = -2, -1, 0, 1, veya 2
Uzaydaki 5 farklı yönelim
16
Schrodinger Dalga Denklemi
(n, l, ml, ms)
spin kuantum sayısı ms
ms = +½ veya -½
ms = +½
ms = -½
17
18
n=2 ise kaç tane p orbitali vardır ?
n=2
Eğer l = 1, ise ml = -1, 0, veya +1
2p
3 orbital
l=1
3d alt kabuğunda kaç orbital bulunur?
n=3
3d
l=2
Eğer l = 2, ise ml = -2, -1, 0, +1, veya +2
5 adet d orbitai ve toplam 10 e- bulunur.
19
Schrodinger Dalga Denklemi
kuantum sayıları: (n, l, ml, ms)
Atomdaki elektronun bulunabileceği enerji seviyeleri onun
kendisine özgü Dalga fonksiyonu (Ψ) ile tanımlanır
Pauli dışarlama prensibi – bir atomdaki iki elektron aynı
dört kuantum sayısını alamaz.
Wolfgang Ernst Pauli
20
Schrodinger Dalga Denklemi
Kuantum sayıları: (n, l, ml, ms)
Yörünge – elektronlar aynı n değerini alır.
Alt yörünge – aynı n ve l değerini alan elektronlar bulunur.
Orbital – elektronlar aynı n, l, ve ml değerlerini, alır.
Bir orbital kaç elektron barındırır ?
Eğer n, l, ve ml ise o zaman ms = ½ or - ½
y = (n, l, ml, ½) veya y = (n, l, ml, -½)
Bir orbital 2 elektron bulundurur.
21
HUND KURALI
Elektronların bir alt kabuktaki en kararlı dağılımı, en fazla
paralele spinin bulunduğu haldir.
AUFBAU PRENSİBİ
Elektronlar orbitalleri en düşük enerjili olandan başlayarak
doldururlar.
22
Çok elektronlu bir atomda orbitallerin doldurulması
1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s
23
Elektron konfigurasyonu elektronların değişik orbitallere
nasıl dağıldığını gösterir.
Alt kabuk yada orbitaldeki
elekronların sayısı
1s1
Baş kuantum sayısı, n
açısal momentum
kuantum sayısı l
Orbital diagramı
H
1s1
24
Mg un elektron konfigürasyonu nedir ?
Mg 12 elektron
1s < 2s < 2p < 3s < 3p < 4s
1s22s22p63s2
2 + 2 + 6 + 2 = 12 electron
3.periyot 2A grubu
[Ne] 1s22s22p6
Kısaca [Ne]3s2
Cl un en dış elektronunun muhtemel 4 kuantum sayısını
yazınız.
Cl 17 elektron
1s < 2s < 2p < 3s < 3p < 4s
1s22s22p63s23p5
2 + 2 + 6 + 2 + 5 = 17 elektron
En dış (son) elektron 3p orbitalinde bulunur.
n=3
l=1
ml = -1, 0, +1
ms = ½ , -½
25
Periyodik cetvelde elementlerin, elektronlar tarafından
doldurulan kabuklarına göre sınıflandırılması
26
27
DİYAMANYETİZM VE PARAMANYETİZM
Atom, iyon veya molekül halinde bulunan maddelerin
manyetik özellikleri elektronik biçimlenmeleri ile ilgilidir.
Diyamanyetik maddelerin elektronlarının hepsi çiftleşmiş
halde bulunur. Bundan dolayı manyetik alan tarafından
hafifçe itilirler. Paramanyetik maddeler bir veya birden
fazla çiftleşmemiş elektrona sahiptir ve manyetik alan içine
çekilirler.
28
Paramanyetik
çiftleşmemiş elektronlar
2p
Diamanyetik
Tüm elektronlar çift
2p
29