1
1. PERİYODİK SİSTEMİN TARİHÇESİ
Alman Lother Mayer ve Rus Dimitri Mendeleev,
Avogadro'nun makalesinin kopyasını alarak memleketlerine
dönmüşlerdi. 1869 yılında Mayer ve Mendeleev birbirinden
habersiz olarak elementlerin artan atom kütlelerine göre
sıralanması halinde düzenli olarak tekrarlanan özelliklerin
gözlenebildiğini keşfettiler. Mendeleev bu gözlemlere peri
yodik kanun adını verdi.
Argonun bağıl kütlesi 40 idi ve kalsiyumun aynısı idi.
Fakat argon bir asal gaz, kalsiyum ise aktif bir metaldi. Böyle
beklenmeyen durumlar, araştırmacılarda, bağıl atom
kütlelerinin elementlerin düzenlenmesinde temel olarak
alınmasında şüpheler uyandırdı.
2
1. PERİYODİK SİSTEMİN TARİHÇESİ
Mendeleev'in hazırladığı periyodik cetvel kimya
literatürüne elementlerin aileleri (grup) kavramını
kazandırmıştı.
Mendeleev'in periyodik cetvelindeki tutarsızlıklar,
gözlenen periyodikliğin temelinde, atom kütlesinden daha
başka bazı temel özelliklerin, alabileceği düşüncesini akıllara
getirmiştir. Bu özelliğin, atom numarası ile bağlantılı
olabileceği de düşünülmekteydi.
3
2. MODERN PERİYODİK SİSTEM
α saçılma deneylerinde elde edilen verileri kullanan
Rutherford, bir kaç elementin çekirdeğindeki pozitif yükün
miktarını tahmin edebilmişti. Ancak 1913'e kadar atom
numaralarının tayini için genel bir yöntem yoktu. 1913 yılında
genç bir fizikçi olan Henry Moseley yüksek enerjili
elektronlarla bombardıman edilen elementlerin ürettiği X
ışınlarının frekansları ile atom numaraları arasında, bir ilişki
olduğunu keşfetti. Birkaç istisna dışında Moseley, atom
numaralarının artış sırasının, atom kütlesinin artış sırası ile
aynı olduğunu buldu. Örneğin, kalsiyumun atom kütlesinin
artış sırasına göre, yirminci elementtir ve atom numarası da
yirmidir.
4
2. MODERN PERİYODİK SİSTEM
Bu çalışmalarıyla Moseley, elementlerin kimyasal
davranışlarının atom ağırlıklarına değil atom numaralarına
göre sıralanması gerektiğini göstermiştir. Bugünkü modern
periyodik çizelge atom numaralarını esas almaktadır. Modern
bir periyodik çizelge, genellikle element simgesiyle atom
numarasını birlikle gösterir. Elementlerin elektron dağılımları,
fiziksel ve kimyasal özelliklerdeki tekrarların açıklanmasına
yardımcı olur.
Periyodik çizelge bir grubun veya bir periyodun içinde
yer alan elementlerin genel özelliklerini ve kimyasal
eğilimlerini anlamamıza, her hangi bir elementin özelliklerini
oldukça doğru bir şekilde tahmin edebilmemize yardımcı olur.
5
2. MODERN PERİYODİK SİSTEM
Elementleri özelliklerinden benzerliklerine göre
sınıflandıran çizelgeye periyodik cetvel veya periyodik tablo
denir. Periyodik cetvel, periyot ve gruplardan oluşur.
Periyodik cetvelin yatay sıralarına periyot denir.
Periyotlar enerji seviyelerini temsil eder. Temel elektron
dizilişinde elektron içeren enerji seviyeleri eşit olan elementler
atom numaralarının artışına göre sıralanarak periyotlar
oluşturulmuştur.
Periyodik cetvelin düşey sütunlarına grup denir.
Gruplar değerlik elektron sayısını temsil eder. A ve B olmak
üzere iki tür grup bulunmaktadır.
6
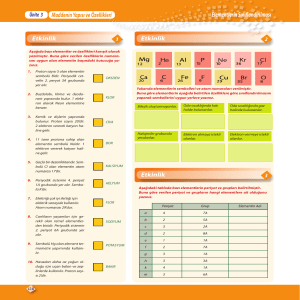
2. MODERN PERİYODİK SİSTEM
Periyodik cetvel periyotlar ve gruplar dışında dört ana
bloğa ayrılmıştır.
Bunlar s, p, d ve f bloklarıdır.
Temel Elektron dizilişleri
s ile biten elementler s bloğunda (He hariç),
p ile bitenler p bloğunda,
d ile bitenler d bloğunda ve
f ile bitenler f bloğunda yer alır.
7
8
2. MODERN PERİYODİK SİSTEM
s ve p bloklarındaki elementler A gruplarını,
d ve f bloklarındaki elementler ise B gruplarını oluşturur.
Periyot ve grupların bulunmasında başkuantum
sayısı, değerlik orbitaller ve değerlik elektron sayısı
kullanılır.
***Temel elektron dizilişinde
*başkuantum sayısı (en yüksek enerji seviyesi olup en son s
orbitalinin katsayısıdır) periyot numarasını,
*değerlik orbitaller grubun türünü,
*değerlik elektron sayısı ise grubun numarasını verir.
9
10
11
12
13
3. ELEKTRON DİZİLİMİ, PERİYOT, GRUP VE BLOK
a) Periyotlar
En yüksek enerji düzeyleri eşit olan elementlerin atom
numaralarındaki artışa göre, soldan sağa doğru sıralanmasıyla
elde edilen satırlardır.
Bir elementin değerlik elektronlarının bulunduğu enerji düzeyini
gösterir. Bundan dolayı 7 tanedir. Yukarıdan aşağıya
numaralanır. Periyotların numarası “n” ile gösterilir. “n” baş
kuantum sayısıdır.
Birinci periyot hariç, her periyot bir metalle başlar.
Yedinci periyot hariç, her periyot bir soygaz ile biter.
14
3. ELEKTRON DİZİLİMİ, PERİYOT, GRUP VE BLOK
b) Gruplar
Gruplar değerlik orbitallerin türünü ve değerlik elektron sayısını
temsil eder. Bir gruptaki elementlerin kimyasal özellikleri
birbirine benzer. Bu ilkeye 1H elementi uymaz. 1A grubu
elementlerine alkali (bazik) metaller denir. Bu elementlerin
özellikleri birbirine benzer. Ancak H elementi metal değildir ve
özellikleri gruptaki elementlerin özelliklerine benzemez. Periyo
dik tablonun gruplarının ve bloklarının ortak özelliklerinden
kaynaklanan özel adları vardır.
15
3. ELEKTRON DİZİLİMİ, PERİYOT, GRUP VE BLOK
* B gruplarına dahil olan f bloğundaki elementlere ise iç
geçiş elementleri denir.
16
3. ELEKTRON DİZİLİMİ, PERİYOT, GRUP VE BLOK
c) Bloklar
Bir element atomunun değerlik katmanındaki elektron dizilimi,
o elementin periyodik sistemdeki yerini belirler.
Kesin olarak helyum s bloğuna aittir, fakat p bloğunda göste
rilmiştir. Helyum, 2A gruptaki metallerden ziyade 8A gruptaki
(18. grup) asal gazların özelliklerini gösteren bir gazdır. 8A
grubunun diğer elementlerinde olduğu gibi helyum da dolu bir
değerlik katmanına sahip olduğundan onun yeri 8A grubudur.
Hidrojen, periyodik sistemde, ayrıcalıklı bir yerde
bulunmaktadır. Bir tane s - elektronu olduğundan birinci grup
(1A grup) tadır.
Hidrojen aynı zamanda asal gazlardan bir eksik elektrona sahip
olduğundan 7A grubu (17. grup) üyesi gibi davranabilir.
17
3. ELEKTRON DİZİLİMİ, PERİYOT, GRUP VE BLOK
s ve p blokları, ana grupları oluştururlar. Aynı ana grupta
bulunan elementlerin atomlarının değerlik katmanındaki
elektron dağılımı aynı olup yalnız baş kuantum sayıları farklıdır.
Bir temel grupla atomların özelliklerinin büyük ölçüde benzer
olmasının nedeni;
aynı dış enerji seviyesinde bulunan elektron sayısının ve
dağılımının benzerliğidir. Grup numarası, değerlik elektron
sayısını verir.
18
3. ELEKTRON DİZİLİMİ, PERİYOT, GRUP VE BLOK
Altıncı periyotta 32 element bulunur. Bu periyotta 57'den 71'e
kadar olan elementlere lantanitler veya nadir toprak elementleri
denir. Bu periyotta 6s, 4f, 5d ve 6p orbitallerine elektron
girdiğinden, toplam 32 elektronun girebileceği yer vardır.
Lantanitler genellikle benzer kimyasal özellikler gösterirler.
7. periyottaki f-blok elementlerinin de kimyasal özellikleri
birbirine benzer. 89'dan 103'e kadar olan elementlere aktinitler
denir.
Bunların hepsi radyoaktif element olup, çok benzer özelliklere
sahiptirler.
19
3. ELEKTRON DİZİLİMİ, PERİYOT, GRUP VE BLOK
20
3. ELEKTRON DİZİLİMİ, PERİYOT, GRUP VE BLOK
21
3. ELEKTRON DİZİLİMİ, PERİYOT, GRUP VE BLOK
22
3. ELEKTRON DİZİLİMİ, PERİYOT, GRUP VE BLOK
23
3. ELEKTRON DİZİLİMİ, PERİYOT, GRUP VE BLOK
24
25
26
27
28
29
30
31
32
33
34
35
36
37
38
39
40
41
42
43
44
45
46
47
48
49
50
51
52
53
54