Ratlarda Siklofosfamitle
Oluşturulmuş Hemorajik Sistit Modeli
Ercan Malkoç, Turgut Topal
Giriş
Siklofosfamid, solid tümörlerin tedavisinde yaygın olarak kullanılmasının yanında
lenfoma, miyeloma, kronik lenfositik lösemi ve Waldenstrom makroglobulinemisi gibi
B-hücre malignitelerinde de kullanılmaktadır. Ayrıca siklofosfamid ve sentetik analoğu olan ifosfamidin trombositopenik purpura, romatoid artrit, sistemik lupus eritematozis, nefritik sendrom ve Wegener granulomatozisi gibi nonneoplastik hastalıkların tedavisinde de kullanılmaktadır.
Siklofosfamidin ilk yan etkileri 1960 yılında rapor edilmiştir[1]. Ürolojik yan etkileri
irritatif işeme yakınmalarından, hayatı tehdit eden hemorajik sistite kadar değişkenlik göstermektedir. Siklofosfamid tedavisinden sonra %68 oranlarına varan hemorajik sistit ve kontrol edilemeyen kanama nedeniyle %4 oranında mortalite rapor edilmiştir [2]. Hemorajik sistit siklofosfamidin en önemli potansiyel toksisitesi ve doz sınırlayan yan etkisidir.
Fizyopatoloji
Siklofosfamid karaciğerde hidroksillenerek bir metaboliti olan akroleine dönüşmektedir ve akroleinin böbrekten atılmasıyla yan etkiler ortaya çıkmaktadır. Akrolein sadece siklofosfamidin yıkılmasıyla oluşmamakta ayrıca sigarada, böcek ilaçlarında,
bazı yiyeceklerde ve yanmış organik malzemelerde de bulunabilmektedir. Akroleinin
ürotelyumla direk temasıyla üroteliyal hasar başlamaktadır [3]. Mesanede vasküler
konjesyon, ödem, hemoraji, epiteliyal nekroz ve inflamatuar infiltrasyon ile karakterize ağır bir sistit tablosu görülmektedir. Mesanenin ağırlığı da büyük oranda ödem
nedeniyle artmaktadır [4]. Mesane ağırlığı siklofosfamid uygulandıktan 2 saat sonra anlamlı derecede artmaya başlamakta ve 4-72 saatte en yüksek seviyelere çıkmaktadır [5].
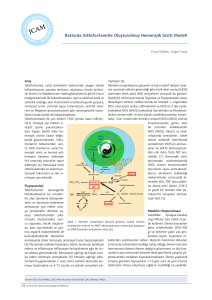
Akrolein üroepitelyumu geçerek ve bazı reaktif oksijen türlerini uyararak etkisini gösterdiği gibi nitrik oksit sentaz [NOS] üzerinden nitrik oksit [NO] seviyelerini artırarak da gösterir [Şekil] [6]. NO birçok önemli fizyolojik ve fizyopatolojik süreci düzen362 DERMAN MEDICAL PUBLISHING
1
Ratlarda Siklofosfamitle Oluşturulmuş Hemorajik Sistit Modeli
leyen serbest radikal öncülü bir üründür.
L-argininden NOS vasıtasıyla sentez edilmektedir ve NOS’un 3 tipi vardır. Endotelial NOS [eNOS] endotelial hücrelerden ve
fibroblastlardan sentez edilir ve ana olarak vazodilatasyondan sorumludur. Sinir
sisteminde üretilen nöronal NOS [nNOS]
sinirsel sinyalizasyonda görev alan bir
enzimdir. İndüklenebilir NOS [iNOS], lökosit ve makrofajlarda sentezlenir. Genel
olarak patolojik durumlarda sentezlenen
iNOS’un aktivasyonu ile eNOS aktivasyonundan çok daha fazla NO üretilebilir [7].
Hemorajik sistit durumunda subüretelyumda iNOS üreten immünoreaktif hücrelerin sayısı artmaktadır. Ayrıca akroleinin tetiklediği mekanizmalar sonucunda interlokin alfa, TNF beta, platelet aktive edici faktör, COX-2 ve güçlü bir oksidan olan peroksinitrit seviyeleri artmaktadır [8,9,10].
Şekil 1. Akrolein üroepitelyal hücreye girmesi, reaktif
oksijen türevlerinin üretimi ve iNOS aktivasyonunun
artmasıyla başlayan ve DNA hasarıyla sonuçlanan süreç
[6].
Modelin Oluşturulması
Genellikle Sprague-Dawley veya Wistar türü erkek sıçanlar kullanılır. Deney hayvanları genç erişkinlerden [200-300 g] ve birbirine yakın yaş grubundan seçilir. Sıçanların erkeklerden seçilmesinin nedeni, dişilerin menstrüel siklusları esnasında antioksidan özelliğe sahip olduğu bilinen östrojen hormonunun dönem dönem değişim göstermesi ve dişi hayvanların aynı menstrüel döneme denk getirilerek çalışma yapılmasındaki zorluktan kaynaklanmaktadır. Deney yapılacak ortama getirilen hayvanların
7-10 gün süre ile yeni ortama aklimatize olması [alışması] sağlanır. İçebildiği ve yiyebildiği kadar normal musluk suyu ve sıçan yemi ile beslenir. Özel bir çalışma yapılmıyorsa genel olarak ortamın ışıklanması 12 saat gündüz-12 saat gece şeklinde beyaz ışık altında sağlanır. Yaşam alanı sakin ve stressiz bir ortam olmalıdır.
Tek doz 100-200 mg/kg siklofosfamid, 500-1500 μl. serum fizyolojik içerisinde gidecek şekilde intraperitoneal olarak uygulanır. Yapılacak çalışmanın tipine göre ilk siklofosfamid uygulamasında 24-72 saatler arasında hayvanlar sakrifiye edilerek çalışma sonlandırılabilir. Genel olarak hemorajik sistit belirtileri 24-48 saat aralığında en
yüksek düzeye ulaşır, 72 saat sonrasında da sonlanır. Hayvanın hemorajik sistitinin
varlığı ve ağırlığının takibi idrar stiği [en pratik yoldur, başka yollar da kullanılabilir]
ile hematürinin tespiti ve takibi ile ortaya konur. Bu amaçla siklofosfamid verildikten
sonra 12 saatte bir karın masajı ile elde edilen idrar değerlendirilir. Bunun yanında
sık idrara çıkma, proteinüri de gözlenebilir. Ayrıca bu süre içerisinde tablonun ağırlığına göre hayvan kilo kaybedebilir.
Çalışma sonlandırılacağında ilk olarak anestezi [örneğin 85 mg/kg ketamine HCl ve
12.5 mg/kg xylazine HCl karışımı intraperitoneal veya intramusküler olarak kullanılabilir] yapılmalıdır. Hemorajik sistit tablosunun ağırlığının veya yapılan tedavinin et2
DERMAN MEDICAL PUBLISHING 363
Ratlarda Siklofosfamitle Oluşturulmuş Hemorajik Sistit Modeli
Ratlarda Siklofosfamitle Oluşturulmuş Hemorajik Sistit Modeli
kinliğinin değerlendirilmesinde ise cerrahi olarak çıkarılan mesanenin ağırlığının tespiti [ödem değerlendirmesi] ve %7-10’luk formole alınan örneklerde histopatolojik
olarak mesane kesitlerinde hemoraji, inflamasyon, ödem, nekroz’un değerlendirilerek skorlanması kullanılır. Bunun haricinde çeşitli biyokimyasal analizler, ependorflara konan mesane parçaları sıvı nitrojende dondurulup, - 80oC derin dondurucuya kaldırılarak zamanı gelince yapılabilir. Ayrıca mesanede, histopatolojik veya biyokimyasal örnekleme yapılmadan önce de in vitro analizler de [organ banyosu vb] yapılabilir.
Deneysel çalışmalarda “patolojik kontrol grubu” olarak nitelendirebileceğimiz sadece siklofosfamidin uygulandığı grupta, genellikle histopatolojik olarak yüksek düzeyde hemoraji, inflamasyon, ödem; daha düşük düzeyde olmak üzere nekroz ortaya çıkar. Bu durumun histopatolojik olarak ortaya konması, aynı zamanda modelin de
oturduğunun veya düzgün uygulandığının bir göstergesidir. Bu bulguların çeşitli tedavi ajanları ile azaltılması ise o tedavi ajanının etkinliğinin bir göstergesi olarak nitelendirilebilir.
Kaynaklar
1. Coggins PR, Ravdin RG, Eisman SH. Clinical evaluation of a new alkylating agent: cytoxan (cyclophosphamide). Cancer. 1960;13:1254–60.
2. Gray KJ, Engelmann UH, Johnson EH, Fishman IJ. Evaluation of misoprostol cytoprotection of the bladder with cyclophosphamide (cytoxan) therapy. J Urol. 1986;136:497–500.
3. Masuda H, Chancellor MB, Kihara K and Yoshimura N: 15-deoxy-Delta12,14-prostaglandin J2 attenuates development
of cyclophosphamide-induced cystitis in rats. Urology 2006; 67: 435.
4. Ribeiro RA, Freitas HC, Campos MC, Santos CC, Figueiredo FC, Brito GA et al: Tumor necrosis factor-_ and interleukin-1_ mediate the production of nitric oxide involved in the pathogenesis of ifosphamide induced hemorrhagic cystitis in mice. J Urol 2002; 167: 229.
5. Matsuoka Y, Masuda H, Yokoyama M, Kihara K. Protective effects of heme oxygenase-1 against cyclophosphamideinduced haemorrhagic cystitis in rats. BJU Int 2007; 100: 1402–8.
6. Korkmaz A, Topal T, Oter S. Pathophysiological aspects of cyclophosphamide and ifosfamide induced hemorrhagic cystitis; implication of reactive oxygen and nitrogen species as well as PARP activation. Cell Biol Toxicol Sep
2007;23(5):303-12.
7. Szabo C.: The pathophysiological role of peroxynitrite in shock, inflammation, and ischemia-reperfusion injury. Shock,
6: 79, 1996.
8. Kiuchi H, Takao T, Yamamoto K. Sesquiterpene Lactone Parthenolide Ameliorates Bladder Inflammation and Bladder
Overactivity in Cyclophosphamide Induced Rat Cystitis Model by Inhibiting Nuclear Factor-kappa B Phosphorylation. The
Journal of Urology. May 2009. Vol. 181, 2339-2348.
9. Souza-Filho MV, Lima MV, Pompeu MM, Ballejo G, Cunha FQ, Ribeiro Rde A.: Involvement of nitric oxide in the pathogenesis of cyclophosphamide-induced hemorrhagic cystitis. Am J Pathol, 150: 247, 1997.
10. Korkmaz A, Oter S, Sadir S, Coskun O, Topal T, Ozler M, Bilgic H. Peroxynitrite may be involved in bladder damage caused by cyclophosphamide in rats. J Urol 173:1793–1796, 2005.
364 DERMAN MEDICAL PUBLISHING
3