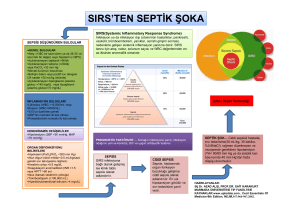
NEONATAL SEPSİS
Yrd. Doç. Dr. Duran Karabel
Tanım
Yaşamın ilk ayında bakteriyeminin eşlik ettiği sistemik bulgularla seyreden bir klinik
sendromdur.
Etiyolojik ajanların çoğunu bakteriler ve kandida oluşturur. Bunun yanında viruslar ve nadiren
de protozoonlar septisemi oluşturabilirler.
Epidemiyoloji
Gelişmiş ülkelerde sepsis sıklığı için canlı doğanlarda 1-8 /1000 oranı bildirilmesine rağmen
gelişmekte olan ülkelerde bu oran daha yüksektir. Neonatal septiseminin insidansı
gestasyonel yaşla ters orantılıdır. Çok düşük doğum ağırlıklı bebeklerde (ağırlık<1500 gr)
sepsis oranı 1-2/100’e kadar çıkabilmektedir.
Risk Faktörleri
1) EMR (Erken membran rüptürü): Amnion kesesinin açıldıktan sonra 24 saat içinde doğum
gerçekleşmemesi neonatal sepsis riskini arttırır.
2) Prematürite: Bebeğin gestasyon yaşı ne kadar küçükse risk o kadar artar.
3) Maternal ateş ve korioamnionitis
4) Perinatal asfiksi: Bebeğin anoksi ve iskemiye maruz kalması savunma sisteminde
yetersizliğe yol açmaktadır.
Risk Faktörleri
5) Erkek bebek: Nedeni tam anlaşılamamakla birlikte erkek bebekler kızlardan 2-6 kez daha
yüksek enfeksiyon riski taşımaktadır.
6) Gebeliğin son döneminde anne vajeninde grup-B streptokok (GBS), Herpes vs
kolonizasyonu olması.
7) Çoğul gebelik: Özellikle bebeklerden biri enfekte ise risk çok artar.
8) Konjenital anomaliler (Meningomyelosel, aspleni, üriner anomaliler).
Risk Faktörleri
9) Yenidoğan immun sisteminin immatür olması:
A) Defektif granülosit fonksiyonu
a.Anormal kemotaksis
b.Anormal fagositoz
c. Azalmış bakterisidal aktivite
B) Anormal serum opsonik aktivite
a. Spesifık antikorların düşük konsantrasyonda olması
b. Komplemanın ve/veya nonspesifık opsoninlerin düşük
konsantrasyonda olması
C) Klasik (Cıq, C3, C5) ve properdin kompleman yolundaki eksiklikler
Risk Faktörleri
10) Çevresel faktörler: Normalde bebek intrauterin ortamda steril amniyotik sıvı içindedir.
İntrauterin kolonizasyon ve kontaminasyonun esas mekanizmalarından biri asendan
enfeksiyondur. Transplasental geçiş daha seyrek olarak meydana gelir. Sezaryen dışında,
vajinal yolla doğan tüm bebekler doğarken vajinal flora ile kontamine olur. Üç gün içerisinde
anterior burun delikleri, boğaz ve deri gram pozitif mikroorganizmalar ile enfekte olur (Alfa
hemolitik streptokoklar, S.aureus, S.epidermidis). Bir hafta içinde enterobakteriler (özellikle
E.Coli formula ile beslenen bebeklerde, Lactobacillus spp anne sütü ile beslenen bebeklerde
daha fazla) gastrointestinal sistemi kolonize eder.
Yoğun bakım ünitelerinde tedavi edilen bebeklerin çoğu geniş spektrumlu antibiyotik
aldıklarından, bunların deri, gastrointestinal sistem ve respiratuvar sistemlerinde birçok
ilaca dirençli gram pozitif (S.epidermidis) ve gram negatif (E.coli, Klebsiella, Pseudomonas)
mikroorganizmalar kolonize olur.
Yenidoğan Sepsisine neden olan mikroorganizmalar
Grup B Streptokoklar: Bu grupta S. agalactiae bulunur. Yenidoğan döneminde fokal veya
sistemik enfeksiyonların en sık görülen nedenidir. Yeni çalışmalar son zamanlarda azaldığını
göstermiştir. Erken başlayan hastalıkta bebek mikroorganizmayı doğum esnasında ve
doğarken alır. Gebelikte maternal kolonizasyon oranı ortalama % 20 kadardır. Fakat kültür
pozitif bebeklerdeki yaygın hastalık oranı % 1' den daha azdır. Bunun nedeni kolonize
annedeki bu serotipe karşı serum antikor oranının yüksek olmasından ve bunun fetusa geçip
korumasındandır. Son yıllarda anneye antibiyotik verilmesiyle yenidoğanda GBS enfeksiyonu
önlenebileceği gösterilmiştir.
Yenidoğan Sepsisine neden olan mikroorganizmalar
Escherichia coli: E.Coli neonatal sepsis ve menenjite yol açan en önemli gram negatif
mikroorganizmadır. Annenin normal vajinal ve intestinal florasında bulunabilen bir bakteridir.
Epidemiyolojik çalışmalar esas olarak anneden vertikal geçişin sorumlu olduğunu
göstermiştir. Personelden kaynaklanan nazokomiyal geçişler de gösterilmiştir. K1 tipi
kapsüler antijen içeren suş neonatal menenjitin %88’inden sorumlu bulunmuştur.
Yenidoğan Sepsisine neden olan mikroorganizmalar
Koagülaz negatif stafilokoklar: Normal deri florasının bir parçası olan bu stafilokoklar
geleneksel olarak nonpatojen olarak sınıflandırılmalarına rağmen, son zamanlarda neonatal
mortalite ve morbiditenin önemli nedenlerinden biri haline gelmiştir. Bu grupta
S.epidermidis, S.saprophyticus ve S.hemolyticus bulunur. Özellikle S.epidemidis polietilen
intravenöz kateterler yolu ile enfeksiyona neden olmaktadır. Birçok suşu penisilinaza dirençli
penisilinlere karşı rezistan olduğundan (meticilin, oxacillin), bu enfeksiyon parenteral
vankomisin ile tedavi edilmelidir.
Yenidoğan Sepsisine neden olan mikroorganizmalar
Listeria monocytogenes: Kısa, gram negatif, hareketli çomaklardır. Transplasental geçerek
düşüklere neden olur. Enfekte bebekler prematüre olup, hepatosplenomegali ve multisistem
hastalığı ile karakteristiktir. Vertikal geçiş sıktır. Enfekte bebeklerde erken başlayan hastalık
grup B streptokoklardan ayrılmalıdır.
Yenidoğan Sepsisine neden olan mikroorganizmalar
Candida enfeksiyonu: Candida türleri yenidoğanda ağızda lokal lezyon moniliasis ve genital
bölgede dermatitis yapabildiği gibi özellikle çok düşük doğum ağırlıklı bebeklerde septisemiye
yolaçabilmektedir. Gebelikte anne vajinasındaki kolonizasyon oranı %33’e kadar
çıkabilmektedir. Çok düşük doğum ağırlıklı bebeklerde septisemi oranı %2-5 olarak
bildirilmektedir. Uzun süre ventilatör tedavisi alan ve immun direnci baskılanmış miadında
yenidoğanlarda da septisemiye yol açabilmektedir.
Yenidoğanda sepsisinin klnik olarak sınıflandırılması
Yenidoğan sepsisinin klinik bulguları oldukça değişkendir. İyi giden bir bebekte anormal
saptanan her bulgu sepsisin bir belirtisi olabilir. Bazen bir sisteme özgü klinik bulgular
izlenebilirken çoğunlukla multisitemik bulgular karşımıza çıkar. Bebekte metabolik asidoz
gelişir, hipoksemi ve karbondioksit retansiyonu başlar.
Yenidoğan sepsisinde klinik bulgular
Yenidoğan sepsisinde laboratuvar incelemeleri
A) Kültür:
Kesin tanı kültürde mikroorganizmanın göstermesiyle konur. Bu yüzden tedavinin
başlangıcında kan kültürü, BOS kültürü, idrar kültürü ve mümkünse trakeal aspirat kültürü
alınmalıdır. Boğaz, cilt ve dış kulaktan alınan kültürler kesin tanıyı sağlamaz, fakat bebeğin
hangi mikroorganizmalarla kontamine olduğunu gösterir. Kültür örneklerinin yanında gram
boyama incelemesi de yapılabilir. Pozitif sonuçta daha erken tanı koyma imkanı elde edilir.
Kültürlerde üreme bekleninceye kadar ampirik antibiyotik tedavisi başlanmalıdır. Son yıllarda
lateks agglütinasyon yöntemiyle mikroorganizmaları daha erken tanıma yolunda ilerlemeler
sağlandı. Fakat bu testler kültürler kadar sensitif değildir ve yalancı pozitiflik oranı da oldukça
fazladır.
B)Tam kan sayımları:
1. Lökositoz ve lökopeni. Yenidoğan döneminde ilk bir haftada 25000/mm3 daha sonra 15000
/mm3 üzerindeki değerlere lökositoz, 5000 /mm3 altındaki değerlere ise lökopeni denir.
Lökopeni ile seyreden yenidoğan sepsislerinin prognozu daha kötüdür.
2. Formülde sola kayma. Yenidoğan döneminde ilk 7 günde nötrofil ağırlıklı (%65-70 PNL, %2530 lenfosit) hücre sayılırken, 7 günden sonra lenfosit ağırlıklı hücreler sayılır. Formülde
nötrofil oranıyla birlikte immatür nötrofil (çomak) hücrelerinin artması (sola kayma)
yenidoğan sepsisisnde sık rastlanan bir laboratuvar bulgusudur.
3. İmmatür nötrofil / Nötrofil oranı. Bu oranın 0.20’den büyük olması yenidoğan sepsisi için
anlamlıdır.
4. Toksik granülasyon. Nötrofillerin içinde toksin içeren granüllerin görülmesi sepsis lehine
yorumlanır.
5. Trombositopeni: 100 000/mm3 altındaki değerler sepsis için anlamlıdır. Trombositopeni ne
kadar ağır ise prognoz o kadar kötü olur.
6. CRP (C-reaktif protein) tayini. Sepsis teşhisi için oldukça hassas bir testtir. Yenidoğan
döneminde enfeksiyondan başka hemen hemen hiçbir durum CRP’yi artırmaz. Sepsisin
başlangıcından 48-72 saat sonra kanda pozitif bulunur. 6 mg/L üzerindeki değerler sepsis için
anlamlıdır.
C)Diğer incelemeler:
Kan gazı. Sepsiste, özellikle multisistemik tutulumda ağır metabolik asidoz gelişir. Pnömoni
ön planda olan hastalarda ise karbondioksit birikimi olur. Düzensiz solunum ve ağır apne
ataklarında hipoksemi dikkati çeker.
Kan glukozu. Sepsiste stress hormonlarına yanıt olarak hiperglisemiye rastlanabilir. Tam
tersine özellikle prematüre bebeklerde ise hipoglisemi gelişebilir. Hipoglisemide prognoz
daha ağırdır.
PT/PTT aktiviteleri. Karaciğer tutulumu olan ve DIC’a giren hastalarda PT/PTT değerleri
uzamıştır ve hastada durdurulması güç kanamalar başlar.
Göğüs filmi ve ayakta direk abdominal grafi. Pnömoni teşhisini koymak için mutlaka göğüs
filmi incelenmelidir. Ayakta direk abdominal grafide ise batın gaz dağılımı, hava-sıvı seviyesi
ve batında serbest hava bulguları aranarak NEK şüphesi giderilmeye çalışılır.
Tedavi
İlk ampirik tedavi
Neonatal sepsisin, özellikle erken dönemdeki bulguları çok belirsizdir ve yenidoğan
bebeklerin diğer hastalıklarının bulgularından ayırt edilmesi mümkün değildir. Neonatal
sepsis yaşamı tehdit eden çok acil bir durumdur. Tanı ve tedavide gecikmenin sonuçları
ağırdır. Kültür sonuçlarının beklenmesi zaman kaybına neden olacağından, şüpheli vakalarda
kan kültürü alındıktan hemen sonra ampirik antibiyotik tedavisine başlanması gerekir.
Şüpheli vakalarda hemen başlanan ampirik antibiyotik tedavisi, tedaviye başlanmamış
bebeklerdekinden çok daha zararsızdır. İki veya üç günlük ampirik antibiyotik tedavisinden
sonra, kültür ve antibiyotik duyarlılık testlerinin sonuçlarına göre seçilecek antibiyotikler
ayarlanır veya tamamen kesilebilir. Klinik bulguları iyi olan bir bebekte kültürlerde üreme
olmazsa antibiyotik tedavisi kesilmelidir. Aksi takdirde dirençli gram-negatif bakteri
kolonizasyonu gelişebilir.
Gebelik yaşı küçüldükçe enfeksiyon sıklığı daha fazladır. Ancak küçük prematüre bebeklerde
sepsis bulgularını ayırt etmek, daha büyük bebeklerden çok daha zordur. Bu nedenle kan
kültüründe üreme olmasa bile küçük prematüre bebeklerde antibiyotik tedavisine sıklıkla beş
gün veya daha fazla devam edilir.
Şüpheli sepsis” vakalarının belirlenmesinde “Töllner’in Skorlaması” kullanılabilir
** 4 puan verilir.
Toplam puan: 5-10 sepsis olasılığı , > 10 kesin sepsis.
Erken neonatal sepsiste tedavi
Yaşamın ilk haftası içinde sepsis gelişen bebeklerde seçilecek ampirik antibiyotikler GBS, E.
coli ve Listeria monocytogenes’e etkili olmalıdır. ABD ve Avrupa’da erkek neonatal sepsis
etkenleri aşağı yukarı aynı iken, tropikal ülkelerde GBS oldukça seyrek görülürken, E. coli,
Klebsiella ve Serratia türleri daha sıktır. Ülkemizde de erken neonatal sepsis etkenleri
arasında gram-negatif enterik bakterilerin, GBS’lerden önde geldiği sanılmaktadır. Gelişmiş ve
gelişmekte olan ülkeler arasında görülen bu farklılığın nedeni cinsel alışkanlıklara ve genetik
özelliklere bağlanmaktadır
Erken neonatal sepsiste penisilin veya ampisilin ile birlikte bir aminoglikozitle ampirik
tedaviye başlanması uygun olur. Ampisilin ve aminoglikozit kombinasyonun antimikrobiyal
aktivitesi daha geniştir. Penisilin ile karşılaştırıldığında, ampisilinin L. monocytogenes ile bazı
gram-negatif patojenlere (özellikle E. coli ve Proteus mirabilis’e) karşı etkinliği daha fazladır.
Geç neonatal sepsiste tedavi
Yaşamın ilk haftasından sonra görülen sepsis vakalarında da tedaviye erken neonatal sepsis
etkenleri ile birlikte Stafilokoklar, Enterokoklar ve Pseudomonas aeruginosa da göz önüne
alınarak başlanır. Erken neonatal sepsiste olduğu gibi tedaviye penisilin veya ampisilin ve bir
aminoglikozitle başlanabilir.
Stafilokokal enfeksiyon yönünden riskli bir durum varsa (örneğin vasküler kateterizasyon), ilk
ampirik tedaviye antistafilokokal penisilin veya vankomisin artı bir aminoglikozit ile
başlanması uygun olur. Geç neonatal sepsisin ampirik tedavisine seftriakson ve vankomisin
kombinasyonu ile de başlanabilir. Psödomonas enfeksiyonu riski varsa (örneğin tipik
mukokütanöz lezyonları varsa), ilk ampirik tedavide anti-psödomonas ilaçlar kullanılabilir.
E.coli ve K. pneumonia enfeksiyonları bir penisilin türevi (ampisilin veya izole edilen suşa göre
geniş-spektrumlu penisilin) ve bir aminoglikozit ile tedavi edilebilir. Bu enfeksiyonların
tedavisinde bazen dirençli olsalar da üçüncü-jenerasyon sefalosporinler yalnız veya bir
aminoglikozitle birlikte kullanılabilir.
Enterobacter, Serratia, Citrobacter ve indol-pozitif Proteus türleri ile P. aeruginosa’ya bağlı
enfeksiyonların tedavisinde üçüncü-jenerasyon sefalosporinler aminoglikozitlerle birlikte
kullanılır.
Geniş-spektrumlu penisilinler karboksipenisilinler ve açilampisilinlerdir. Neonatal sepsise yol
açan bakterilerin çoğu bu antibiyotiklere duyarlıdır. Bu antibiyotiklerin üstün yanlarından
birisi de ampisiline dirençli P. aeruginosa ve bazı Proteus türlerine de etkili olmalarıdır. Buna
karşılık stafilokokların yaptığı beta-laktamaz’a duyarlı olduklarından, stafilokoklara bağlı
enfeksiyonlarda kullanılmaları önerilmez.
Karboksipenisilinler; karbenisilin ve tikarsilin’dir. Her ikisinin antimikrobiyal etkinlikleri
birbirlerine benzer. Ancak P. aeruginosa’ya karşı tikarsilin’in etkinliği daha fazladır. Kuvvetli
bir beta-laktamaz inhibitörü olan klavulonik asit ile birlikte verilmesi tikarsilin’in etkinliğini,
tikarsilin’e dirençli türleri de kapsayacak şekilde artırır.
Açilampisilinler; ureidopenisilinler (mezlosilin ve azlosilin) ve piperasilin’dir. Piperasilin ve
azlosilin, geniş-spektrumlu penisilinler arasında P. aeruginosa’ya karşı en etkili olanlardır. Bu
üçü arasında P. aeruginosa’ya karşı en az etkili olan mezlosilin olmasına karşı, bu bakteriye
karşı etkinliği tikarsilin kadardır.
Dirençli bakterilere karşı diğer antibiyotikler
Karbapenemler: Beta-laktam yapısındaki karbapenemler arasında ilk kullanılan imipenem’dir.
İmipenem ile aminoglikozitler arasında sinerjistik etki vardır. İmipenem meningeal
enflamasyon varlığında BOS’a iyi geçer. Ancak imipenem’in nörotoksik olması, menenjit
vakalarında kullanımını sınırlar. P. aeruginosa dışında tedavi sırasında imipenem’e dirençli
suşların ortaya çıkması çok az görülür. Diğer bir karbapenem olan meropenem’in gramnegatif bakterilere karşı etkinliği daha fazladır.
Aztreonam: Aztreonam bir sentetik monosiklik beta-laktam (monobaktam) antibiyotiktir.
Ancak beta-laktamaz’lara karşı dirençlidir ve kromozomal beta-laktamaz indüksiyonu
yapmaz. Aztreonam’ın antibakteriyel etkinliği diğer beta-laktam antibiyotiklerden farklı olup,
daha çok aminoglikozitlere benzer. Aminoglikozitlere benzer etkinliği, BOS’a geçişinin iyi
olması, nefrotoksik ve ototoksik yan etkilerinin olmaması, neonatal sepsis tedavisinde
ampisilin ile birlikte kullanılmasını sağlamıştır. Aztreonam, diğer aminoglikozitlerle birlikte
kullanıldığında P. aeruginosa ve diğer birçok gram-negatif enterik bakteri üzerinde sinerjistik
etki yapmaktadır.
Kinolonlar: Kinolonlar, yani florokinolonlar bakteriyel DNA repilakasyonun inhibe ederek
bakterisidal etki gösterirler. Bazı merkezlerde P. aeruginosa dahil gram-negatif bakterilere
bağlı enfeksiyonların tedavisinde siprofloksasin yalnız başına veya diğer antibiyotiklerle
birlikte kullanılmaktadır. Bununla birlikte küçük çocuklarda gelişen kıkırdak dokusu üzerindeki
olası etkileri nedeniyle kullanılması önerilmemektedir. Ancak bugüne kadar daha büyük
çocularda yapılan çalışmalarda, kinolonların böyle bir etkisi görülmemiştir.
Neonatal sepsisin ilk ampirik tedavisinde seçilecek antibiyotik kombinasyonları.
Neonatal sepsis tedavisinde kültür sonuçlarına
göre verilebilecek antibiyotikler.
Tedavi süresi
Neonatal sepsiste antibiyotik tedavisinin süresi, her vakada değişmekle birlikte fokal
enfeksiyonu olmayan veya çok az olan bebeklerde 10-14 günden az olmamalıdır. Gramnegatif bakterilere bağlı menenjit varsa bu süre en az 21 gündür. GBS ve L. monocytogenes’e
bağlı menenjitlerde tedavi süresi en az 14 gündür.
Profilaksi
Grup B streptokok enfeksiyonları
Toplumda vajinal GBS taşıyıcılığının yüksek olduğu yörelerde, yenidoğan bebekte GBS
enfeksiyonlarını önlemek için en uygun yaklaşım, taşıyıcı gebelere intrapartum antibiyotik
verilmesidir. Çünkü bu kadınlardan doğan bebeklerin % 30-70’inde GBS kolonizasyonu
olmakta, bu bebeklerin de % 1-2’sinde hastalık görülmektedir.
Erken membran rüptürü (EMR)
EMR ve korioamnionit bütün gebeliklerin sırasıyla % 10 ve % 1’inde görülür. Yalnız EMR olan
gebelerin bebeklerinin % 1’inde, EMR ile birlikte korioamnionit olanların % 10’unda
yenidoğan bebekte sepsis gelişir. Bu oranlar prematüre bebeklerde çok daha fazladır. EMR’li
annelerden doğan prematüre bebeklerin üçte ikisinde intrauterin enfeksiyon bulguları
saptanmıştır. Bu nedenle EMR’li veya korioamnionitli kadınlara anaerop bakterileri de
kapsayan geniş spektrumlu antibiyotikler (örneğin ampisilin) verilmelidir. Ancak EMR
saptanmamış, prematür eylemdeki gebelere rutin olarak antibiyotik başlanması uygun
değildir.
Mekonyum aspirasyonu
Mekonyum aspirasyonu için endotrakeal aspirasyon yapılan bebeklere genellikle (erkensepsisdeki gibi) proflaktik antibiyotik başlanmaktadır. Bu konuda son zamanlarda yapılan bir
çalışmada zamanında doğan bebeklerde böyle bir işlemden sonra antibiyotik başlanmasının
gereksiz olduğu saptanmıştır. Ancak prematüre bebeklerde böyle bir antibiyotik proflaksisi
gerekmektedir.
İnvasif girişimler
Örneğin endotrakeal entübasyon, vasküler kateterizasyon yapıldıktan sonra proflaktik
antibiyotik başlanmasının nazokomiyal enfeksiyonları önlemede yeterli olmadığı
gösterilmiştir. Hatta gereksiz yere başlanan antibiyotikler dirençli mikroorganizmaların ortaya
çıkmasına yol açmaktadır. Vasküler kateterizasyon yapılan hastalarda stafilokokal
enfeksiyonlar daha sık görülürse de enfeksiyon süresini belirleyen daha çok kateterizasyonun
süresidir ve proflaktik antibiyotik başlanmasına gerek yoktur.