394
Derleme Review
İlaçlarla İlişkili İnterstisyel Akciğer
Hastalıkları
Drug-Induced Interstitial Lung Diseases
Dr. Abdurrahman ŞENYİĞİT
Dicle Üniversitesi Tıp Fakültesi, Göğüs Hastalıkları Anabilim Dalı, Diyarbakır
ÖZET
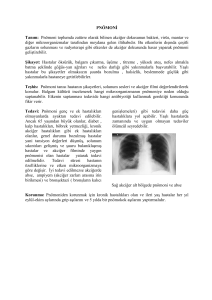
İlaçlara bağlı akciğer hastalıkları sık görülen iatrojenik hastalıklardır. Klinik prezentasyonları hafif-ağır olabileceği gibi fatal seyredebilir. İlaçlara bağlı akciğer hasarı çeşitli sitotoksik ve nonsitotoksik ilaçlara bağlı gittikçe
daha fazla görülen akut ve kronik akciğer hastalıklarına neden olmaktadır. İlaçlara bağlı akciğer toksisitesinin
en sık görülen formu ilaçlara bağlı akciğer hastalığıdır (İBAH). İlaçların oral ve parenteral kullanımı İBAH’a en
sık sebep olan kullanım şekli olarak bildirilmesine karşın nebül ve intratekal uygulanımı da buna sebep olabilir.
Anahtar Kelimeler: İlaçlar, pulmoner hastalıklar
SUMMARY
Drug-induced adverse respiratory disorders are common iatrogenic illnesses. Their clinical presentation may be
mild to severe and even fatal. Drug-induced lung injury, an increasingly common cause of both acute and chronic
lung disease, is caused by numerous cytotoxic and noncytotoxic drugs. The most common form of drug-induced
lung toxicity is drug-induced interstitial lung disease (DILD). Oral and parenteral routes of drug administration
are most frequently cited as causing DILD; however, nebulized and intrathecal administration have also been
implicated.
Key Words: Drugs, pulmonary diseases
Yazışma Adresi / Address for Correspondence
Prof. Dr. Abdurrahman ŞENYİĞİT
Dicle Üniversitesi Tıp Fakültesi, Göğüs Hastalıkları Anabilim Dalı, Diyarbakır
e-posta: [email protected]
DOI: 10.5152/gghs.2014.030
Güncel Göğüs Hastalıkları Serisi 2014; 2 (3): 394-401
Şenyiğit A.
GİRİŞ
İlaçlara bağlı akciğer hastalıkları (İBAH), tedavi
amaçlı olarak kullanılan maddelerin solunum sistemi
üzerinde oluşturduğu hasar ve yan etkilerdir(1). Literatürde İBAH üzerine ilk kaynak 1880 yılına aittir.
Günümüze kadar gittikçe artan miktarda vakalar bildirilmesine karşın çalışmaların çoğu kemoterapötik
ajanların akciğerler üzerindeki etkilerine bağlıdır. Ancak İBAH sıklığı tam olarak bilinmemektedir. Konu
ile ilgili ilk yayınlarda ABD’de bildirilen ilaç yan etkilerinin % 5’inin akciğerler ile ilgili yan etkiler olduğu
bildirilmiştir.
Çok sayıda ilacın akciğerler üzerine yan etkileri vardır. Oluşan klinik hafif, orta veya ağır olabileceği gibi
bazen fatal seyredebilir(2). Günümüzde 700 civarında
ilacın buna sebep olduğu ancak en fazla kemoterapötik ilaçların buna sebep olduğu bildirilmiştir. Bu ilaçların listesine www.pneumotox.com web sayfasından
ulaşılabilmektedir(3, 4).
Epidemiyoloji: ABD’de yıllık yaklaşık 2 milyon ilaç reaksiyonu 100.000 ölüm bildirilmektedir. Yine İngiltere’de advers, ilaç reaksiyonlarına bağlı yıllık 250.000
hospitalizasyon bildirilmektedir. Yine bir İsveç çalışmasında advers ilaç reaksiyonlarının 7. ölüm sebebi
olduğu bildirilmiştir. Ancak İBAH’ın tam sıklığı bilinmemesine karşın rakamların bildirilenlerden daha
fazla olduğu tahmin edilmektedir. İnterstisyel akciğer
hastalıklarının tam insidansı bilinmiyor ise de bunların %2-3’ünün ilaçlara bağlı olduğu kabul edilmektedir(5). İBAH’ın %70 kadarını interstisyel akciğer hastalığı oluşturmaktadır(3, 4, 6).
•
•
•
•
•
•
•
•
Cinsiyet
Genetik yatkınlık
Bazal akciğer işlevleri
Altta yatan hastalık
Çevresel faktörler
İlacın aktivasyon ve detoksifikasyonu
Doz
Radyasyon
Patogenez:
İBAH oluşumunda toksik ve immünolojik mekanizmalar sorumlu tutulmaktadır(5, 7). Toksisiteye bağlı olanlarda reaksiyon doza bağımlı olarak izlenir (amiodaron,
bleomisin, siklofosfamid gibi). Ancak immünolojik mekanizmalarla gelişenler ise dozdan bağımsız oluşur(8).
İBAH başlıca 3 şekilde ortaya çıkmaktadır:
1) Kronik diffüz akciğer hastalığı,
2) Akut akciğer hasarı ve
3) Vasküler hastalıklar.
Bu 3 tablo çoğu zaman iç içe geçmiş durumdadır.
İBAH’ın etkileri sıklıkla akciğer parankiminde olmak
üzere plevrada, hava yollarında, pulmoner vasküler sistemde, nöromusküler sistemde ve mediastende görülebilir. Bunlar nonkardiyojenik pulmoner ödem, hipersensitivite pnömonitisi, organize pnömoni, pulmoner
hipertansiyon, interstisyel pnömoni, plevral efüzyonlar, diffüz alveoler hasar, eozinofilik pnömoni, pulmoner hemoraji, granülomatöz pnömonitis ve mediastinal lenfadenopati vb. içeren geniş bir spektrumdur(9).
İBAH fizyopatolojisi
Klinik: İBAH’da klinik semptomlar genellikle benzerdir. Ancak bazen benign infiltratlarla karakterize olmasına karşın bazen de akut respiratuar distres sendromuna yol açabilir(7). Yakınmalar akut, subakut veya
kronik olabilir. İlaç kullananlarda yeni ve ilerleyici
solunum yakınması olan her hastada ilaç reaksiyonları düşünülmelidir(6). Ateş, kırgınlık, nonprodüktif
öksürük ve dispne genellikle mevcuttur. Bazı olgularda hipoksi gelişir(2). Çoğu olguda solunum fonksiyon
testlerinde restriktif tipte solunum fonksiyon bozukluğu ve DLCO’da azalma vardır(2, 7).
Bazı ilaçlar akciğerlerde endotel hücreleri üzerinde
direkt toksik etkiye sahiptir. Böylece kan bariyeri bozulur ve proteinler önce interstisyuma sonra da alveollere geçer. Proteinler burada kompleksler oluşturur
ve sonuçta hyalen membranlar oluşur. Ayrıca eksuda
vasfında sıvıda alveollere geçerek hipoksi oluşturur.
Bu dönemde maruziyet devam ederse organize pnömoniye gidiş olur. Yine bazı ilaçlar immün kompleksler oluşturur (ya immünojenik mekanizmalarla veya
hapten rolü oynayarak). Bu olgularda nonspesifik interstisyel pnömoni (NSIP) veya lenfositik interstiyel
pnömoni (LIP) paternleri oluşur(1).
Risk Faktörleri: İBAH’ın oluşumunda bildirilen bazı
risk faktörleri şunlardır(5):
Ancak İBAH’da tüm interstisyel paternlerin oluşabileceği de unutulmamalıdır(10).
• Yaş: İleri yaş ve çocukluk dönemlerinde İBAH
daha fazla görülür.
• Birlikte alınan ilaç ve tedavi etkileşimleri: Örneğin cisplatin ve bleomycinin birlikte verilmesi
durumunda toksisite artabilir.
İBAH’DA histolojik paternler
İBAH’da farklı histolojik paternler izlenebilir. Birçok
ilaç kullanımında benzer histolojik paternler izleneGüncel Göğüs Hastalıkları Serisi 2014; 2 (3): 394-401
395
396
İlaçlarla İlişkili İnterstisyel Akciğer Hastalıkları / Drug-Induced Interstitial Pulmonary Diseases
bildiği gibi birden fazla paterni aynı ilaca bağlı görmek
mümkündür. Ancak tüm bu paternler nonspesifiktir
ve kollajen doku hastalıkları veya idiyopatik interstisyel akciğer hastalıklarını taklit edebilir(7). Tablo 1’de
İBAH histolojik paternleri görülmektedir(8, 9).
İlk grupta yer alan interstisyel patern en sık görülen
formdur. Bu hastalıklarda görülen radyolojik bulgulara benzer görünümler saptanır. Bu tabloyu oluşturan ilaçlar içinde amiodaron, altın, busulfan, kinidin,
klorambusil, kokain, siklofosfamid, metotreksat,
fenitoin vb. sayılabilir(9, 11). Yine bu grupta yer alan
diffüz alveoler hasar ARDS tablosu olarak klinisyenin
karşısına çıkabilir. Özellikle amiodaron, amitriptilin,
azatioprin, bleomisin, busulfan, eroin, erlotinib, gefitinib, kokain, IV immunglobulinler bu tabloyu oluşturabilir(9, 12). Bu grupta yer alan organize pnömoniler
(eski adı ile bronşiolitis obliterans organize pnömoni
–BOOP-) hava boşluklarını dolduran organize tıkaçlarla karakterizedir. İdiyopatik olanına kriptojenik
organize pnömoni denir(13). İlaç kullanımı dahil herhangi bir sebebin saptanmadığı durumlarda kriptojenik organize pnömoni olarak sınıflandırılır. Sorumlu
ilaçlar; amiodaron, bleomisin, kokain, siklofosfamid,
lökovorin, kromolin sodyum, penisilamin, fenitoin
vb. sayılabilir(9, 11). Yine özellikle romatoid artrit nedeniyle D-penisilamin ve 5-aminosalisilik asit kullanan
kadın hastalar ile inflamatuar barsak hastalıklarında
kullanılan sulfasalazin ve 5-aminosalisilik asit BOOP
ile ilişkili bulunmuştur. Ancak romatoid artrit ile inflamatuar barsak hastalıkları da akciğerlerde BOOP
yaptığından bunun primer nedene mi yoksa ilaçlara
bağlı mı olduğunu ayırt etmek kolay değildir. BOOP
klinik tablosunun ortaya çıkması ilk 2 haftadan 3 yıla
kadar uzayabilir ve genellikle progresiftir. Hastalarda
genellikle ilerleyici dispne, öksürük, ateş ve hırıltılı
solunum vardır. Çekilen akciğer grafisinde bilateral
yama tarzında, asimetrik ve gezici yer değiştiren opasiteler saptanır(8, 14).
İkinci grupta yer alan pulmoner eozinofili ilaç reaksiyonlarında görülebilen ve periferik eozinofilinin de
eşlik ettiği (her zaman olmayabilir) bir paterndir. En
sık sorumlu tutulan ilaçlar nonsteroid antiinflamatuar ilaçlar (NSAID), asetaminofen, ampisilin, bleomisin, kaptopril, kokain, hidralazin, nitrofurantoin,
penisilin, prokarbazin, propranolol, streptomisin,
sulfasalazin, tetrasiklin vb.’dir(9, 12, 15). Yine bu grupta
yer alan pulmoner ödemin tanınması da önemlidir.
Genelde klinik bulgular tanı için yeterli olup nadiren
biyopsiye gerek duyulur. Nonkardiyojenik pulmoner
ödemden sorumlu olan bazı ilaçlar albuterol, aspirin,
klordiazepoxide, kokain, kodein, eroin, haloperidol,
hidroklorotiazid, magnezyun sülfat, nifedipin, penisilin, salbutamol, radokontrast ilaçlar, salisilat, sulindak, lidokain vb. ‘dir(9, 11, 12). Bu gruptaki pulmoner hemoraji alveoler boşlukların kan ve hemosiderin yüklü
Güncel Göğüs Hastalıkları Serisi 2014; 2 (3): 394-401
Tablo 1. İBAH histolojik paternleri.
1. İnterstisyel patern
a. Diffüz alveoler hasar
b. Organize pnömoni
c. Usual interstisyel pnömoni benzeri patern
d. Diffüz sellüler interstisyel infiltratlar-granülomlar
e. Nonspesifik interstisyel pnömoni
f. Lenfositik interstisyel pnömoni
g. Hipersensitivite pnömonitisi
h. Metastatik kalsifikasyon
i.Bronşiolit
j.Bronşektazi
2. Alveoler patern
a. Nonkardiyojenik pulmoner ödem
b. Alveoler hemoraji
c. Alveoler proteinozis benzeri reaksiyon
d. Akut veya kronik eozinofilik pnömoni
e. Panasiner amfizem veya büllöz hastalıklar
3. Vasküler patern
a. Yabancı cisim dev hücre reaksiyonu (IV ilaç kullanımına bağlı)
b. Küçük damar vasküliti
c. Pulmoner arteryel hipertansiyon
d. Pulmoner veno oklüziv hastalıklar
e. Pulmoner tromboembolizm
4. Plevral patern
a.Plörit
b. Plevral efüzyon
c.Pnömotoraks
d.Hemotoraks
makrofajlarla dolması ile karakterize olup amfoterisin-B, amiodaron, atanersept, kokain, siklofosfamid,
haloperidol, hidralazin, mitomisin, antikoagülan ve
trombolitik ajanlar gibi farklı yaklaşık 80 ilaca bağlı
görülebilir(6, 9, 11). İlaca karşı oluşan immün reaksiyon,
alveolokapiller bazal membranda hasarlanma ve ilaca bağlı koagülasyon sisteminde bozukluk bu konuda
öne sürülen 3 temel mekanizmadır(8, 16, 17). Otoantikorlar (ANCA) bu durumda yüksek titrede bulunur (8).
Üçüncü grupta yer alan vaskülit genellikle küçük çaplı
arterleri tutan vaskülittir. Lökotrien reseptör antagonistlerine bağlı vaskülitler bildirilmiştir(9, 18). Yine
Şenyiğit A.
mitomisin ve kombine kemoterapi ilaçlarına bağlı
vasküler trombozlar bildirilmiştir(11). Bu grupta yer
alan pulmoner hipertansiyon bazen ölümcül olabilmektedir. Mitomisin, aminorex, fenfluramin ve metamfetamin gibi ilaçların yanı sıra kokain gibi maddelerde pulmoner vazokonstriksiyona neden olabilir.
Literatürde yaklaşık 36 ilaç pulmoner arteriyel hipertansiyonla ilişkilendirilmiştir (11, 19, 20). Mekanizmasında serotonin artışı (pulmoner arter düz kas hücreleri
için büyüme faktörüdür) suçlanmıştır(19, 20). European
Respiratory Society/European Society of Cardiology
pulmoner arteriyel hipertansiyon yapan ilaçları 4 kategoriye ayırmıştır(21):
mu için yeterli olmakta ve ilaç kullanım öyküsü son
3 aydan 2 yıla kadar uzayabilmektedir. Tedavinin kesilmesi ile birlikte plevral sıvı birkaç gün veya birkaç
ay içinde gerilemektedir. Propiltiourasil, sülfasazalin,
izoretinoid ve dantrolen gibi ilaçlar eozinofilik plevral
efüzyona yol açabilir. Pnömotoraks bleomisin veya
trimipramin kullanan hastalarda oluşabilir. P. jirovecii
pnömonisi geçiren ve inhale pentamidin proflaksisi
uygulanan AIDS’li hastalarda da gözlemlenebilir. Oral
antikoagülan olan warfarin kullanan olgularda hemotoraks görülebilir. Özgeçmişinde asbest maruziyeti
olanlarda bromokriptin kullanımında bunun sinerjistik etkisi ile plevral fibrozis oluşabilir(8).
1) Definite: aminorex, fenfluramine, dexfenfluramine
veya benfluorex
Bu histolojik paternler dışında 2) Possible: cocaine, phenylpropanolamine, chemotherapeutic agents veya selective serotonin reuptake
inhibitors (SSRI)
3) Likely: amphetamines/methamphetamines veya
L-tryptophan
4) Unlikely: cigarette smoking, oral contraceptives
veya oestrogens.
Yine özellikle pulmoner hipertansiyon tedavisinde
de kullanılan tirozin kinaz inhibitör grubuna ait dasatinibin kendisi de pulmoner hipertansiyona yol açmaktadır(8, 22). Akciğerlerde granülomatöz lezyonların
en sık sebepleri genellikle mikobakteriyel veya fungal
enfeksiyonlardır. Nekroz varlığı sıklıkla enfeksiyonu
düşündürür. Asebutol, kokain, fenoksimetilpenisilin,
metotreksat, nitrofurantoin, prokarbazin, sirolimusun yanı sıra mesane kanserinde kullanılan BCG’de
akciğerlerde granülom oluşumuna neden olabilir(9, 11).
Bu grupta yer alan pulmoner tromboembolizme yol
açan birçok ilaç vardır. Oral kontraseptifler, östrojen,
klozapin ve darbepoetin başta olmak üzere yaklaşık
38 ilaç PTE yapabilir. Yine bu gruptaki pulmoner venooklüziv hastalık pulmoner ven/venüllerin organize
trombus ve/veya endoluminal fibrozis ile daralmasıyla karakterizedir. Buna yol açan 9 ilaç (karmustin, bleomisin, mitomisin, busulfan vb.) bildirilmiştir(8, 13, 22).
Plevral hastalıklara neden olan yaklaşık 40 ilaç içinde asiklovir, amiodaron, nitrofurantoin, itrakonazol,
mitomisin minoksidil vs sayılabilir. Yine klorpromazin, izoniazid, meselamin, metildopa, penisilamin ve
kinidin plevral efüzyonun eşlik ettiği veya etmediği
lupus benzeri plöroperikardite neden olabilir(9). İlaca
bağlı lupus (antinükleer ve antihiston antikor pozitif) iatrojenik plevral efüzyonun en sık nedenidir.
İlaca bağlı lupus olgularının %50’sinden fazlasında
akciğer veya plevra tutulumu olması spontan gelişen
lupus eritematozustan başlıca farkını oluşturur. Az
bir doz uygulanması bile lupus eritematozus oluşu-
1. Hava yolları etkilenimi oluşturan ve özellikle
astımlılarda bu etkiyi oluşturan 2 ilaç asetil salisilik asit ve beta blokerlerdir. ACE inhibitörleri
öksürük oluşturabilir. Ayrıca analjezik intoleransı asetil salisilik asit veya diğer NSAİ ilaçların alımından sonra birkaç saat içinde gelişebilen bronkospazm, anaflaktik şok, ürtiker veya
rinit semptomlarından oluşan bir klinik tablodur. Altta yatan mekanizma tam olarak bilinmemekle beraber prostaglandin metabolizması
ile ilişkili olduğuna dair yayınlar mevcuttur.
2. Mediastinal tutulum: Antimigren bir ilaç olan
metiserjid mediastinal ve retroperitoneal fibrozise yol açabilir. Steroid tedavisi ile mediastinal
lipomatozis oluşabilir. Bleomisin, karbamazepin, penisilin, fenitoin vs kullananlarda hiler
veya mediastinal büyümüş lenf nodları gözlenebilir.
3. Nöromusküler tutulum: Myastenia gravis hastalarında IV aminoglikozid uygulanması sonrası akut solunum yetmezliğine yol açan solunum
kas paralizisi oluşabilir. Uygulanan neostigmin
ile tablo geri dönebilirse de bazen mekanik ventilasyon uygulanması gerekebilir(8, 23).
Radyolojik Bulgular:
Akciğer radyogramları radyolojik tanıda ilk başvurulan görüntülenme yöntemleri olmakla beraber tanıda
yeri sınırlıdır. Yüksek çözünürlüklü BT (YÇBT), parankimal değişikliklerin varlığı ve dağılımını detaylı
göstermede, ayırıcı tanıda ve tedaviye yanıtı belirlemede son derece yararlıdır. Ancak spesifik tanıyı koymada yetersizdir(13). Genellikle bu olgularda yaygın/
yama tarzında konsolidasyonlar ve/veya intralobüler
retiküler opasite ve septal kalınlaşmaların eşlik ettiği
veya etmediği buzlu cam opasiteleri ile karakterizedir(10).
Güncel Göğüs Hastalıkları Serisi 2014; 2 (3): 394-401
397
398
simlerinde periferik yerleşimli, buzlu cam/konsolide alanlar en sık izlenen bulgulardır. Buzlu
cam alanını çevreleyen konsolidasyon olarak
tanımlanan ters halo bulgusu, küçük nodüller,
septal kalınlaşma ve retiküler dansitelerde izlenebilir. En sık izlenen eozinofilik pnömoni nedenlerinden biri ilaç reaksiyonudur.
İBAH’da oluşan radyolojik görünümler:
1. Yaygın alveoler hasar: İBAH’ın en ağır formudur(10). Akciğer grafilerinde orta ve alt zonlarda
yama tarzında opasiteler mevcuttur. YÇBT’de
eksudatif fazda bilateral, yama tarzında buzlu
cam alanları saptanır. Maruziyet devam ederse fibrozise ilerler. İlaç kullanımının yanı sıra
enfeksiyon, travma, aspirasyon, inhalasyon
yaralanmaları, kollajen doku hastalıkları, akut
interstisyel pnömoniler de bu tabloya sebep
olabilir.
2. Alveoler kanama: Akciğer grafisinde bilateral
homojen/heterojen iç yapı özelliğinde opasiteler, YÇBT’de yama tarzında/yaygın buzlu cam
alanları görülür; buzlu cam alanlarına eşlik
eden intralobüler-interlobüler septal kalınlaşma ile karakterize “Arnavut kaldırımı” görünümü de izlenebilir.
3. NSIP: İlaçlara bağlı kronik interstisyel pnömonilerin tüm formları görülebilirse de en sık
NSIP izlenir. Görüntü diğer NSIP sebepleri ile
aynıdır. Akciğer grafisinde yaygın ve heterojen
iç yapı özelliğinde opasiteler gözlenir. YÇBT’de
erken dönemde yama tarzında/yaygın buzlu
cam alanları, sonrasında retiküler dansiteler,
traksiyon bronşektazileri ve bal peteği akciğerler ile seyreden fibrozis görülür(10).
4. Organize pnömoni (OP): Özellikle respiratuar
bronşioller ve alveoler duktuslar tutulur(2). Distal hava yollarında lipid yüklü makrofajlar ile
birlikte ayrıca immatür fibroblastların oluşturduğu fokal plaklar (masson cisimcikleri) saptanır(24). Akciğer grafisinde tipik olarak periferik
yerleşimli, yama tarzında pulmoner opasiteler
gözlenir. BT’de en sık bulgu asimetrik-bilateral
dağılım gösteren, üst ve alt akciğer kesimlerini eşit olarak tutan, subplevral ve peribronşial
alanlarda yerleşme eğiliminde kötü sınırlı ve
nodüler konfigürasyonlu konsolide alanlardır.
Buzlu cam alanları, tomurcuklanan ağaç görünümleri, bronşial genişlemeler, septal kalınlaşma, enfeksiyon veya neoplaziyi andıran soliter/
multipl parankimal nodül’de organize pnömonide izlenebilir(2, 13, 25, 26). OP özellikle düşük doz
MTX alan RA’lı hastalarda saptanır. Ayırımda
özellikle Pneumocystis jirovecii pnömonisi düşünülmelidir. İkisi arasında net ayırım çok zor
ise de KL-6, beta- D-glucan ve mikrobiyolojik
testler yararlı olabilir(10).
5. Eozinofilik pnömoni: Akciğer grafisinde periferik yerleşme eğilimi gösteren homojen
opasiteler mevcuttur. BT bulguları organize
pnömonidekilerine benzer. Akciğer üst-orta keGüncel Göğüs Hastalıkları Serisi 2014; 2 (3): 394-401
6. Hipersensitivite pnömonisi: BT’de yaygın bilateral buzlu cam alanları ve/veya küçük, kötü
sınırlı sentrilobüler nodüller izlenir(13, 25, 26).
7. Nonkardiyojenik pulmoner ödem: BT’de hemen
hemen bütün hastalarda bilateral yaygın alveoler veya alveoler-interstisyel infiltrasyonlar izlenir(8). Nedeni tam olarak bilinmese de artmış
alveoler kapiller membran geçirgenliğine bağlı
geliştiği düşünülmektedir.
8. Pulmoner venookluziv hastalık: Akciğer grafisinde bilateral dağınık yerleşimli ve yama tarzında infiltrasyon alanları, pulmoner arterlerde
genişleme ve Kerley-B çizgileri izlenir. BT’de
buzlu cam dansiteleri veya konsolidasyon alanları, multipl küçük parankimal nodüller, interlobüler septal kalınlaşma ve plevral sıvı gözlenir(13, 25, 26).
9. Sınıflandırılamayan paternler: Yukarıdaki hiçbir görüntüye benzemeyen görüntüler saptanabilir(10).
Tanı:
Tanı çoğu zaman benzer patolojilere sebep olan diğer
nedenlerin ekarte edilmesine dayanır. Hastalık ilaç
kullanımından sonraki birkaç gün içinde ortaya çıkabileceği gibi bazen de ilacın yıllarca kullanılmasından
sonra ortaya çıkar(7). Tanıda ayrıntılı bir öykü yanında, fizik muayene, laboratuvar tetkikleri, solunum
fonksiyon testleri ve gerektiğinde bronkoskopi, biyopsi gibi invaziv girişimler yapılmalıdır. Ayrıca ekokardiyografi, balgam gram boyama, balgam kültürü
ile vaskülit ve konnektif doku hastalıkları tanısında
gerekli immünolojik belirteçler araştırılabilir. İlaç kullananlarda yeni ve ilerleyici solunum yakınması olan
her hastada ilaç reaksiyonları muhakkak düşünülmelidir.
Hastanın en sık saptanan yakınması öksürüktür.
Semptomlar öksürük şeklinde başlayıp akut solunum
yetmezliğine kadar değişik şekillerde ortaya çıkabilir.
Yakınmalar akut, subakut veya kronik seyirli olabilir.
Hastanın ağırlığına göre klinik değişkendir. Örneğin,
anjiotensin konverting enzim inhibitörü kullananlarda öksürük ön planda iken pulmoner hemoraji olgularında hemoptiziyle birlikte dispne, hipoksemi ve akut
anemi görülür(6).
Şenyiğit A.
Tablo 2. İBAH’da tanı kriterleri.
1. İlaç kullanımının doğrulanması (dozu?, kullanım
süresi?)
2. Primer ve sekonder akciğer hastalıklarının dışlanması
3. Yeterli latent periyot
4. İlacın bırakılması ile belirtilerin düzelmesi,
yeniden verilmesi ile nüks
5. Tek ilaç kullanımı? Birlikte aldığı ilaçlar?
6. Spesifik ilaç kullanımına bağlı reaksiyon paterni?
7. İlaç reaksiyonunun kesinlik derecesi (kesin,
muhtemel mümkün)
İBAH’da bazı tanı kriterleri tanımlanmıştır (Tablo 2)(15).
Detaylı bir klinik ve ilaç anamnezi İBAH’ın tanısında
veya dışlanmasında önemlidir. Hastanın halen kullandığı veya daha önce kullandığı ilaçlar yanında göz
ve burun damlaları, vitaminler gibi reçetesiz alınabilen ilaçlar da sorgulanmalıdır. Bazı ilaçların akciğerdeki etkileri hızla gelişirken bazılarının etkileri yıllar
sonra ortaya çıkar.
Ayırıcı tanıda özellikle akciğer infeksiyonları, kardiyojenik pulmoner ödem, kollajen vasküler hastalıklar
vb. sistemik hastalıkların akciğer tutulumları yanı
sıra malignite de düşünülmelidir(9).
Yine ilacın kesilmesi ile bulguların gerilemesi de tanıda yardımcıdır(6).
Bronkoskopi ve bronkoalveoler lavaj: Pnömonitisin varlığını belirlemede lenfanjitis karsinomatoza,
vaskülit, alveoler hemoraji veya infeksiyöz ajana bağlı
pnömoni ayırımında önemlidir(27). Ancak bildirilen
vakaların % 10’undan azı histopatolojik verileri içermektedir. HP’de BAL’da lenfositoz, düşük CD4/CD8
oranı ve nadiren nötrofillerde artış saptanırken kemoterapötik ajanlara bağlı sitotoksik pnömonitiste
tipik nötrofil hakimiyeti ve EP’de ise eozinofili vardır.
Ancak nadiren de olsa BAL’da bazı tipik bulgular saptanabilir. Örneğin, amiodarona bağlı İBAH’da BAL’da
alveoler makrofajlarda köpüksü intrasitoplazmik değişiklikler saptanır. Ancak genellikle BAL bulguları
İBAH’ta tanı koydurucu değildir(5).
Transbronşial biyopsiler tanıda çoğu zaman faydalı
olmadığından açık akciğer biyopsisi yapmak gerekirse
de az sayıda ilacın spesifik histolojik reaksiyona neden olduğu unutulmamalıdır(28).
İBAH’da kullanılabilecek bazı testler de vardır. İlaç
lenfosit stimülasyon testi (İLST) ve lökosit migrasyon
testleri ile flow sitometri en sık kullanılan testlerdir.
İLST ve LMT gibi testler sadece duyarlılaşmanın olduğunu (ilaca duyarlı lenfosit varlığını) gösterir ancak
duyarlaşmanın semptomlara yol açıp açmadığını göstermez(6). İlaç provokasyon testleri (İPT) ise sadece
duyarlılığın geliştiğini göstermekte kalmayıp klinik
belirtilerinin de belirlenmesine yardımcı olmaktadır.
Ama İBAH’da İPT’nin genellikle irreversibl değişikliklere yol açabileceği, bu nedenle etik olmadığı bildirilmektedir(6, 10). Yine KL-6, SP-A, SP-D ve ADAM8 değerlerinin de İBAH’ta artabileceği bildirilmiştir(27, 29).
PET-CT’nin semptom ve radyolojik bulgular başlamadan pozitif olduğu bildirilmiştir(7).
Tedavi: İBAH’ın tedavisi öncelikle sorumlu olduğu
düşünülen ilacın kesilmesi ve semptomlara yönelik
tedavi verilmesidir. İlaç kullanımına bağlı ortaya çıkan klinik tablolar genellikle 24-48 saat sonra kaybolur. Buna karşılık daha sinsi seyreden, uzun sürede ortaya çıkan İBAH’da klinik tablonun gerilemesi
daha uzun zamanda olup tam iyileşme mümkün olmayabilir(5, 30). Genellikle İBAH’a neden olan ilaç bir
daha verilmez. Bunun bir istisnası akut promyelositik lösemide kullanılan all-trans retinoik asitin
(ATRA) neden olduğu ATRA sendromudur. Bu tablo
respiratuar distres, interstisyel pulmoner infiltrasyonlar, plöro-perikardiyal efüzyonlar, hipotansiyon
ve akut böbrek yetmezliği ile karakterizedir. Sendrom başladığında Dexametazon 2x10 mg başlanmalı, 4 gün süreyle veya semptomlar gerileyinceye
kadar devam etmelidir. ATRA sendromun başlangıcında kesilmeli ancak akut bulgular kaybolduğunda
tekrar başlanmalıdır. Ancak şiddetli solunum yetmezliği durumunda ilaç bir daha verilmez. Amiodaron gibi yağ dokusunda biriken İBAH’da ilacın 45
günlük yarılanma ömrü nedeniyle bu ilaç kesilse bile
İBAH progresif seyredebilir. Bu durumda tedaviye
40-60 mg/gün sistemik kortikosteroid (KS) eklenmeli ve 2-6 ay gibi uzun sürede tedricen azaltılarak
kesilmelidir. KS dozu azaltıldığında progresyon saptandığında tekrar kontrol sağlayıcı KS dozuna çıkılmalıdır. Yağ kütlesi fazla olan hastalarda tedavi 1 yıla
uzatılabilmektedir. Diğer İBAH olgularında da bazen
KS verilmesi gerekmektedir. Gözlemsel çalışmalarda
ağır solunum yetmezliğinin geliştiği İBAH olgularında KS tedavisinin hızlı klinik iyileşme sağladığı bildirilmiştir. Ayrıca İBAH başlangıcı akut veya subakut
olan vakalarda (istirahatte dispne varlığı, oksijen
satürasyonunun % 90’ın altına düşmesi veya bazal
değere göre 4 birim azalması veya klinik tabloda kötüleşme durumu) sistemik KS önerilmektedir. Özellikle akciğer biyopsisi alınıp NSIP, organize pnömoni
veya eozinofilik pnömoni saptanan olgularda –ki
bunlarda klinik genellikle akut veya subakut seyirlidir- KS tedavisine daha iyi yanıt alınır. Dolayısıyla
Güncel Göğüs Hastalıkları Serisi 2014; 2 (3): 394-401
399
400
İlaçlarla İlişkili İnterstisyel Akciğer Hastalıkları / Drug-Induced Interstitial Pulmonary Diseases
sorumlu ilaç kesildiğinde klinik tablosu düzelen veya
stabil seyreden olgulara KS verilmemeli, buna rağmen kliniği düzelmeyen veya daha da kötüleşen hastalarda sistemik KS tedavisi hemen başlanmalıdır.
KS dozu genellikle 40-60 mg/gün prednizolon dozu
şeklinde olmasına karşın (daha sonra yanıt alınanlarda aşamalı olarak doz azaltılarak 1-2 ay içinde kesilir) mekanik ventilasyon gerektiren ağır solunum
yetmezliği olgularında 3 gün süreyle 1 gr/gün dozunda verilmelidir. İleri derecede pulmoner fibrozis
gelişen vakalarda KS’ler progresyonu önlemekle beraber ciddi komplikasyonlara yol açabilmektedir(30).
Prognoz: İlacın akciğerlerde oluşturduğu hasara bağlı
olarak değişir. Fibrozis oluşturan ilaçlar bazen prognozu belirlemede primer hastalıktan daha fazla rol
oynar. Yine bazı İBAH’lılarda mortalite oranı yüksektir. Örneğin, akut amiodaron toksisitesinde mortalite
%40-50 civarındadır. Yine bir seride MTX’e bağlı mortalite % 15 civarında bildirilmiştir(5).
Sonuç: İBAH klinik ve radyolojik olarak geniş bir yelpazeye sahiptir. Bulguların hiçbiri veya herhangi bir
patern tek bir ilaç için spesifik değildir. Hastalık farklı antitelerle klinisyenin karşısına çıkabilir. Bir ilacın
bazen birden fazla paternle karakterize yan İBAH
oluşturabileceği unutulmamalıdır. Ancak İBAH tanısı
olup bazen ölümcül seyreden tablolar oluşturabildiğinden klinisyenin ilaç kullanan ve yukarıda bahsedilen paternlere sahip olgularda dikkatli olması gerekir.
KAYNAKLAR
1.
Popper HH. Interstitial lung diseases—can pathologists
arrive at an etiology-based diagnosis? A critical update.
Virchows Arch 2013; 462: 1-26.
2.
Erasmus JJ. Drug-induced lung injury. Seminars in Roentgenology, 2002; 37: 72-81.
3.
İlvan A. İlaçlara bağlı akciğer hastalıklarına genel bakış
(Tanım, tarihçe, epidemiyoloji, risk faktörleri). Türkiye
Klinikleri J Pulm Med-Special Tropics 2013; 6: 1-4.
4.
Amar RK, Jick SS, Rosenderg D, et al. Drug/radiation-induced interstitial lung disease in the United Kingdom general population: Incidence, all-cause mortalityand characteristics at diagnosis. Respirology 2012; 17:
861-8.
5.
Schwaiblmair M, Behr W, Haeckel T, et al.Drug Induced
Interstitial Lung Disease. The Open Respiratory Medicine Journal 2012; 6: 63-74.
6.
Erel F, Sarıoğlu N. İlaca bağlı akciğer hastalıklarında
klinik, laboratur bulguları ve tanısal yöntemler. Türkiye
Klinikleri J Pulm Med-Special Tropics 2013; 6: 66-70.
Güncel Göğüs Hastalıkları Serisi 2014; 2 (3): 394-401
7.
Matsuno O. Drug-induced interstitial lung disease: mechanisms and best diagnostic approaches. Respiratory
Research 2012, 13: 39.
8.
Özgür ES. İlaçlara bağlı hastalık yan etki hastalık paternleri. Türkiye Klinikleri J Pulm Med-Special Tropics
2013; 6: 13-9
9.
Batur Ş, Öz B. İlaçlara bağlı akciğer hastalıkları: Patogenez, patoloji. Türkiye Klinikleri J Pulm Med-Special Tropics 2013; 6: 5-12.
10. Sakai F, Johkoh T Kusumoto M, et al. Drug-induced interstitial lung disease in molecular targeted therapies: high-resolution CT findings. Int J Clin Oncol 2012;17: 542-50.
11. Flieder D, Travis W. Pathologic characteristics of drug-induced lung disease. Clin Chest Med 2004; 25: 37-45.
12. Stoclin A, Delbos F, Dauriat G, et al. Transfusion related acute lung injury after intravenour immunoglobulin
treatment in along transplant recipient. Vox Sang 2013;
104: 175-8.
13. Apaydın FD. İlaçlara bağlı akciğer hastalıklarında radyoloji. Türkiye Klinikleri J Pulm Med-Special Tropics
2013;6(2):60-5.
14. Camus P, Foucher P, Bonniaud PH, et al. Drug-induced
infiltrative lung disease. Eur Respir J 2001; 32: 93-100.
15. Matsumo O. Durg induced interstitial lung disease:mechanisms and best diagnostic approaches. Respir Res
2012; 13: 39.
16. Myers JL, Katzenstein AL. Beyond a consensus for idiopathic interstitial pneumonias: progress and controversies. Histopathology 2009; 54: 90-103.
17. Schwarz MI, Fontenot AP. Drug-induced diffuse alveolar
hemorrhage syndromes and vasculitis. Clin Chest Med
2004; 25: 133-40.
18. Conen D, Leuppi J, Bubendorf L, et al. Montelukast an
Churgg Strauss syndrome. Swiss Med Wkly 2004; 134:
377-80.
19. Montani D, Seferian A, Savale L. Drug-induced pulmonary arterial hypertension: a recent outbreak. Eur Respir Rev 2013; 22: 244–50.
20. Seferian A, Chaumais MC, Savale L, et al. Drugs induced
pulmonary arterial hypertension. Presse Med 2013; 42:
303–10.
21. Galie N, Hoeper MM, Humbert M, et al. Guidelines for
the diagnosis and treatment of pulmonary hypertension.
Eur Respir J 2009; 34: 1219–63.
22. Peacock A. Pulmonary hypertension. Eur Respir Rev
2013; 22: 20-5.
23. Fabien M, Andrew HL. Drug-induced pulmonary disease. In: Mason RJ, Broaddus VC, eds. Masson:Murray
and Nadel’s Textbook of Respiratory Medicine. 5th ed.
Philadelphia: Saunders;2010. P: 1690-719.
Şenyiğit A.
24. Epler GR, Colby TV, McLoud TC, et al. Bronchiolitis ohliterans organizing pneumonia. N Engl J Med 1985; 312:
152-8.
25. Erasmus JJ, McAdams HP, Rossi SE. High-resolution
CT of drug-induced lung disease. Radiol Clin North Am
2002; 40: 61-72.
28. Romagnoli M, Bgliazzi C, Casoni G, et al. The role of
transbronchial lung biopsy for the diagnosis of diffuse
drug-induced lung disease: a case series of 44 patients.
Sarcoidosis Vasc Diffuse Lung Dis 2008; 25: 36-45.
26. Schwaiblmair M, Behr W, Haeckel T, Märkl B, Foerg W,
Berghaus T, et al. Drug induced interstitial lung disease.
Open Respir Med J 2012; 6: 63-74.
29. Matsuno O, Ono E, Ueno T, et al. Increased serum
ADAM8 concentration in patients with drug-induced
eosinophilic pneumonia -ADAM8 expression depends
on the allergen route of entry. Respir Med 2010, 104:
34–39.
27. Inomata S, Takahashi H, Nagata M, et al. Acute lung
injury as an adverse event of gefitinib. Anticancer Drugs
2004, 15: 461–7.
30. Özgür ES, İlvan A. İlaçlara bağlı akciğer hastalıklarında
tedavi ve prognoz. Türkiye Klinikleri J Pulm Med-Special Tropics 2013; 6: 71-4.
Güncel Göğüs Hastalıkları Serisi 2014; 2 (3): 394-401
401