MADDENİN YAPISI VE ATOM
Madde, atom adı verilen taneciklerden oluşur.Atom maddenin yapı taşıdır.
Atomun yapısında proton, nötron ve elektron bulunur.
Proton ve nötron atomun çekirdeğinde yer alır. Elektron ise çekirdek etrafında
dolanır.
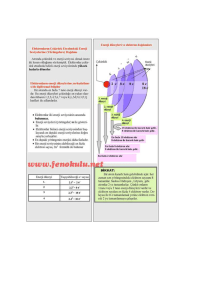
Atomun yapısı ve gösterimi
Atomu oluşturan tanecikler belli başlı özellikleri vardır.
Proton: Atomun çekirdeğinde bulunur. (+) yüklü bir parçacıktır. Kütlesi 1 akb’dir.
Nötron: Atomun çekirdeğinde bulunur. Kütlesi hemen hemen protona eşittir. Elektrik yükü taşımaz.Yani
yüksüz bir parçacıktır.
Elektron: Atomun çevresinde çok büyük hızla dönen hareketli bir parçacıktır. Elektronlar çekirdek etrafında
farklı enerji seviyelerinde dolanır.
Atom çekirdeğinin çapı, atom çapının 100 binde biri kadardır. Atom çekirdeğinde yüklü olarak sadece
protonlar bulunduğu için, atomun çekirdek yükü daima (+) artıdır.
1 Karbon atomunun kütlesinin 1/12’sine, 1 atomik kütle birimi adı verilmiştir. Atomik kütle birimi akb ile
gösterilir.
1 Karbon atomu = 12 akb’dir.
Kimyasal hesaplamalarda atomların kütleleri gram cinsinden değil, akb cinsinden alınır.
Atom numarası: Bir element atomunun çekirdeğinde bulunan proton sayılarının toplamına, atom numarası
adı verilir. Atom numarası Z ile gösterilir.
Z=p
Nötr karbon atomunda (+) ve (–) yük sayısı eşittir.
Kütle numarası: Bir atomun çekirdeğindeki proton ve nötron
sayılarının toplamı, o atomun kütle numarasını verir. Kütle numarası
A ile gösterilir.
Kütle numarası = Proton sayısı + Nötron sayısı
A=p+n
Nötr ve Yüklü Atom: Bir atomdaki proton ve elektron sayıları
birbirine eşitse
bu atoma nötr atom denir. Nötr atomda (+) ve (–) yükler birbirine
eşittir.
Örneğin nötr karbon atomunda 6 proton 6 elektron vardır. Nötr atomda,
p = e’dir.
Atomlar elektron alıp verebilirler. Ancak çekirdekte bulunan proton ve nötronu alıp veremezler.
ÖRNEK: Nötr bir magnezyum atomunda proton sayısı 12, nötron sayısı 13’tür.
Bu atomun;
a. Elektron sayısı nedir?
b. Kütle numarası nedir?
(–) yüklü atom
Eğer bir atom dışarıdan elektron alırsa, (–) yük sayısı (+) yük sayısından
fazla olur. Bu durumda atom (–) yüklü olur.
Örneğin nötr flüor atomunun 9 elektronu, 9 protonu vardır.
Flüor atomu 1e– alınca 10 elektronlu ve (–) yüklü olur.
(–) yüklü flüorun (–) yük sayısı
(+) yüklü atom (+) yük sayısından fazladır.
Eğer bir atom bir elektronunu kaybederse, (+)
yük sayısı (–) yük sayısından fazla olur. Bu durumda
atom (+) yüklü olur.
Örneğin nötr lityum atomunun 3 protonu 3 elektronu
vardır. Lityum 1e– verirse 2 elektronlu ve (+)
yüklü olur.
(+) yüklü lityumun (+) yük sayısı (–) yük sayısından fazladır.
Elementlerin Sembollerle Gösterilmesi
Kimyasal hesaplamalarda maddelerin Lâtince isimleriyle işlem yapmak zordur. Bunun yerine elementlerin
Lâtince isimlerinin kısaltmalarından oluşan semboller kullanılır.
Element sembollerinde ilk harf her zaman büyük, varsa diğerleri daima küçük yazılır.
Örneğin;
Hidrojen H,
Helyum He,
Karbon C
Kalsiyum Ca,
Bor B,
Berilyum Be
Element sembolünün sol üst köşesine atomun kütle numarası, sol alt köşesine ise atom numarası yazılır.
Kütle numarası
X=
Atom numarası
A
p+n
X=
X
Z
p
ÖRNEK:56Aşağıda verilen nötr hâldeki atomların atom numarası (Z), kütle numarası (A), nötron (n) ve
elektron (e) sayılarını belirtiniz.
a. 167 N
b. 126 C
c. 73 Li
ÖRNEK: I. 157 X
II. 189 X
III. 1910 X
17
Yukarıdakilerden hangilerinin nötron sayısı, 8 O elementinin nötron sayısıyla aynıdır?
A) Yalnız I
B) Yalnız II
C) I, II
D) II, III
Elektron Dağılımı
Elektronlar çekirdek çevresinde belli enerji seviyelerinde ve belli sayılarda dolanır. Enerji seviyeleri
çekirdekten dışa doğru, 1. seviye, 2. seviye, 3. seviye şeklinde sıralanır. Bazen enerji seviyeleri, K, L,M, N...
harfleriyle de gösterilir.
1. seviyede en fazla 2 elektron bulunur.
2. seviyede en fazla 8 elektron bulunur.
Bir enerji seviyesinde bulunabilecek en fazla elektron sayısı, 2 n 2 bağıntısı ile hesaplanır. (n, enerji seviyesini
gösterir.)
Atomun en dış enerji seviyesinde en fazla 8 elektron bulunabilir. En dış enerji seviyesinde 8 elektron
bulunduran elementlere soy gazlar ya da asal gazlar adı verilir. Bunun tek istisnası helyumdur. Helyum
elementi soy gaz olduğu hâlde 2 elektronu vardır.
Bazı atomlar ve enerji seviyelerine göre elektronların dağılımı;
2He )
3Li ) )
2
21
8O ) )
10Ne ) )
26
28
12Mg ) ) )
16S ) ) )
282
286
Örnek:
İlk iki enerji seviyesi dolu olan bir atomun toplam elektron sayısı nedir?
Örnek:
Atom numarası 13 olan nötr bir atomun elektron dağılımı nasıl olur?
Örnek:
18X atomunun elektron dağılımı nasıldır?
Örnek:
Üçüncü enerji seviyesinde 2 elektron bulunan bir atomun atom numarası kaçtır?
A)6
B)10
C) 12
D) 26