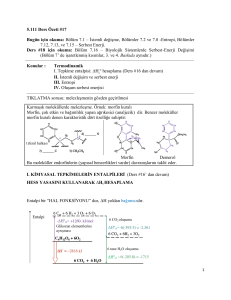
KİMYASAL
REAKSİYONLARLA İLGİLİ
HESAPLAMALAR
1.
2.
3.
4.
5.
6.
7.
8.
DENKLEMLİ BASİT MİKTAR GEÇİŞLERİ
ARDIŞIK REAKSİYONLARDA MİKTAR GEÇİŞLERİ
AŞIRI MADDE PROBLEMLERİ
KİMYASAL REAKSİYONLARIN VERİMİ
ARI OLMAYAN MADDE İÇEREN PROBLEMLER
DENKLEMLİ KABA FORMÜL VE MOLEKÜL FORMÜLÜ
PROBLEMLERİ
KİMYASAL TEPKİMELERDEN YARARLANILARAK MOL
KÜTLESİ HESABI BULMA PROBLEMLERİ
KİMYASAL REAKSİYON OLAN KARIŞIM PROBLEMLERİ
1.DENKLEMLİ BASİT MİKTAR
GEÇİŞLERİ
TANIM:
Bir kimyasal tepkimede maddelerden
birinin hacmi, kütlesi veya tanecik
sayısı verilir ve tepkimedeki başka bir
maddenin kütlesi, hacmi veya
tanecik sayısı istenir.
YÖNTEM:
Verilen nicelik mole
çevrilir.
İstenilen niceliği mol
sayısı tepkime
denklemi yardımıyla
hesaplanır
İstenilen molü
istenilen birime
çevrilir
Kütle
m
(m)
Hacim
mol
mol
V
(v)
İstenen
madde
Verilen
madde
Tanecik
N
(n)
1.adım
2.adım
3.adım
2.ARDIŞIK REAKSİYONLARDA MİKTAR
GEÇİŞLERİ
Tanım:
Bir maddeyi elde etmek için birden
fazla art arda gerçekleşen
reaksiyonlar dizisine ardışık
reaksiyonlar denir.
Yöntem:
Denklemlerdeki giren ve çıkan (aynı
maddenin) katsayılarının eşitlenmesi için
gereli katsayılarla bütün denklem çarpılır.
Daha sonra daha kolay görmek için taraf
tarafa toplanabilir.
1.YOL
x4
x2
x1
A+B
2D + E
4G + H
C+D
F + 2G
E+Y
4A + 4B + E + H
4C + 2D + 2F + Y
4mol 4mol 1mol 1mol
4mol 2mol 2mol 1mol
3.AŞIRI MADDE PROBLEMLERİ
Tanım:
Bu problemde reaksiyona
giren maddelerin ikisinin de
miktarı verilir. Reaksiyona
giren maddelerden biri
tamamen tükenirken diğerinin
tamamı reaksiyona girmez, bir
kısmı artar. Artan bu miktar
aşırıdır.
Yöntem:
Tamamen kullanılan
madde esas alınarak
istenilenin
hesaplanması gerekir.
Tepkime
Verilen miktarlar:
Tepkimeye giren:
Tepkime sonucu:
2A +
4mol
4mol
-----
A maddesi için;
B maddesi için;
Verilen: 4mol
Tepkiyen: 4mol
Artan : yok
verilen: 3mol
tepkiyen: 2mol
artan: 1mol
B
3C
3mol
---2mol 6mol
1mol 6mol
C maddesi için
verilen: ---reaksiyon sonucu
oluşan : 6mol
4.KİMYASAL REAKSİYONLARIN
VERİMİ
Tanım :
Bir kimyasal tepkimenin teorik olarak
verimi; tepkime denklemine göre
beklenildiği ve hesaplandığı miktarda
ürün elde edilmesidir. Verilen
tepkimede aksi belirtilmezse %100
verim elde edilir, diye kabul edilir.
Yöntem :
Verilen denkleme göre verilen madde
miktarları karşılaştırılır. Oluşan madde
miktarının olması gereken madde
miktarına oranının yüzde olarak
hesaplanması bize o tepkimenin verimini
verir.
Denklem:
Veriler :
0,15mol
%100 verimde:
2A
0,4mol
3B + 3C
0,4mol
0,6mol
Oran:
0,6mol oluşması gerekirken 0,15mol oluşuyorsa
100mol “
“
x mol oluşur
x = 25
Buna göre tepkimenin verimi % 25 tir.
5.ARI OLMAYAN MADDE İÇEREN
PROBLEMLER
Tanım :
Doğada hatta
neredeyse
laboratuarlarda
bile %100 arı
madde yoktur. Bu
gibi maddelerle
yapılan
tepkimelerin
hesaplanmasına
denir.
Yöntem :
Verilen miktar ve yüzde arılıktan
ne kadar arı madde bulunduğu
hesaplanır. Denkleme göre işlem
yapılır.
1-Verilen miktar . Arılık yüzdesi / 100 = arı madde miktarı
2-Denkleştirilmiş tepkimede;
Denklemdeki miktar
Arı madde miktarı
istenen madde miktarı
X
X: istenen maddeden oluşan miktar
6-DENKLEMLİ KABA FORMÜL VE
MOLEKÜL FORMÜLÜ PROBLEMLERİ
Tanım:
Verilen
denklemlerde
belirtilmemiş
maddenin
formülünü
isteyen
problemlerdir
Yöntem:
Verilen bilgilere göre denklem
kurulur. Verilen madde miktarları en
küçük tam sayı olacak şekilde
sadeleştirilerek mol sayısına çevrilir.
Tepkimedeki atom sayısı
denkliğinden yararlanılarak formülü
bilinmeyen bileşiğin kaba formülü
bulunur.
2An +Bn
C2 3An
2A2B
2D
2n=4 n=2
D
2CAз
KİMYASAL TEPKİMELERDEN
YARARLANILARAK MOL KÜTLESİ
HESABI BULMA PROBLEMLERİ
Tanım:
Verilen tepkimelerde bazı
yasaları kullanarak miktarı
belirtilmemiş olan
maddenin mol kütlesini
bulmamızı sağlar
Yöntem:
Kimyasal tepkimede kütlenin ve atom
sayılarının korunumu ilkesinden
yaralanılarak istenilen bulunur.
A+B
8 g 4g
8+4=3+X
X = 9g
C+D
3g X
KİMYASAL REAKSİYON OLAN
KARIŞIM PROBLEMLERİ
Tanım:
En az iki
maddeden
oluşan karışım
ile ayrı bir
maddenin
ortama ilave
edilmesiyle
oluşan kimyasal
tepkimeler ve
elde edilen
sonuçlardır.
Yöntem:
İlk önce karışımda hangi
maddenin reaksiyona girdiği tespit
edilir. Ayrı ayrı denklem yazılarak
sonuç elde edilir.
Karışım
A ve B
İlave edilen
C
Reaksiyon veren
A, B, C
Denklemler:
A+C
B + 2C
1.
2.
D+E
E
Denklemler denkleştirilir.
Soruda verilenlere göre iki bilinmeyenli iki
denklem kurulur.
NOT:
BU YÖNTEMLERİN HEPSİ O KONULARIN
EN GENEL YÖNTEM ŞEKİLLERİDİR.
YÖNTEMLER HER SORUYA GÖRE
DEĞİŞEBİLİR VE ÇOĞALTILABİLİR.