SOMATİK HÜCRE KALITIMI
(epigenetik kalıtım)
Doç.Dr.Öztürk ÖZDEMİR
“Aynı organizmaya ait hücrelerarası gen
aksiyon farklılığını inceleyen genetik alt
dalı”
Ocak 2005
TEŞEKKÜR
Öğrenci
Komite
1-Ayşe Gül VURAL III
1-Mustafa ORAL
III
2-Bilgin DEMİR
III
3-Naciye AYGÜN
III
Not
87
87
86
85
GENETİK DÜZENLEMEDE – SOMATİK KALITIM EVRELERİ
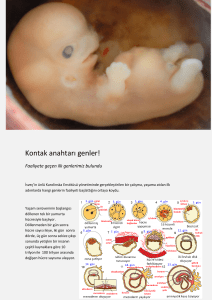
1- Yumurta hücresi düzeyinde düzenleme : Yumurta hücresinde bulunan
anterioposterior gradiyent farkı fertilizisyon öncesi yumurta hücresinden meydana
gelecek embriyonun anteriyor ve posteriyor kısmını verecek bölgeler öncelikle
belirlenmektedir. Burada sadece yumurta hücresiyle sınırlı bazı regülatör-modülatör
proteinler yumurta-polarity ve segmentasyondan sorumlu (25 adet tanımlanmıştır)
genler görev almaktadırlar.
2. Zigot evresinde düzenleme : Bu evrede yine çoğu yumurtadan orijin alan ve
döllenmeyi takiben aktive olan zigotik-effekt genler olarak bilinen; remodelling
faktörler, integrinler, transkripsiyonel faktörler ve kromatin bağlayıcı özgül
proteinler gibi düzenleyici moleküllerin görev aldıkları saptanmıştır. Bu genlerin
görevi yumurta ve sperm çekirdeklerinin kaynaşmasını sağlamak ve hücre
bölünmesi öncesi görev yapan proteinlerin bazı regülasyonunda görev alırlar.
3. Gastrulasyon-Embriyogenez evresinde düzenleme : Bu evrede görev alan en önemli
gen grubunun yine yumurta hücresine ait 8 çift oldukalı saptanan pair-rule ve 10 adet
oldukarı saptanan segment polarity genlerdir. Bu gen grubu her tür için farklı olmakla
birlikte embriyogenezin 2, 8 ve 16 hücrelik bölünme evrelerinde inaktive edilirler. Örneğin
farelerde zigot 2, koyun ve insanda 16 hücrelik embriyo olana kadar görev yapmaktadırlar.
Bu sayı türe göre değişmektedir. Zigot hücresinin maksimum 16 hücreye kadar
bölünmesinden sorumlu gen grubudur. Bu genler sadece totipotent hücrelerde görev alırlar.
4. Fetus dönemi düzenleme : Bu dönem, fetus hücrelerine ait genlerin ifade edilmesiyle
başlar. Bu dönemden sonra yumurta regülasyonu yerini fetus gen regülasyonuna terk eder.
Görev yapan genler homeotik ya da homeodometik (hox) gen ailesi olarak adlandırılır. Diğer
bir tanımla bu genler geniş bir aileden ibaret olup, yetişkin dokuların ilkin farklılaşmasından
sorumlu oldukları için homeotik seçici genler olarak adlandırılırlar. Türlerarası somatik doku
farklılaşmasından birinci dereceden bu gen grubu sorumludur. Bir dokunun normal ya da
anormal bir şekilde farklılaşması bu gen grubunun normal ve zamanında fonksiyon
yapmasına bağlıdır. İlk kez blastoderm evresinde aktive olurlar. Memelilerde 4 adet
homolog homeotik kompleks genin varlığı saptanmıştır. Homeodometik seçici genleri
meydana getiren homeodomain zincir genleri evrim süresince korunan ve en az varyasyon
gösteren genlerdir. Herbiri 60 aa uzunluğunda protein sentezinden sorumlu 650.000 bç
uzunluğunda regülatör alt birimlerinden ibaret genlerdir. Genlerin regülatör alt birimlerini
meydana getiren diziler, segmentasyonel ve yumurta -polarity gen ürünlerine özgül bağlantı
bölgeler içerirler. Vücudun segmentasyonunda spesifik görev yapan bu gen grubudur.
Moleküler mekanizmaları kesin olarak bilinmemekle birlikte regülatör alt birimleri
aracılığıyla aktive ve inhibe edildikleri sanılmaktadır.
5-YETİŞKİN (ADULT) DÖNEM DÜZENLEME
1- Housekeeping genler
2- Doku spesifik genler
3- Alel spesifik genler
4- Diğer (ekspresyon farklılığı gösteren
genler, onkogenler, TS genler vb)
EPİGENETİKTE (SOMATİK KALITIM) ETKİLİ
MEKANİZMALAR
I- DNA METİLASYONU
II- FOSFORİLASYON
III- ASETİLASYON
IV- UBİQUTİNASYON
V- HIGH MOBIL NON-HISTON PROTEİNLER
DNA METİLASYONU
•
•
•
•
•
•
•
•
- DNA replikasyonunun başlatılması
- DNA transkripsiyonunun başlatılması
- DNA tamiri
- Mutagenezis
- İkili sarmal DNA stabilitesinin sağlanması
- Lokal mutasyon oranının artırılması
- Nükleer parçalanmanın engellenmesi
- Kromozom paketlenmesi
• - Hücre farklılaşması
•
- X-kromozom inaktivasyonu
• - Gen ekspresyonu
• - Yaşlanma
•
•
•
- Tümör baskılayıcı gen inaktivasyonu ve proto-onkogen aktivasyonu aracılı
onkogenezis
- Genomun aktif gen ya da kondanse bölgeler şeklinde yapılanması ve
yerleşimi
- Apoptozis
DNA METİLASYONU
•
•
•
•
•
Post-replikatif bir mekanizmadır
DNA düzeyinde yapılan modifikasyonla karakterize epigenetik mekanizmadır
DNA metiltransferaz görev alır
İnsanda % 90 oranında metillenenz nükleotidler mCpG dinükleotididir.
DNA metilasyon oranı açısından;
–
–
–
–
Ametile DNA (Ökromatik DNA, Housekeeping genler)
Hipometile DNA (Fakültatif heterokromatik DNA, Pseudogenler, inaktif X)
Undermetile DNA (bazı onkogenler)
Metile DNA (Heterokromatik DNA, İnterkalar heterokromatik DNA,
protoonkogenler)
– Hipermetile DNA (Sentromerik DNA, İnaktik Junk DNA)
•
•
mC, 5-metilsitozin yada episitozin olarak adlandırılır
Semikonservatif kalıtılır
ELEMANLARI
-
Metil vericisi SAM (S adenozil methionin)
Substrat template DNA
Enzim DNA Metil transferaz
SAM metil grubunu kaybedince SAH (S adenozin
homosistein)’e dönüşür.
- Ökaryot ve prokaryot hücrelerin herikisinde en yaygın
metillenen baz sitozin ( C) dir.
- Prokaryotlarda CCGG dizilerindeki ilk sitozin,
ökaryotlarda ise CpG dinükleotidlerdeki ilk sitozin en
yaygın metillenen bazdır.
- DNA yapısından metil grubunun koparılmasında görev
alan enzim DNA Mtaz dır.
METİLASYONUN ONKOGENEZDE
ÖNEMİ
• Bütün onkogenler ökaryotik hücrelerde öncelikle DNA
düzeyinde modifiye edilerek inaktive dilir
• DNA metisyonu görev alır
• Onkogenler hipermetile durumda inaktif durumdadırlar
• Onkogen hipermetile ya /yada metillenerek inaktive edilir,
protoonkogene dönüştürülür.
• Fosforilasyon, ubiqutinasyon, yüksek mobiliteye sahip non-histon
proteinlerin varlığı ve asetilasyon ise nükleoproteinler düzeyinde
(histon –non-histon) yapılan epigenetik modifikasyon mekanizmaları
olup gen ekspresyonu farklılaşmasında rol alan en önemli
mekanizmalardır.
• Tümör supressör (20 adet) genler ÖR : p53 DNA hipermetilasyonu
sonucu ekspresiyonel olarak inaktive edilir, hücre onkogeneze girer.
• Bu genler normal hücrelerde aktif genlerdir, inaktif durumda hücrede
kansere neden olurlar. Genlerin inaktivasyonları da DNA
hipermetilasyonu ile olur.
Alternative
models for CpG
methylation in
cancer
HÜCRE ÖLÜM
MEKANİZMALARI
Apoptozis
Nekrozis
Sitotoksisite
Tablo I. Apoptozda etkili basamaklara genel bakış.
Uyarıcılar
Upstream Caspase Aktivasyonu
Mitokondriyal membranında potansiyal kayıp
ROS üretiminde artış
Kromatin condensasyonu
Asidifikasyon
Fosfatidilserin translokasyonu
Downstream Caspase Aktivasyonu
Hücre membran permeabilitesinde artış
DNA fregmantasyonu
Apoptatik body oluşumları
Fagositozis (ölüm)
APOPTOZİS
Kontrol edilen – proğramlı hücre ölümüdür
Fizyolojik bir process olup istenmeyen yada
yararsız hücrelerin ölümünden sorumlu
mekanizmadır.
yüksek canlılarda özellikle gelişme ve doku
farklılaşması dönemlerinde görev yapar”fiyolojik
apoptozis”.
Farklılaşmasını tamamlamış doku –hücrelerde
meydana gelirse “patolojik apoptozis “adlandırılır.
APOPTOZİS EVRELERİ
Membran blebbing
Kromatin(çekirdek)kompertmentalizasyonu
Sitoplazma kondensasyonu
DNA fragmentasyonu
Mitokondri membran yapı bozukluğu
Apoptotik body oluşumu
Fagositozis
APOPTOZİS
1- Özel grup hücrelerde meydana gelir
2- Hormonal değişim ve büyüme faktörlerinin
yokluğu gibi fizyolojik sitimülasyona bağlı gelişir
3- Apoptotik body ler makrofaj ve diğer komşu
hücrelerce fagosite edilir
4- İnflamasyonel yanıt görülmez.
APOPTOZİS ÖZELLİKLERİ
Enzimatik basamakları düzenlenebilen
mekanizmadır
37 C’de meydana gelen ATP bağımlı bir
mekanizmadır.
Agaroz elektroforezde ladder yapı gösterir
Mitokondri membran değişiklikleri
mevcuttur:
- Fosfatidilserin translokasyonu
-AIF ve sitokrom C sekresyonu
APOPTOZİS GÖREVLERİ
Embriyogenezis
Doku homeostazisi
İmmün tolerans
Sinir hücrelerinin gelişimi
Normal hücre gelişimi
Endokrin bağımlı doku atrofisi
Primer gonad - seks gelişimi
Metamorfozis
APOPTOZİS TETİK
ÇEKİCİLERİ
Hücre yüzey reseptör ölümleri (CD95, APO 1, Fas
ve ras aktivasyonu)
Fosfatidilserin translokasyonu, extrinsik matiriks
değişimi
11 farklı intrasellüler Cystein proteaz enzimlerin
sitozole salınımı (Caspase 8 ve 9)
AIF salınımı
Ca ve Mg bağımlı oligonükleozomal endonükleaz
aktivasyonu
NEKROZİS
Kazaen hücre ölümüdür
Patolojik bir process tir
İstenmeyen hücre ölüm mekanizmasıdır
Hücrenin çok ciddi bir fiziksel yada kimyasal
ajanlara maruz kaldığı durumda kendi siteği
dışında gelişen bir ölüm mekanizmasıdır.
İnflamasyonel yanıt mevcut (yangı)
Makrofajlarla fagositozis görülür
Homeostazis yokluğu en önemli etkendir
NEKROZİS ÖZELLİKLERİ
Homeostazis regülasyonu ortadan kalkmıştır
Enrji gereksinimi yoktur
Hücre özgüllüğü yoktur
“Smear DNA” yapısına sahiptir
+ 4 C’de meydana gelir
Hücre ölümünün son basamağında rastgele DNA parçalanması görülür
Vesikül oluşumu görülmez
Smoot mitokondri ve hücre membran yapısı
Sitoplazma vemitokondri membran yapısında
irreversible swelling (şişme)
Total hücre ölümü ile sonlanır
NEKROZİS ETKENLERİ
-
metabolik zehirlenmeler
ischemia
hipoksi
Hipertermi
litik viruslar
complemen ataklar
homeostasis gerilemesi(hücreye su ve iyon
geçişinde düzensizlikler)
SİTOTOKSİSİTE
İlaç
Kozmetikler
Çeşitli yiyecekler
Ağır kimyasal bileşenler gibi toksik etkenlerin
neden olduğu hücre ölüm mekanizmasıdır.
Patolojik bir mekanizmadır
T-hücreler aracılı fagositozis bu mekanizmaya
dahil edilir
MHC reaksiyonların tamamı sitototoksisite ile
ölümdür
Apoptotik body fagositozu yine bir sitotoksisite
ölümdür olarak kabül görür.
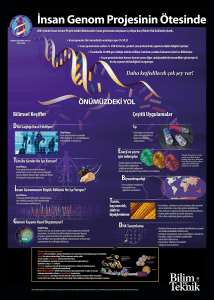
Dr Alan Wolffe (1999) “Epigenetics is heritable changes in gene
expression that occur without a change in DNA sequence”
Epigenetics is ingenious system to selectively utilize genome information,
through activating or inactivating functional genes.
Identified epigenetic processes involved in human disease:
1. DNA methylation
2. imprinting
3. histone modifications
Each of these processes influences chromatin structure and
Thus regulates gene expression and DNA methylation, replication,
recombination and repair.
Ac -acetylated histones; mC-methylated Cytosine
HDAC -histone deacetylases: Pol II- RNA polymerase II
GTF- general transcription factors
HAT -histone acetyltransferases;
MBD -methylated DNA binding domain
1. System of DNA methylation
*CpG islands: >200 bp stretches of DNA that have a significantly higher
concentration of 5’-CpG;3’ dinucleotides than the bulk of the genome
*Cytosine resudue in complementary 3’-GpC-5’ that makes a basepair, is
also methylated symmetrically, and these two methyl groups show a
three-dimentional structure prominent in the major groove of the dsDNA
*50-60% of human genes have CpG islands in front of and covering core
promotor and transcription start site
*70-80% of CpGs in the genome is methylated
*CpG islands in front of genes are mostly unmethylated
*exceptions: imprinted genes and X-linked genes
*CpG island are divided into several classes:
(1) methylated on both alleles in all tissues located in high CG isochores
(2) differentially methylated and located in low CG (<0.5) isochores
*genomic methylation pattern is stable and heritable
*genome-wide methylation patterns are reprogrammed in mammalian
germ cells and in pre-implantation embryos
Mammalian methyltransferases:
1.DNMT1 - maintenance DNA methyltransferase
*methylates hemi-methylated DNA providing methylation pattern to the
newly replicated daugther strand, based on parent strand
*represses transcription in complex with histone deacetylases
2. DNMT3a, DNMT3b - de novo methylases
*add a methyl group to unmethylated CpG base pairs, resulting in
creation of a new hemi-methylated and then fully methylated CpG
*de novo methylation is implicated in cell growth and differentation,
and in altered methylation in tumorigenesis.
DNMT3b - mutated (common splice variant) in patients with ICF
syndrome (immunodeficiency in association with centromere instability
of chromosome 1, 9, 16, and facial anomalies): hypomethylation of
pericentromeric satellite sequences
Methyl-CpG binding proteins: MeCP2, MBD1-4
*Methylated DNA is replicated later than actively transcribed DNA
*Monoallelically expressed genes (imprinted) have coordinated
replication timing along human chromosomes
Replicated (active) genes
Non-replicated (silenced) genes
FISH analysis with imprinted gene pairs selected from one chromosome
2. Histone modifications
The amino termini of histones contain a diversity of posttranslational
modifications. The most promonent of them are acetylation and methylation
of Lysine (K) residues in the highly concerved H3 and H4
174 bp of
Histone tails
Histone fold domain
Methyl
modifications
Acetyl
modifications
ACETYLATION
TRANSCRIPTION
Many of trans-acting factors required for HT assembly are
either enzymes that directly modify histones or factors binding
to histones
*e.g. SIR (silent information regulator) genes in yeast - Sir 2 is a NADdependent histone deacetylase; Sir3&4 bind to deacetylated histone tails
*in mammals, Drosophila and yeast methylation of H3 lysine 9 correlates
with heterochromatin assembly. This residue is methylated by concerved
methyltransferase SUV39H1 in human, Su(var)3-9 in drosophila and Clr4
in fission yeast
*Swi6 (yeast) and HP1 (human, Drosophila) bind to Lys 9 methylated H3
tails
Histone methylation/HP1-binding cycle is an ancient
mechanism for propagating epigenetic states.
CpG methylation/histone deacetylase binding cycle in evidently
added later.
How are heterochromatin complexes targeted to a specific chromosomal
domain? Evidence suggests a role for repetitive DNA elements and noncoding RNAs in regional targeting of HT complexes.
S. cerevisiae
S. pombe
Small HT
RNAs
RNA interference (RNAi) pathway
1.Required for HT formation and H3 Lys9 methylation in S. pombe :
Argonaute (ago1), member of PAZ/Piwi family
Dicer (dcr1), RNaseIII-like protein
RNA-dependent RNA polymerase (rdp1)
2. Centromeric repeat sequences that are transcribed at low levels
and produce ds RNA are sufficient to recruit HT at an ectopic site
3. Small HT RNAs provide specificity for targeting histone
modifying activities and epigenetic modification of the genome
through homology recognition
4. The role of RNAi in epigenetic gene silencing appears to be
concerved among diverse species
1.
2.
3.
RISC- RNA induced silencing complex
Model for formation
of silenced chromatin
domains
E-histone-modifying
Enzyme
SF- silencing factor
BE- boundary
element
Deacetylation and
methylation of H3
Lys9 are followed by
deacetylation of H3
Lys 14 and create a
binding site for Swi6
silencing factor
H3 Lys 9 acetylation+ H3 Lys4
methylation= STOP heterochromatin
Ac -acetylated histones H3 Lys9
CpG-Me -methylated Cytosine
HDAC -histone deacetylases
DNMT -DNA methyltransferase
HMT-histone methyltransferase
MBD -methylated DNA binding
domain
HDAC deacetylates lysine
residues as the prerequisite for
methylation
HP1 protein recognizes MeK9,
binds also HMT and
heterchromatin can spread
3. Chromatin remodeling
The positioning of histones along DNA is mediated by ATP-dependent nucleosome
- remodeling complexes that use the energy of ATP hydrolysis to noncovalently
reposition histone octamers and generate nucleosome free or dense chromatin.
Genes
Mechanims
where
involved
Diseases
SIOD - Schimle immuno-osseous dysplasia
COFS - cerebro-oculo-facio-skeletal syndrome
CBS - Cockayne syndrome type B
RTS - Rubinstein Taybi syndrome
Chromatin remodelling disorders:
1.ATRX, SNF2-family helicase (a-thalassemia X-linked mental
retardation) mutations:
Causes several mental retardation disorders, facial, skeletal, an
urigenital abnormalities, a -thalassemia and microcephaly
ATRX protein resides predominantly in repetitive DNA, ribosomal
gene clusters, pericentromeric heterochromatin.
In ATRX cells, the ribosomal DNA repeats are hypomethylated.
3. SMARCAL1 (SWI/SNF-related matrix-associated, actindependent regulator of chromatin, subfamily A-like protein 1):
Schimke immuno-osseous dysplasia characterized by T-cell
immunodeficiency, renal failure, hypothyroidism, bone-marrow
failure etc.
SMARCAL1 probably regulates a subset of genes necessary for
cellular proliferation.
2. ERCC6 gene (excision repair cross-complementing rodent
repair deficiency, compelentation group 6):
(a) COFS (cerebro-oculo-facio-skeletal) syndrome: failure of
multiple systems and premature death (b) Cockayne syndrome:
UV-sensitivity, dwarfism, skeletal abnormalities, mental
retardation etc.
Both cellular phenotypes include increased sensitivity to
oxydative and UV-induced DNA-damage and failure to recover
RNA synthesis after UV irradiation
ERCC6 plays key role in transcription coupled DNA repair,
presumably opens the chromatin allowing access of the DNA
repair apparatus to the DNA
MeCP - Methyl-CpG binding protein
IGF2 - insulin-like growth factor 2
Epigenetics and human disease
CBP - CREB binding protein, coactivator of transcription
Mi2 - nucleosome remodelling histone
deacetylase
How is the heterochromatic state inherited?
*During DNA replication, histones H3 and H4 are randomly distributed to
sister chromatides.
*modified parental histones and assambled heterochromatin proteins
(Swi6/HP1 or Sir 3) can serve as “molecular bookmarks” to imprint the
parental histone-modification pattern onto newly assambled nucleosomes.
4. Cancer epigenetics
Feinberg and Vogelstein (1983): loss of DNA
methylation in cancer cells compared to normal tissues
Hypomethylation and gene activity:
1. Hypomethylation can lead to gene activation (e.g. HRAS, which is
normally expressed only in testis)
*Overexpression of:
cyclin D2 in gastric carcinoma
MN/CA9 in renal-cell carcinoma
S100A4 metastasis associated gene in colon-cancer
HPV16 in cervical cancer
2. A cellular ‘methylator phenotype’ has been linked to mismatch
repair (Lengauer et al)
*Hypermethylation of the mismatch-repair gene MLH1 is commonly
found in mismatch-repair-defective tumors
3. Hypomethylation in cancer is related to chromosomal instability
*Frequent unbalanced chromosomal translocations with breakpoints
in pericentromeric satellite sequences (otherwise highly methylated)
4. Hypomethylation is a mechanism of drug, toxin and viral effects in
cancer
*MDR1, multidrug resistance gene correlates with increased
expression and drug resistance in acute myelogenous leukemia
*Cadmium inhibits DNA methyltransferase activity and leads to
acute hypomethylation, which is followed by hypermethylation of
dna after chronic exposure to this “epigenic’ carcinogen
*Arsenic induces Ras hypomethylation in mice
*cervical cancer latency is caused by hypermethylation of HPV16
genome
Hypermethylation and cancer
Promotor CpG hypermethylation of tumor supressor genes:
Retinoblastoma gene RB
Cyclin-dependent kinase inhibitor (INK4A,p16, CDKN2A)
Mismatch repair gene MLH1
Von Hippel-Lindau (VHL) tumour supressor
E-cadherin
Is the INITIAL SILENCING HYPERMETHYLATION?
Or is HYPERPEMTHYLATION a consequence?
Probably it is part of “programmed” silencing, but is not per
se responsible for inactivation of a gene
Loss of imprinting in cancer
BWS is fetal overgrowth disorder due
to deregulation of imprinted genes at
11p15: paternally expressed IGF2,
KCnQ1OT1 & maternally expressed
H19, CDKN1C, KNCQ1
Wilms tumour: hypermethylation of
H19 due to LOI of IGF2 leading to
biallelic expression and twofold
increase in doses
sporadic
germline