2008–2009 ÖöRETøM YILI
FEN BÖLÜMÜ
YARIùMA PROJESø
øLAÇ TAùIMA SøSTEMLERøNøN
GELøùTøRøLMESøNE YÖNELøK
ELEKTROKøMYASAL UYGULAMALAR
Proje Dalı: Kimya
Proje Danıúmanı: Binnur ORAL (AKINERø)
Proje Ö÷rencileri: Ebru Donk ve Deniz Yi÷iter (10-A sınıfı ö÷rencileri)
GøRøù
Elektrokimyasal sensörler (elektrokimyasal algılayıcı sistemler) Analitik
Kimya’da oldukça yaygın kullanımı olan cihazlardır. Bu cihazlara IUPAC tarafından
literatürde getirilen tanım úu úekildedir:
“Kimyasal bileúiklere ya da iyonlara seçici ve tersinir bir úekilde cevap veren ve
konsantrasyona ba÷ımlı elektriksel sinyaller oluúturan küçültülmüú cihazlara
elektrokimyasal sensörler “denir (1). Bu sensörler, yapılarına enzim, hücre, doku,
antikor, DNA, vb. biyolojik maddelerin eklenmesiyle BøYOSENSÖR adını almıúlardır.
Nitel ve nicel analiz yapabilen kompleks cihazlar olan biyosensörler, “biyo”
(=biyolojik kökenli) ve “sensör” (= algılayıcı) kelimelerinden oluúmaktadır. Di÷er bir
tanım ise; “Biri biyokimyasal, di÷eri ise elektrokimyasal özellikte, birbiri içine geçmiú
iki çeviriciden oluúan algılayıcı cihazdır” denilebilir. Biyokimyasal çevirici
analizlenecek madde ile etkileúerek onu tanır. Bu etkileúme sonucunda oluúan
madde (biyokimyasal ürün), elektrokimyasal çevirici tarafından okunabilir bir sayısal
de÷ere çevirilir.
Nükleik asitlerden oluúan tanıma yüzeyleri, Analitik Kimya alanında her geçen
gün daha ilgi çekici konular halini almaktadır. Bu tür tanıma yüzeyleri, bilinen
elektrokimyasal biyosensörlere yeni ve ender boyutlarda özellikler eklemektedir. Bu
geliúme ile, elektrokimyasal DNA biyosensörlerinin gelecekte hasta baúında
yapılacak doktor gözetimindeki analizlerde çok önemli bir rol oynayaca÷ı kesindir.
Elektrokimyasal yöntemlerle birlikte DNA’nın nitel ve nicel analizini yapma
amacına yönelik tasarlanan biyosensörlerde tanıma yüzey katmanı olarak DNA
kullanılmasına ilgi artmaktadır (2-4).
Nükleik asit(DNA) tanıma yüzeyi içeren biyosensörler, bu yüzey ile etkileúime
giren analizlenecek maddenin (karsinojen maddeler, ilaçlar vb.) etkileúim
mekanizmasının aydınlatılması veya miktarının tayininde veya DNA’daki baz dizisi
belli bölgelerdeki hibridizasyon olaylarının izlenmesi gibi amaçlarla kullanılabilir (527). Analizlenecek maddenin, DNA ile etkileúmesi sonucunda, incelenen maddenin
veya DNA’daki bir bazın sinyalinde meydana gelecek de÷iúiklikler sayesinde tayini
yapılabilmektedir.
Bazı ilaç molekülleriyle DNA' nın etkileúmesi (özellikle de antikanser özellik
taúıyan ilaç molekülleri ile etkileúim) ve bu etkileúmenin geliútirilen yeni yöntemlerle
tayin edilmesi; yeni ilaç tasarımları için çok önemlidir. Yine bazı maddelerin (çevresel
kirlilik ajanları, toksik molekül, vb.) çift sarmal DNA ile interkalasyon (düzlemsel
yapıdaki maddenin DNA çift sarmalı arasına girerek yerleúmesi), baza seçimli
ba÷lanma vb. yollarla etkileúimi sonucu bir ürünün oluúması, bu ürüne duyarlı
elektrokimyasal DNA biyosensör tasarımını getirmiútir. Bir kimyasal maddenin veya
metabolitin DNA ile etkileúimi sonrasında DNA’da oluúabilecek yan ürünlerin
(=adduct) kısa zamanda tespiti kanser araútırmaları için çok önemlidir (9).
Madde-DNA etkileúiminin sonucunda, çalıúmanın türüne göre elde edilen
madde sinyali ya da DNA’daki bir bazın sinyalindeki artma veya azalmaya ba÷lı
olarak elektrokimyasal tayin gerçekleútirilmektedir. Bu amaçla kullanılan DNA
modifiye edilmiú camsı karbon elektrotlar (GCE), karbon pastası elektrotlar (CPE),
perde baskılı karbon (SCPE) ve altın perde baskılı elektrotlar (Au-SCPE), Altın
elektrotlar (AuE) ve asılı civa damla elektrodu (HMDE) incelenen maddelerin
mikromolar ve hatta nanomolar konsantrasyonlarının dahi, kısa bir biriktirme aúaması
sonrası güvenli ölçümlerini mümkün kılmaktadır (10-14).
Çalıúmamızın amacı, manyetik partikül yüzeyine tutturulan antikanser ilaç olan
Daunorubisin (DNR)’in, etkin manyetik ayırma ve tek kullanımlık elektrokimyasal
sensör teknolojisi ile tayin etmek ve gelecekte hedeflenen ilaç taúıma sistemlerinin
izlenmesine yönelik mevcut yöntemlere kıyasla daha kolay, daha ucuz, daha hızlı,
daha seçimli ve güvenli bir úekilde tanımlanmasına yönelik alternatif bir yöntem
tasarlamaktır.
GELøùME
ELEKTROKøMYA
Maddenin elektrik enerjisi ile etkileúmesini ve bunun sonucunda oluúan
kimyasal dönüúümleri, fiziksel de÷iúiklikleri ve kimyasal enerjinin elektrik enerjisine
çevrilmesini inceleyen bilim dalı, elektrokimya olarak tanımlanır. Elektrokimyasal
tepkimeler, yükseltgenme-indirgenme türü tepkimelerdir; elektron transferi veya
geçiúi söz konusudur ve elektrokimyasal hücre adı verilen bir hücrede yürütülür.
Analizi yapılacak çözelti, bir elektrokimyasal hücrenin parçası oldu÷unda
çözeltinin elektrokimyasal özelliklerine dayanan bir grup kantitatif analitik yöntemin
incelenmesi “elektroanalitik kimya”nın kapsamına girmektedir. Elektroanalitik
teknikler, çok düúük tayin sınırlarına ulaúabilirler ve elektrokimyasal yöntemlerin
uygulanabildi÷i sistemler hakkında, bilgileri de içeren çok fazla sistemi karakterize
eden bilgiler verirler.
Elektroanalitik yöntemler, di÷er analiz yöntemlerine göre bazı üstünlüklere
sahiptirler. Birincisi, elektrokimyasal ölçümler ço÷u kez bir elemente, moleküle veya
tepkime sonunda oluúan ürüne özel bir yükseltgenme basama÷ı için spesifiktir.
Elektroanalitik yöntemlerin ikinci bir önemli üstünlü÷ü de, kullanılan cihazların di÷er
yöntemlerde kullanılan cihazlara nispeten ucuz olmasıdır.
Bir elektrokimyasal tepkimenin oluúabilmesi için, incelenen maddeyi içeren bir
çözelti, maddenin kimyasal dönüúüme u÷radı÷ı elektrot sistemi (genellikle üçlü
elektrot sistemi) ve bu elektrotları birbirine ba÷layan bir çevirim sistemi (transducer)
gereklidir. Çözelti olarak elektriksel iletkenli÷i sa÷lamak amacıyla tampon çözelti
kullanılır. Çeúitli elektrolitik yöntemler ile Do÷ru akım (DC), Diferansiyel Puls (DPV),
Dönüúümlü Voltametri (CV) vb. de belirli potansiyel aralı÷ında tarama yapılarak
meydana gelen akım úiddeti ölçülür. Akım, difüzyona ba÷lı olarak oluútu÷undan
dolayı burada ölçülen difüzyon akımıdır. Difüzyon hızı akım ile do÷ru orantılıdır.
Difüzyon, elektrot yüzeyinin yakınındaki difüzyon tabakasında oluúur.
VOLTAMETRø VE ESASLARI
Elektroda uygulanan gerilimin(potansiyelin) bir fonksiyonu olarak akımın
ölçülmesine dayanan elektrokimyasal yönteme voltametri denir. Uygulanan gerilimin
ölçülen akım de÷erlerine karúı çizilen grafi÷ine voltamogram denir. Voltametride,
herhangi bir maddenin elektrokimyasal davranıúını incelemek için elektroda
uygulanabilecek gerilim aralı÷ının sınırları, kullanılan çalıúma elektrodunun ve
kullanılan çözücü ve elektrolit türlerine ba÷lıdır.
Tarihsel olarak, voltametri Çekoslavak kimyacı Jaroslav Heyrovsky tarafından
1920 ‘lerin baúında geliútirilen ve voltametrinin özel bir tipi olan polarografi tekni÷ine
dayanarak geliútirilmiútir. Voltametrinin hala önemli bir kolu olan polarografinin di÷er
voltametrik tekniklerden en büyük farkı çalıúma elektrodu olarak bir damlayan civa
elektrodunun (DCE) kullanılmasıdır.
Voltametri, inorganik, fiziko ve biyokimyacılar tarafından çeúitli ortamlarda
oluúan yükseltgenme ve indirgenme iúlemlerinin incelenmesi, yüzeydeki adsorpsiyon
iúlemlerinin araútırılması ve kimyasal olarak modifiye edilmiú elektrot yüzeylerinde
gerçekleúen elektron aktarım mekanizmalarının aydınlatılması gibi analitik olmayan
amaçlar için de oldukça yaygın bir úekilde kullanılmaktadır.
Voltametrik Cihazlar:
Voltametrik
analizde
kullanılacak cihazlar,
elektrokimyasal
hücre,
analizlenecek madde ve destek elektrolit adı verilen elektrolitin aúırısını içeren bir
çözeltiye daldırılmıú üç elektrottan yapılmıútır.
Tanım olarak;
1) Çalıúma elektrodu; tasarımı yapılacak bir biyosensör bu üçlü sistemlerde
kullanılabilmektedir. Bu elektrot, yüzeyinde analizlenecek maddenin yükseltgendi÷i
veya indirgendi÷i elektrottur.
2) Referans elektrot; Referans elektrot, potansiyeli deney süresince sabit
kalan bir elektrottur. Ag / AgCl veya doygun kalomel elektrot (DKE) kullanılabilir.
3)Yardımcı elektrot; Platin bir tel veya bir civa havuzu úeklinde olan ve
elektri÷in çözelti içinden çalıúma elektroduna aktarılmasını sa÷layan karúıt
elektrottur. Bu elektrot, çalıúma elektrodu ile bir çift oluúturan fakat ölçülen
potansiyelin büyüklü÷ünün tayininde rol oynamayan bir elektrottur. ùekil-1, üçlü
elektrot sistemini göstermektedir.
ùekil 1 : Üçlü elektrot sistemi
Voltametride kullanılan çalıúma elektrotları
Çalıúma elektrodunun yapımında kullanılan iletken malzeme, platin ya da altın
gibi inert bir metal; karbon, pirolitik grafit ya da camsı karbon; kalay oksit ya da
indiyum oksit gibi yarı-iletken veya bir civa filmi ile kaplanmıú bir metal olabilir. Bu
elektrotlar çeúitli úekil ve büyüklükte olabilmektedirler ve biyosensör tasarımı için en
uygun úekilde geliútirilmektedirler.
Bu tür elektrotların kullanıldı÷ı potansiyel aralı÷ının tespiti çok önemlidir.
Özellikle de bu potansiyel aralı÷ı, sulu çözeltilerde sadece elektrot malzemesine
de÷il, aynı zamanda bu elektrotların daldırıldı÷ı çözeltinin bileúimine ba÷lı olarak da
de÷iúir. Pozitif potansiyel sınırları genellikle moleküler oksijen verecek úekilde, suyun
yükseltgenmesi sonunda oluúan büyük akımlarca belirlenir. Negatif potansiyel
sınırları yine suyun indirgenmesi sonunda oluúan hidrojenden kaynaklanır.
Kullanılan çalıúma ortamına göre çalıúma elektrotları için seçilen potansiyel
aralıkları ; civa elektrodu için 1 M H2SO4 çalıúma ortamında, (-0,8 V) ile (+0,4 V)
aralı÷ı ve 1 M KCl çalıúma ortamında, (-1,6 V) ile (+0,2 V) aralı÷ıdır. Karbon
elektrodu için ise, 1 M HClO4 ortamında, (+0,2 V) ile (+1,8 V) aralı÷ı ile, 0,1 M KCl
ortamında (-1,0 V) ile (+1,2 V) aralı÷ıdır.
Karbon elektrotlar :
Karbon elektrotlar, özellikle çok ucuz olmaları ve geniú bir potansiyel
aralı÷ında çalıúma yapılmasına olanak verdi÷inden dolayı elektrokimyasal analizlerde
sık kullanılır. Ancak, karbonun, yüksek bir yüzey aktivitesi vardır ve bu nedenle
organik bileúikler tarafından kolayca kirletilebilir. Hidrojen, hidroksil ve karboksil
grupları ve hatta kinonlar ile karbon yüzeyinde ba÷lar oluúabilmektedir. Bu
fonksiyonel grupların varlı÷ı nedeniyle karbon yüzeyine birçok de÷iúik madde
tutturulabilir.
Karbon elektrotların çeúitleri:
Karbon Pastası Elektrodu (CPE):
Grafit tozunda bulunan karbon moleküllerinin düzlemsel ve aromatik halkalar
halinde dizilimi, ùekil-2' de görülmektedir. Zayıf S ba÷ları ile birbirine ba÷lanmıú olan
bu tabakalar arasında hızlı bir elektron alıúveriúi olabilmektedir.
ùekil 2. Grafit tozunda bulunan karbon
moleküllerinin dizilimi.
ùekil 3. Karbon pastası elektrodu.
CPE, ucuz olması, yüzey yenilenmesinin kolay olması, düúük artık akımlar
oluúturması nedeniyle tercih edilmektedir (15,16). Ba÷layıcı madde olarak, Nujol
(mineral ya÷), parafin ya÷ı, silikon ya÷ı ve bromonaftalen kullanılmaktadır. Elektrot
aktivitesine pasta bileúiminin büyük etkisi vardır. Ba÷layıcı organik sıvı oranı arttıkça,
elektron transfer hızı azalmaktadır. CPE'nin en önemli sakıncası, yeterli miktarda
organik çözgen içeren çözeltilerde kullanıldı÷ı zaman, karbon pastası çözeltide
da÷ılmaktadır.
Kalem grafit elektrodu:
Çalıúmada kullanılan kalem grafit elektrot (PGE); grafitten oluúmuú olup, Tombo
HB kalem uçlarının 3 cm boyutunda kesilmesiyle hazırlandı.
ùekil 4: Kalem ucu elektrot.
BøYOSENSÖR
Biyosensörler biyolojik tepkimelerde hedef analizlenecek maddeleri tayin etmek
için kullanılan küçük algılayıcı cihazlardır. Birbiri içine geçmiú biri biyokimyasal, di÷eri
elektrokimyasal özellikteki iki çeviriciden oluúmaktadır. Biyokimyasal kısmın görevi
analizlenecek maddeyle etkileúerek onu tanımaktır. Bu tanıma olayının sonucunda
bir biyokimyasal ürün de oluúabilmektedir. Biyosensörün ikinci kısmı olan
elektrokimyasal kısım ise, bu tanıma olayını okunabilir (ölçülebilir) bir sayısal de÷ere
çevirmekle görevlidir (15).
ùekil 5: Biyosensörün yapısı.
ødeal bir biyosensörün sahip olması gereken özellikler:
1.
2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
Seçicilik
Kullanım Ömrü
Kalibrasyon Gereksinmesi
Tekrarlanabilirlik
Stabilite
Yüksek Duyarlılık
Yeterli Düzeyde Tayin Sınırı
Geniú Ölçüm Aralı÷ı
Hızlı Cevap Zamanı
Hızlı Geriye Dönme Zamanı
Basitlik ve Ucuzluk
Küçültülebilirlik ve Sterilize edilebilirlik
DENEYSEL BÖLÜM
KULLANILAN CøHAZLAR VE KøMYASAL MADDELER
Ölçümler ve deneyler esnasında kullanılan tüm cihaz, donanım ve yazılımlar;
Terazi (Mettler Toledo AB204-S )
pH-metre (Orion 420A)
Manyetik karıútırıcı (Biosan MS 3000)
Vorteks (Biosan V1)
Potansiyostat (AUTOLAB 302, GPES 4,9 yazılımlı; Eco Chemie,Hollanda)
Manyetik Ayırıcı (Sigris, A.B.D)
Ag/AgCl referans elektrot (BAS)
Platin tel (Yardımcı elektrot olarak kullanıldı)
Çalıúma elektrodu (kalem grafit elektrot-PGE)
Asetik Asit (%99-100)
(Merck)
Manyetik partiküller
(Dynal Biotech ASA))
Hidroklorik asit (%37)
(Merck)
Sodyum Hidroksit
(Merck)
Daunorubisin
(Sigma)
Tris (hidroksimetil)aminometan hidroklorür
(Sigma)
Sodyum klorür
(Sigma)
Tüm çalıúmalarda sterilize edilmiú deiyonize su kullanıldı. Deneysel çalıúmalar
oda sıcaklı÷ında (25.0 r 0.5) q C’ de gerçekleútirildi.
ùekil 7. Deneylerde kullanılan bilgisayara ba÷lı elektrokimyasal ölçüm cihazı
ùekil 8. Deneylerde kullanılan üçlü elektrot sistemi.
Kullanılan elektrotların hazırlanıúı
Kalem Ucu Grafit Elektrot (PGE) hazırlanıúı:
Grafit uç içeren kalem elektrodun tekrarlanabilirli÷inin daha iyi olması, daha
düúük tayin sınırı, ucuz ve tek kullanımlık olması sebebiyle bu elektrodun
kullanılmasına artan bir ilgi bulunmaktadır (16,22).
Çalıúmada kullanılan kalem ucu elektrot; Tombo HB kalem uçlarının 3 cm
boyutunda kesilmesiyle hazırlandı.
Manyetik partiküllere dayalı sistemin ilaç algılamaya yönelik
uygulamaları:
Çalıúmamızda manyetik partiküller (MNP) ve bu partiküllerin prosedüre göre
hazırlanması ve ayrılmasında, MCB 1200 Biyomanyetik ayırma platformu kullanıldı.
Antikanser ilaç Daunorubisin (DNR)’nin manyetik partikül yüzeyine tutturulması
iúlemlerinde aúa÷ıdaki prosedür izlenerek gerçekleútirildi (16):
3 μL manyetik partiküller (MNP) 1.5 mL’lik ependorf tüpüne transfer edildi ve
üzerine 50 μL, 5 mM Tris tampon (TBS) çözeltisi ilave edilerek 5 dakika yıkandı ve
daha
sonra
yıkama
çözeltisi
ortamdan
uzaklaútırıldı.
Ortama
farklı
konsantrasyonlardaki DNR çözeltisinden 25 μL ilave edildi ve 5 dakika boyunca
karıútırılarak DNR’nin partikül yüzeyine tutturulması sa÷landıktan sonra çözelti
ortamdan uzaklaútırıldı. Manyetik partiküller, 5 mM fosfat tamponu (PBS) ile 5 dak
süreyle yıkandı. Daha sonra yıkama çözeltisi ortamdan uzaklaútırıldı. Yıkama
iúleminden sonra partiküllere, alkali hidroksit çözeltisi ile muamele edildi. Alkali
muamelesi basama÷ından sonra örnek üzerine, asetat tamponu (ABS) ilave
edildikten sonra, çözelti viyal içine transfer edildi. Daha sonra yüzeyi aktive edilmiú
elektrot PGE, adsorpsiyon iúlemi için, bu viyallere daldırıldı. Elektrotlar süre sonunda
ABS ile yıkandıktan sonra, DPV ölçümü için, ABS içeren elektrokimyasal hücredeki
üçlü elektrot sistemine yerleútirildi.
Voltametrik ölçüm:
Üçlü elektrot sistemi elektrokimyasal hücre içine daldırıldı ve daha sonra
voltametrik ölçüm gerçekleútirildi. DNR yükseltgenme sinyali, DPV tekni÷i ile ölçüldü.
Aynı deneysel úema, ortamda DNR yokken tekrarlandı.
BULGULAR VE TARTIùMA:
Manyetik partiküllere dayalı sistemin ilaç algılamaya yönelik uygulamalar
ile ilgili bulgular:
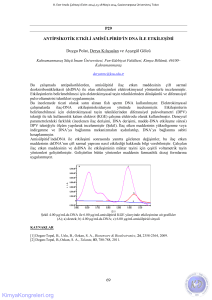
Manyetik partiküllere dayalı sistemde, farklı konsantrasyonlarda DNR’nin
partikül yüzeyine tutturulması sonrasında +0.55 V civarında görülen DNR
yükseltgenme sinyali DPV yöntemiyle ölçüldü. Elde edilen voltamogram ve histogram
sırasıyla, úekil 9 ve 10’da gösterildi.
ùekil
9:
Manyetik
partiküllere
dayalı
sistemde,
farklı
DNR
konsantrasyonlarında PGE ile ölçülen DNR yükseltgenme sinyallerini gösteren
voltamogram: (a) 0, (b) 2, (c) 4, (d) 6, (e) 8, (f) 10 ve (g) 12 PM DNR
konsantrasyonlarında ölçülen DNR yükseltgenme sinyallerini göstermektedir.
ùekil
10:
Manyetik
partiküllere
dayalı
sistemde,
farklı
DNR
konsantrasyonlarında PGE ile ölçülen DNR yükseltgenme sinyallerini gösteren
histogram.
Manyetik partiküllere dayalı sistemin ilaç algılamaya yönelik
uygulamalara iliúkin tartıúma ve sonuç:
Manyetik partiküllere dayalı sistemde, 2-12 μM aralı÷ında de÷iúen
konsantrasyonlarda DNR’nin partikül yüzeyine herhangi bir ba÷layıcı ajan
kullanılmaksızın tutturulması sonrasında, +0.55 V civarında görülen DNR
yükseltgenme sinyalleri kalem grafit elektrot (PGE) ile ölçüldü ve elde edilen
histogram (úekil 9 ve 10) incelendi÷inde, DNR yükseltgenme sinyalinin, 2-10 μM
aralı÷ında de÷iúen DNR konsantrasyonlarında aúamalı bir úekilde arttı÷ı, 10 μM
DNR konsantrasyon de÷erinden itibaren azaldı÷ı görüldü.
Literatürde farklı ilaçların di÷er ilaç taúıma sistemlerinin yüzeylerine
tutturulmasına yönelik çalıúmalar sonucunda, elde etti÷imiz sonuca paralel sonuçlar
gözlendi÷i saptandı (28).
Çalıúmamızda geliútirdi÷imiz bu sensör teknolojisi ile, daha az madde
kullanılarak, partikül yüzeylerine ilaçların immobilize edilebilece÷i gösterilirken; bu
sayede, gelecekte tedavide kullanılabilecek ilaç taúıma sisteminin ve daha duyarlı,
daha ucuz bir yöntemle, daha kısa sürede sonuçlanabilecek bir elektrokimyasal ilaç
analizininde mümkün olabilece÷i düúünülmektedir.
TEùEKKÜR
Çalıúmalarımız sırasında bize danıúmanlık yapan Doç. Dr. Kadriye Arzum
Erdem Gürsan’a, doktora ö÷rencisi Hakan Karadeniz’e, yüksek lisans ö÷rencisi Ecz.
Ayfer Turan’a ve Özel Ege Lisesi Kimya ö÷retmeni Binnur Oral’a (Akıneri);
gereksinim duydu÷umuz cihaz ve malzemelerinin kullanımına izin veren Ege
Üniversitesi, Eczacılık Fakültesi’ ne teúekkür ederiz.
KAYNAKÇA
1. Wang, J.; Rivas, G.; Cai, X.; Palecek, E.; Nielsen, P.; Shiraishi, H.; Dontha,
N.; Luo, D.; Parrado, C.; Chicharro, M.; Farias, P. A. M.; Valera, F. S.; Grant, D. H.;
Ozsoz, M.; Flair, M. N. Anal. Chim. Acta, 1997, 347, 1.
2. Wang, J.; Cai, X.; Rivas, G.; Shiraishi, H.; Farias, P. A. M.; Dontha, N. Anal.
Chem., 1996, 15, 2629.
3. Wang, J.; Rivas, G.; Cai, X.; Dontha, N.; Shiraishi, H.; Luo, Valera, F. S.
Anal. Chim. Acta, 1997, 337, 41.
4. Wilson, E. K. Chem. & Engin. News, 1998, 76, 21.
5. Wang, J. Biosensors & Bioelectronics, 1998, 13, 757.
6. Wang, J.; Rivas, G.; Cai, X.; Chicharro, M.; Parrado, C.; Dontha, N.;
Begleiter, A.; Mowat, M.; Palecek, E.; Nielsen, P. E. Anal. Chim Acta, 1997, 344,
111.
7. Karadeniz, H.; Erdem, A.; Caliskan A.; Pereira C. M.; Pereira E. M.; Ribeiro
J. A.; Electrochemistry Communications, 2007, 9, 2167.
8. Wang, J.; Rivas, G.; Fernandes, J. R.; Paz, J. L. L.; Jiang, M.; Waymire, R.
Anal. Chim. Acta, 1998, 375, 197.
9. Mikkelsen, S. R. Electroanalysis, 1996, 1, 8.
10. Millan, K. M.; Saraullo, A.; Mikkelsen, S. R. Anal. Chem., 1994, 66, 2943.
11. Erdem, A.; Kerman, K.; Meric, B; Akarca, U. S.; Ozsoz, M. Electroanalysis,
1999, 11, 586.
12. Erdem, A.; Meric, B.; Kerman, K.; Dalbasti, T.; Ozsoz, M. Electroanalysis,
2001, 13, 219.
13. Erdem, A.; Kerman, K.; Meric, B; Akarca, U. S.; Ozsoz, M., Anal. Chim.
Acta, 2000, 422, 139.
14. Karadeniz, H.; Alparslan, L.; Erdem, A.; Karasulu, E. Journal of
Pharmaceutical and Biomedical Analysis, 2007, 45, 322.
15. Coulet, P. R. (1991). What is a Biosensor?, Chapter 1; Biosensor
principles and applications, Editörler; L.J.Blum, P.R. Coulet, Marcel Dekker Inc., New
York, 1-6
16. Wang, J.; Kawde, A.-N.; Erdem, A.; Salazar M. A.; Analyst, 2001, 126,
2020.
17. Wang, J. Nucl. Acids Res., 2000, 28, 3011.
18. Palecek, E.; Fojta, M. Anal. Chem., 2001, 73, 75A.
19. Erdem, A.; Ozsoz, M. Anal. Chim. Acta, 2001, 437, 107.
20. Erdem, A.; Ozsoz, M. Turkish Journal of Chemistry, 2001, 25, 469.
21. Jelen, F.; Erdem, A.; Palecek, E. Bioelectrochemistry, 2002, 55, 165.
22. Karadeniz, H.; Gulmez, B.; Sahinci, F.; Erdem, A.; Kaya, I.G.; Unver, N.;
Kivcak, B.; Ozsoz, M. Journal of Pharmaceutical and Biomedical Analysis, 2003, 33,
295.
23. Querioz, M.R.P.; Castanheira, E.M.S.; Carvalho, M.S.D.; Abreu, A.S.;
Ferreira, P.M.T.; Karadeniz, H.; Erdem, A. Tetrahedron, 2008, 2, 382.
24. Erdem, A.; Ozsoz, M. Electroanalysis, 2002, 14, 965.
25. Wong, E.; Giandomenico, C.M. Chem. Rev., 1999, 99, 2451.
26. Ozsoz M., Erdem A., Kara P., Kerman K., Ozkan D. (2002).
Electroanalysis, 15: 613-619.
27. Erdem, A.; Kosmider, B.; Osiecka, R.; Zyner, E.; Ochocki, J.; Ozsoz, M.
Journal of Pharmaceutical and Biomedical Analysis, 2005, 38 (4), 645.
28. D’Emanuele, A.; Attwood, D., Advanced Drug Delivery Reviews, 2005, 57,
2147-62.