DNA İZOLASYONU
VE ANALİZİ
ELİF SANCAR
130154015
ERZURUM TEKNİK ÜNİVERSİTESİ
DNA ÇALIŞIRKEN GÖZ ÖNÜNDE BULUNDURMANIZ
GEREKEN TEMEL ÖZELLİKLER
1-DNA basit bir moleküldür. Gerçekten Sadece A,T,C ve G
nükleotidlerini içerir. Bu araştırma yaparken önceden tahmin edebilmek
demektir.
2-DNA negatif yüklüdür. Elektronların büyük bir çoğunluğu oksijen
gruplarının etrafında dolanırlar.
3- DNA çok sayıda halka yapısına sahiptir. Halka yapıları oldukça
hidrofobiktir.
4-DNA çok dayanıklı bir moleküldür. Örnek tüpünüzü düşürdünüz mü?
Muhtemelen bir sorun yoktur. Hafta sonu boyunca oda ısısında mı
bıraktınız? Sorun değil Genellikle çalışılması en kolay olan
makromoleküldür.
5-DNA çalışmaları pek çok ihtiyaç gerektirir. Bu molekülle ne
çalıştığınıza bağlı olarak birçok şeye sahip olmalısınız. Bu şey bir prosedür
ya da spesifik bir enzim yada techizat olabilir
UNUTMAYIN!!!
Bazı genel kurallar bütün DNA deneylerinde
geçerlidir!!!
•
•
•
•
•
Deneyi iyi bilmek
Örneği olabildiğince saf elde etmek
Mümkün olduğunca her zaman dikkatli ve nazik olmak.
Molekülün özelliğini çok iyi bilmek
İhtiyaç olan malzemelerin miktarını dikkatlice düşünmek
CANLI HÜCRELERDEN DNA’ NIN SAFLAŞTIRILMASI
• Genetik materyal hücre içerisinde bulunduğu bölgede yoğunlaşmış bir kitle
oluşturur.
• Her insanın hücresinde bulunan DNA çözüldüğünde yaklaşık 183 cm
uzunluğunda olacaktır. Her bir hücrenin küçücük çekirdeğinde şaşırtıcı
miktarda materyal paketlenmiştir. Hücredeki bu olay kromozom
organizasyonu ile açıklanmaktadır.
• Bölünmemiş bir hücrede kromozomal DNA kromatin olarak isimlendirilen
çözülmüş bir görünümdedir.
• Elektron mikroskobuyla gözlendiğinde, histon proteinlerinin bir ipteki
tespih tanesi görünümünü verecek şekilde DNA’ nın sıkı bir şekilde sarıldığı
parçacıklar olarak görev yaptıkları anlaşılır. Hücre bölündüğünde kromotin
sıkı iplikler ve sıkı kıvrımlı ilmikli yapılar halinde yoğunlaşır. Sonuçta bu sıkı
kıvrımlı ilmikler, oldukça yoğun DNA demetinden oluşan tam bir kromozom
oluşturmak için diğer proteinlerin yardımıyla birlikte sıkı bir şekilde
paketlenir.
• Bu paketlenmenin organizasyonu sırasında DNA, çeşitli katyonlar (iki
değerlikli metaller) ile etkileşim halinde bulunur.
Şekil -1: Kromozom organizasyonu
Genetik olayların hücrede moleküler düzeydeki temeli; genetik mertaryal
görevini yüklenen nükleik asitlerin yapı ve özelliklerine dayanır. Nükleik asitlerin
iki türü (DNA ve RNA) nükleotidlerin polimerleridir. Bu nükleotid 3 kısımdan
oluşur; 1- Heterosiklik hakla yapısı gösteren 5 karbonlu bir şeker (pentoz), 2Heterosiklik bir C halkası ve N atomları içeren organik baz ( pürin veya
pirimidin ), 3- Bir fosfat grubu.
Glikozidik Bağ
Şekil-2: Nükleotid yapısı
Nükleotid yapısında, bir glikozidik bağ ile birbirine bağlanmış baz ve pentoz
kısmına nükleozid adı verilir. Nükleotidler birbirlerine bir nükleotidin
pentozunun 5’ pozisyonundaki fosfat (PO4) grubu ile onu izleyen nükleotidin
pentozunun 3’ pozisyonundaki hidroksil (OH) grubu arasında kovalent şekilde
oluşan fosfodiester bağı ile bağlanır.
Canlıların büyük çoğunluğunda çift
zincirli olan DNA molekülünde iki
polinükleotid zincir bazları arasında
oluşan hidrojen bağları ile bir arada
tutulur. Bazlar arasında H bağlarının
oluşumunun
özgüllüğü,
iki
polinükleotid zincirdeki fosfodiester
bağlarının birbirine ters yönde olmasına
yol açar. Bu nedenle iki zincir birbirine
zıt yönde paraleldir.
Şekil-3: Çift zincirli DNA yapısı
• Bazı kimyasal maddeler ve enzimler ile canlı hücrelere ait
hücre zarı veya canlı hücre duvarının yıkılıp DNA’ nın ortaya
çıkarılmasına DNA izolasyonu denir.
DNA izolasyonu moleküler biyolojinin en temel tekniklerinden birisidir.
Neden DNA izolasyonu??
Yüksek molekül ağırlıklı DNA izolasyonu;
DNA parmak izi analizi,
DNA-protein etkileşiminin incelenmesi,
RFLP ( Restriction Fragment Lenght Polymorphism),
genomik kütüphane hazırlanması ve
araştırma laboratuvarları ve endüstride PCR
analizlerindeki artış ile çok önemli hale gelmiştir.
• DNA izolasyonu aynı zamanda;
• kompleks bir DNA populasyonu içindeki spesifik DNA
dizilerinin çalışılmasında,
• gen expresyonu ve
• genom yapısının analizinde de ilk basamaktır.
Doğadaki canlıların tümüne yakın kısmında genetik
materyal DNA’dır. Bu nedenle, genetik materyalle
yapılacak çeşitli çalışmalarda moleküler biyoloji
tekniklerinin uygulanabilmesi için öncelikle yüksek
molekül ağırlıklı DNA molekülünün saf bir şekilde elde
edilmesi gerekmektedir.
DNA İZOLASYONU
Kromozomun DNA
izolasyonu
Organel DNA
izolasyonu
Plazmid DNA izolasyonu
GENOMİK DNA
İZOLASYONU
Genomik DNA nedir?
Profilleme/ Fingerprinting: Kan,
sperm örneklerini karşılaştırmak adli
bilimlerde kullanılan bir metottur.
Yeni bir gen klonlamaya ilk adım
Bir hücredeki ve/veya virüsteki
bütün genleri içeren DNA örneği
demektir. Genomik DNA bütün
hücrelerde bulunur ve bu hücreler
genomik
DNA
analizleri
için
kullanılabilir. Genomik DNA büyüktür,
komplekstir ve sulu oramlarda viskoz
görünür. Örneğin; prenatal tanı için
amniyotik sıvıdaki fetal hücrelerden
veya koryonik hücrelerden genomik
DNA elde edilebilir. Erişkinlerde
periferal kandaki lökositler en kolay
ulaşılabilen DNA kaynağıdır.
Neden genomik DNA elde ediyoruz?
Karakterizasyon/ Tanımlama: Gen ifadesi ve regülasyonunu
araştırmak. Örneğin; transgenik bir organizma yapıyorsunuz
ve modifikasyonun gerçekleşip gerçekleşmediğini kontrol
etmeniz gerekir. İlginç bir fenotip elde ettiniz ve daha
derine bakmak istiyorsunuz.
DNA izolasyonu metodunun seçiminde dikkat
edilmesi gereken noktalar
DNA’yı protein ve RNA gibi ana kontaminantlardan
arındırmalı,
Hücresel DNA’nın çoğunun izole edilebileceği bir
metot olmalı,
DNA’nın fiziksel ve kimyasal yapısını bozmamalı,
Elde edilen DNA yüksek molekül ağırlıklı olmalı,
(çok fazla kırık bulunmamalı)
Hızlı ve kolay olmalı
İzolasyonda Kullanılan Maddeler ve İşlevleri
• Tris (tampon)
• EDTA (Dnase aktivitesi için gerekli kofaktörleri tutar)
• NaCl (proteinleri ayırır)
• SDS (deterjandır; membranları denetüre eder, DNA çok dayanıklı olduğu
için SDS muamelesinden etkilenmez)
• Proteinaz K (DNA’ya bağlı olan proteinleri (ökromatin yapısındaki /
histonlar vb) parçalayarak DNAnın serbest kalmasını sağlar.
• Ribonükleaz (RNA’ların uzaklaştırılmasında)
• Fenol/Kloroform /izoamil alkol
• Protein denatürasyonu
• Isopropanol veya ethanol
• DNA Presipitasyon
• Santrifüj / süpernatant uzaklaştır
DNA İZOLASYONUNU AŞAMALARI
DNA izolasyonunun amacı, bir hücrenin tüm genetik materyalini taşıyan
DNA’nın hücrenin diğer bütün bileşenlerinden ayırmaktır.
Günümüzde bir çok DNA izolasyon metodu geliştirilmiştir.
Ancak kullanılan metot ne olursa olsun, bütün metotlar şu dört ana basamağı
içerir:
1.Hücrelerin parçalanması (LİZİS)
2.Protein ve RNA’nın uzaklaştırılması (PÜRİFİKASYON)
3. DNA’nın yoğunlaştırılması (PRESİPİTASYON)
4. DNA’nın kalite ve saflığının tespiti.
1. Hücrelerin parçalanması (lizis):
•fiziksel,
•kimyasal ve
•enzimatik yollar kullanılarak yapılabilir.
•Sonikasyon, ezme, parçalama ve yüksek basınç uygulama gibi fiziksel
olarak parçalama işlemleri DNA hazırlamak için tercih edilmemeli
Çünkü bu işlemler DNA’nın küçük parçalara ayrılmasına neden olacak
kuvvetli güçler uygular.
•Hücreleri açmak ve bütün bir DNA elde etmek için en iyi yöntem
kimyasal (deterjanlar) ve/veya enzimatik işlemler uygulamaktır.
Deterjanlar hücre zarındaki lipitleri çözerek hücreyi DNA’sına zarar
vermeden parçalarlar. Ayrıca hücresel DNaz enzimlerini inhibe
ederler ve proteinlerin denatüre olmasına neden olurlar ki buda
proteinlerin solüsyondan uzaklaştırılmasına yardımcı olur.
Hayvan hücrelerinin parçalanması;
•SDS (Sodium Deodecyl Sulfate) ve
•Sarcosyl (N-laurylsarcosine, sodium salt) gibi anyonik deterjanların
kullanılması ile gerçekleştirilir.
2. Protein ve RNA’nın uzaklaştırılması:
Proteinlerin hücre lizatından uzaklaştırılması DNA izolasyonunun ikinci
basamağını oluşturur. Bu işlem “deproteinizasyon” olarak adlandırılır.
Proteinlerin DNA solüsyonundan uzaklaştırılması, nükleik asitlerin ve
proteinlerin farklı fiziksel özelliklere sahip olması temeline dayanır.
Nükleik asitler çoğunlukla hidrofilik moleküller olup, suda kolayca
çözünürken proteinler içerdikleri hidrofobik kısımlar nedeniyle organik
çözücülerde kısmen çözünürler.
Fenol ve %4 izoamil alkol içeren kloroform bu amaçla kullanılan organik
çözücüler arasında sayılabilir.
Fenol / Kloroform
Fenolde nükleik asitler çözünmez.
Lipidler, proteinler ve polisakkaritler fenol fazına
geçerler.
Fenol bir denatüre edici olarak davranır, proteinler
denatüre olarak çökelek oluştururlar ve ara fazda
toplanırlar.
**RNA’nın uzaklaştırılması:
DNA preparatlarından RNA ’ nın uzaklaştırılması
genellikle bir enzimatik işlemle gerçekleştirilir.
Bu işlem RNA’nın tümünü uzaklaştırmasa da RNA
kontaminasyonunun en az düzeye indirilmesini sağlar.
Ribonükleaz A ve ribonükleaz T1 bu amaç için
kullanılabilecek iki ucuz ve kolayca temin edilebilen
ribonükleazdır.
3. DNA’nın yoğunlaştırılması:
DNA saflaştırılmasının bu basamağının iki amacı vardır.
•Birincisi, deproteinizasyon solusyonundan yüksek molekül ağırlıklı
DNA’yı konsantre etmek,
•ikincisi ise nükleotidleri, amino asitleri ve hücre
parçalanmasından sonra kalan küçük molekül ağırlıklı atıkların
uzaklaştırılmasını sağlamaktır.
DNA alkol ile çöktürülür
•Bu basamakta iki yol kullanılır
diyaliz ile konsantre edilir
•Etanol ve izopropanol DNA’nın çöktürülmesi için en yaygın
olarak kullanılan alkollerdir. DNA ’ nın çöktürülmesi uygun
konsantrasyondaki sodyum ve amonyum tuzlarının varlığında % 70
lik etanolde gerçekleştirilir.
Diyaliz ile DNA’nın konsantre edilmesi:
Alkol ile çöktürme kullanılarak 150 kb den daha büyük DNA elde etmek
oldukça güçtür
Bu nedenle bu metot 200 kb veya daha yüksek molekül ağırlıklı DNA
elde edilmek istendiğinde kullanılan bir yöntemdir.
4. DNA’nın saflığının ve konsantrasyonunun tayini:
DNA izolasyon işleminin en son basamağı sonuçların
değerlendirilmesidir. DNA için bu değerlendirme şunları
içerir:
DNA konsantrasyonunun belirlenmesi
DNA’nın saflığının değerlendirilmesi
DNA miktarının belirlenmesi
BAKTERİLERDEN TOTAL DNA İZOLASYONU
DNA hazırlama esasları, ilk olarak bir bakteri hücresinin tüm DNA
komplementini gerektiren DNA saflaştırma prosedürünün en basit
tipini göz önüne almakla çok kolay bir şekilde anlaşılır. (Plazmid ve
faj DNA’ sı hazırlamak için daha farklı yöntemler izlenecektir.)
Bir bakteri hücre kültüründen total DNA hazırlamak için prosedür
dört safhaya ayrılır.
1. Bir bakteri kültürü büyütülür ve sonra hücreler toplanır8sıvı
ortamda ise çöktürülür)
2. Hücreler içeriklerini salıvermesi için parçalanır.
3. Bu hücre özütü DNA’dan başka tüm hücre bileşenlerini
uzaklaştırmak için muamele edilir.
4. Elde edilen DNA çözeltisi yoğunlaştırılır.
5. DNA’nın saflığı ve kalitesi kontrol edilir.
1. Bir Bakteri Kültürünü Geliştirme
Pek çok bakteri sıvı kültür ortamında çok fazla zorluk olmaksızın
büyüyebilir. Kültür ortamı, Bakterilerin büyümesine ve etkili
şekilde bölünmesine izin verecek derişimlerde esas besinlerin
dengeli bir karışımını sağlamalıdır. İki tipik büyüme ortamı vardır.
M9, tüm bileşenleri bilinen tanımlı ortama örnektir. Bu ortam
azot, magnezyum ve kalsiyum gibi esas elementleri sağlamak
için inorganik besinlerin bir karışımını hem de karbon ve enerji
sağlamak için glikozu içerir.
Pratikte daha önce bakteri büyümesini destekleyecek iz
elementler ve vitaminler gibi ilave büyüme faktörleri M9’ ilave
edilmelidir. (Bu ilaveler büyütülecek türe bağlıdır.)
Tablo 1: Bakteri kültürlerinin büyümesi için iki tipik
ortamın bileşeni
• Luria-Bertani (LB) bileşenlerinin kesin kimliği ve miktari bilinmeyen,
kompleks yada belirsiz ortamdır.
• Bu, bilineyen kimyasal bileşenlerin karmaşık karışımları olan iki malzemeden
(triptofan ve maya özütü) dolayıdır. LB gibi kültür ortamlarında ilaveye gerek
duyulmaz ve geniş çapta bakteri büyümesini destekler.
Tanımlı ortamlar, bakteri kültürü tam olarak kontrollü şartlar altında
büyütülmek zorunda olduğu zaman kullanılmalıdır. Bununla beraber, kültür
basitçe bir DNA kaynağı olarak büyütülüyorsa buna gerek yoktur ve bu şartlar
altında kompleks bir ortam uygundur.
• Bir hücre özütü hazırlamak için bakteriler, mümkün olduğu kadar küçük bir
hacimde hazırlanmalıdır.
•
Harmanlama bu nedenden dolayı santrifüjleme ile yapılmaktadır.
• Böylece kültür ortamdan uzaklaştırılacak, hücreler dipte topak oluşturacak.
Örneğin; 37°C’ deki LB ortamında, bir döner platformda 150-250 rpm’de
karıştırmakla havalandırılan E.coli hücreleri her 20 dakikada bir yada kültür 2-3
x 109) hücre/ml’lik maksimum bir yoğunluğa varıncaya kadar bölünür. Kültürün
büyümesi bir OD birim 0.8x 109) hücre/ml’ye karşılık gelen 600nm dalga
boyunda optik yoğunluk okunarak gözlenir.
Şekil-5: Optik yoğunluk ölçümüyle bakteri hücre sayısının tahmini
Şekil-4: Bir bakteri kültüründen total hücre DNA’sının hazırlanmasındaki temel
basamaklar
Şekil-6: Santrifüjleme ile bakteri harmanlama
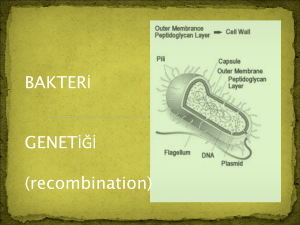
2. Bir Hücre Özütünün Hazırlanması
• Bakteri hücresi sitoplazmik zarla sarılıdır ve sert hücre duvarıyla çevrilmiştir
(peptidoglikan).
• E.coli’yi de kapsayan bazı türlerle, Hücre duvarının kendisi ikinci bir dış zarla
çevrilebilir. Bu bariyerlerin hepsi hücre bileşenlerinin salınması için
yıkılmalıdır.
• Kullanılan kimyasallar kullanılan bakteri türüne bağlıdır.
• E.coli gibi Gram(-) organizmalarda hücre zarını zayıflatma genellikle lizozim,
etilendiamin tetraasetat (EDTA) yada her ikisinin bileşimiyle meydana
getirilir.
Lizozim, yumurta beyazı, gözyaşı ve tükürük gibi salgılarda bulunan, hücre
duvarına katılığını veren polimerik bileşikleri sindiren bir enzimdir.
EDTA hücre zarının bütünsel yapısını korumak için elzem olan magnezyum
iyonlarını uzaklaştırır ve de DNA’ yı inhibe edecek enzimleri uzaklaştırır.
Sodyum dodesil sülfat, lizozim ve EDTA uygulamasını yeterli olmadığı
durumlarda ilave olarak kullanılır. Deterjanlar lipid moleküllerini
uzaklaştırmakla liziz sürecine yardım eder.
Şekil-7: Bir hücre özütünün hazırlanması
3. Bir Hücre Özütünden DNA’nın Saflaştırılması
DNA’ya ilaveten, bir bakteri hücre özütü önemli miktarda protein ve RNA içerir.
Saf DNA’yı bırakan çeşitli yöntemler, bu hücre kalıntılarından uzaklaştırmak için
kullanılabilir. Bir yaklaşım saf bir DNA çözeltisi bırakan hücre kalıntılarını yıkan
ajanlarla karışımı muamele etmektir. Diğer metodlar karışımı bileşenlerine
ayırmak için iyon-değiştirme kromotografisini kullanır, böylece DNA özütteki
proteinler ve RNA’dan uzaklaştırılır.
Şekil-8: a) Saf bir DNA çözeltisi bırakıp,hücre kalıntılarını yıkan kimyasallarla karışımı
muamele etmek b) Karışımı birisi saf DNA olan farklı fraksiyonlara ayırmak
Organik özütleme ve enzim sindirimiyle hücre kalıntılarının
uzaklaştırılması
• Bir hücre özütünü proteinlerden ayırmak için standart yol fenol ya da 1:1
fenol ve kloroform ilave etmektir. Bu organik çözücüler proteinleri çöktürür
fakat sulu çözeltide nükleik asitleri ( DNA, RNA) bırakır.
• Eğer hücre özütü çözücüyle yavaşça karıştırılır ve tabakalar sonra santrifüjle
ayrılırsa, sonuç çöken protein molekülleri sulu ve organik fazlar arasındaki
arafaz da beyaz bir pıhtı kütlesi bırakmalıdır.
• Sulu nükleik asit çözeltisi daha sonra bir pipetle uzaklaştırılır.
• Bazı hücre özütlerinde protein içeriği o kadar çoktur ki tek bir fenol
özütlemesi, nükleik asitleri tamamen saflaştırmak için yeterli değildir.
• Bu problem, birbirini izleyen birkaç fenol özütlemesi gerçekleştirmekle
çözülebilir. Ama bu her bir karıştırma ve santrifüjleme esnasında bir miktar
DNA kırılması ile sonuçlanacağı için sakıncalıdır.
ÇÖZÜM : Fenol özütlemesinden önce pronaz yada proteinaz K gibi bir proteazla
hücre özütünü muamele etmektir. Bu enzimler proteinleri fenol tarafından
daha kolay uzaklaştırılacak daha ufak polipeptitlere parçalar.
Şekil-9: Fenol özütlemesiyle protein bulaşkanlarının uzaklaştırılması
Bazı RNA molekülleri, özellikle elçi RNA (mRNA) fenol muamelesi ile
uzaklaştırılır, fakat çoğu sulu fazda DNA ile birlikte kalacaktır. RNA’yı
uzaklaştırmanın tek etkili yolu bu molekülleri ribonükleotid alt
birimlerine hızlı bir şekilde yıkan ribonükleaz enzimiyledir.
Bir hücre özütünden DNA’yı saflaştırmak için iyon - değiştirme
kromotografisinin kullanımı
Biyokimyacılar kimyasal karışımları farklı bileşenlerine ayırmada elektrik
yüklerindeki farklılıkları kullanmak için çeşitli yöntemler geliştirdiler. Bu
yöntemlerden biri, molekülleri bir kromotografi matriksi ya da rezinde bulunan
elektriksel yüklü parçacıklara bağlanma sıklıklarına bağlı olarak ayıran iyondeğiştirme kromotografisidir.
• DNA ve RNA’ nın her ikisi de bazı proteinler gibi negatif yüklüdür. Bu
nedenle pozitif yüklü rezine bağlanırlar.
• Elektriksel bağlantı tuz tarafından bozulur. Daha sıkı bağlanan moleküllerin
uzaklaştırılması daha yüksek tuz derişimlerini gerektirir.
• Tuz derişiminin kademeli olarak artırılmasıyla, molekülün farklı tipleri
rezinden birer birer ayrılabilir.
• İyon-değiştirme kromotografisini gerçekleştirmenin en basit yolu, rezini
plastik veya cam bir kolona yerleştirmek ve daha sonra hücre özütünü en
üste ilave etmektir. Özüt kolondan geçer. Bu özüt çok az tuz içerdiğinden,
tüm negatif yüklü moleküller rezine bağlanır ve kolonda tutulur.
Şekil-10: İyon-değiştirme kromotografisi ile DNA saflaştırma
4. DNA numunelerinin derişimi
Organik özütleme, çoğunlukla fazla derişik yapma gereği olmayan
çok yoğun bir DNA çözeltisiyle sonuçlanır. Diğer saflaştırma
metotları bazen daha seyreltik çözeltiler verebilir ve bu yüzden
DNA derişimini artırıcı metotları düşünmek önemlidir.
• En sık kullanılan derişim metodu etanol ile çöktürmedir. Tuzun
varlığında (Na iyonları gibi monovalent katyonlar) ve -20°C yada
daha düşük sıcaklıklarda mutlak etanol, polimerik nükleik
asitleri etkili bir şekilde çöktürür. Yoğun bir DNA çözeltisiyle,
etanol moleküllerin arafazda çökmesine yol açıp numunenin üst
kısmında tabakalanabilir.
• Harikulade bir marifet, DNA çözeltisindeki etanole bir cam
çubuk sokmaktır. Çubuk geri çekilince, DNA molekülleri etrafına
yapışır ve uzun bir lif şeklinde çözeltiden uzaklaştırılabilir.
Şekil-11: Etanol çöktürmeyle DNA’yı toplama
• Alternatif olarak, etanol seyreltik bir DNA çözeltisiyle karıştırılırsa, çözelti
santrifüjle toplanabilir ve daha sonra uygun bir hacim suda yeniden
çözünür.
• Etanol çöktürmesi, kısa zincirli ve monomerik nükleik asit bileşenlerini
çözeltide bırakan ek avantaja sahiptir. Ribonükleaz muamelesi sonucu
oluşan ribonükleotidler bundan dolayı bu safhada kaybolacaktır.
5. DNA derişiminin ölçülmesi
• Yapılan deneylerde çözeltide tam olarak ne kadar DNA’nın bulunduğunu bilmek
önemlidir. DNA derişimleri ultraviyole(UV) absorbans spektrofotometresi ile
hassas olarak ölçülebilir. DNA çözeltisi tarafından absorbe edilen ultraviyole
ışınlarının miktarı, numunedeki DNA miktarıyla doğrudan orantılıdır. Genellikle
absorbans, 1.0 absorbanslık ( A260) dalga boyu her ml’deki 50µg çift iplikli DNA’ ya
yaklaşık gelen 260 nm’ de okunur.
• Ultraviyole absorbansı hazırlanan DNA’ nın saflığını ölçmek için de kullanılabilir. Saf
bir DNA numunesinin 260nm ve 280 nm (A260/A280)’deki absorbanslarının oranı 1.8
dir. 1.8 den daha düşük olanlar, hazırlanan DNA’nın fenol yada proteinle bulaşık
olduğunu gösterir.
Total Hücre DNA’sının Hazırlanması için Diğer
Metotlar
DNA’sına gerek duyulacak olan tek canlı bakteriler değildir. DNA’yı
saflaştırmanın temel işlemleri hangi organizma olduğuna bakılmaksızın aynı ise
de kullanılacak olan hücrelerin bazı özel yapıları dikkate alınarak bazı
değişiklikler yapılabilir.
Besbelli sıvı ortamda hücrelerin büyümesi sadece bakteriler, diğer
mikroorganizmalar, bitki ve hayvan kültürleri için uygundur. Bununla beraber
hücreyi parçalama safhasında ana modifikasyonlara ihtiyaç olması
muhtemeldir.
Bakteri hücrelerini parçalamak için kullanılan kimyasallar genellikle diğer
canlılarda işlev görmez. Örneğin; lizozimin bitki hücreleri üzerinde etkisi
yoktur. Pek çok hücre duvarı tipleri için spesifik enzimler vardır, ama
çoğunlukla bir havan yada havanda donmuş materyali ögütme gibi fiziksel
teknikler çok daha randımanlıdır. Hücre duvarı ihtiva etmeyen canlılarda bu
işleme gerek yoktur ve sadece bir SDS ile muamele ederek liziz edilebilirler.
Diğer önemli hususta DNA’nın özütlendiği hücrenin biyokimyasal içeriğidir. Pek
çok bakteride, hücre özütünde var olan ana biyokimyasallar protein, DNA ve
RNA’dır, bu yüzden ribonükleazla RNA’yı uzaklaştırdıktan sonra fenol özütleme
ve / veya proteaz muamelesi saf bir DNA numunesi bırakır.
Bitki dokuları, çoğunlukla fenol özütlemeyle uzaklaşmayan yoğun miktarda
karbonhidrat içerdikleri için bu bakımdan özellikle zordur. Bunun yerine farlı bir
yaklaşım kullanılmalıdır.
DNA, DNA molekülleri ve silika arasındaki etkileşimi kararsız yapan, su eklenmesiyle
yeniden kazanılır.
Bir metod
Nükleik asitlerle çözünmez bir kompleks oluşturan setiltrimetilamonyum
bromür (CTAB) denilen bir deterjandan yararlanmaktır. CTAB bir bitki hücresi
özütüne ilave edildiğinde, nükleik asit - CTAB kompleksi, süpernatantta
karbonhidrat, protein ve diğer bulaşkanları bırakarak çökelir. Çözelti daha sonra
santrifüjle toplanır ve kompleksin yıkılmasına neden olan 1 M sodyum klorürde
yeniden çözündürülür. Nükleik asitler artık etanol çöktürmeyle deriştirilebilir ve
RNA ribonükleaz muamelesi ile uzaklaştırılabilir.
Şekil-12: Bitki DNA’sının saflaştırılması için CTAB metodu
PLAZMİD DNA’SI İZOLASYONU
• Nükleik asitler tüm organizmalardan ve hücre materyallerinden izole
edilebilir. Nükleik asitler bulundukları organizmaya göre farklı
yöntemlerle izole edilebilir. Genomik DNA veya RNA bitki, hayvan ve
mantar hücrelerinden izole edilebilir. Plazmid DNA ise bakteri ve
maya hücrelerinden hücre materyalinin miktarına bağlı olarak farklı
şekillerde izole edilir.
Plazmidlerin rekombinant DNA teknolojisi çalışmalarında taşıyıcı DNA
(vektör) olarak geniş çapta kullanılması plazmid izolasyon yöntemlerinin
geliştirilmesine yol açmıştır.
Plazmidler bakterinin üremesi için gerekli olan temel genleri taşımazlar.
Buna karşılık;
• Bakteriye uygun olmayan ortam koşullarında yaşayabilme
• Çeşitli toksik maddeler üretme
• Toksik maddeleri metabolize edebilme
• Antibiyotiklere dirençlilik ve antibiyotik sentezleyebilme
• Patojen özelliği kazandırma
• Bazıları bakteriye eşey özelliği sağlayabilme
gibi nitelikleri kazandıran genleri içerir.
Hücre içerisinde boyutları ve kopya sayıları çeşitlilik gösteren birden
fazla farklı tipte plazmid bulunabilir.
PLAZMİD İZOLASYONU İÇİN GEREKLİ MALZEMELER
1. 1-5 ml gece boyu büyüyen hücre kültürü
2. Santrifüj
3. Otoklavlanabilir bakteri atık kabı
4. Farklı deterjan ve tamponlar
5. Steril ependorf tüpleri
6. Buz içeren kap
DENEYİN YAPILIŞI
• Gece boyu büyüyen bakteri hücrelerinin toplanması için hücreler
4000 rpm’de 5 dakika santrifüj yapılır.
• Santrifüj yapıldıktan sonra tüpün dibinde hücre peleti görülmelidir.
• Süpernatant kısmı atık kabına atılır.
• Süpernatant kısmı atıldıktan sonra tüp ters çevrilir ve tüpün içinde
kalan süpernatantın uzaklaşması beklenir.
• Bakteri hücrelerinin üzerine 250 μl süspansiyon tamponu
eklenir.
• Süspansiyon tamponu RNA fargmanlarının parçalanması için RNaz
içermektedir.
• Süspansiyon tamponu ile hücre peleti pipetaj yapılarak iyice karışması
sağlanır.
Hücre süspansiyonu küçük reaksiyon tüpüne aktarılır.
• Süspansiye haldeki hücre peleti üzerine 250 μl liziz tamponu eklenir.
• Liziz tamponu sodyum dodesilsülfat ve sodyumhidroksit içerir içerir.
Sodyum dodesil sülfat hücre duvarını yıkar, sodyumhidroksit ise
proteinleri ve genomik DNA’yı denature eder.
• Liziz tamponu eklendikten sonra tüp yavaşça 5 kez ters çevrilir.
• Oda sıcaklığında 5 dakika inkübasyon yapılır.
PLAZMİD DNA’NIN HÜCRE DEBRİSİ VE GENOMİK
DNA’DAN UZAKLAŞTIRILMASI
• Hücre süspansiyonu üzerine 350 μl bağlanma tamponu
eklenir.
• Tüp 5 kez yavaşça ters çevrilir.
• Bağlanma tamponu potasyum asetat içerir ve denature proteinlerin
çökelmesini sağlar.
• Tüp 5 dakika buz üzerinde bekletilir.
• Buz üzerinde inkübasyon sonrası 13000 rpm’de 10 dakika santrifüj
yapılır.
• Santrifüj sonunda beyaz ve grimsi bir pellet oluşur. Bu pellet hücre
debrisini ve genomik DNA kısmını içerir.
• Tüpün içinden plazmid DNA içeren süpernatan dikkatlice alınarak
filtreli tüpe aktarılır .
• Toplama tüpü içinde bulunan filtreli tüp 13000 rpm’de 1 dakika
santrifüj yapılIır.
PLAZMİD DNA SAFLAŞTIRILMASI
• Toplama kabındaki süpernatant kısmı uzaklaştırılır.
• Filtreli tüp üzerine 500 μl yıkama solüsyonu I eklenir.
• Yıkama solüsyonu, filtrede kalan tüm tuzları, proteinleri ve hücresel atıkları
uzaklaştırır.
• Daha sonra en yüksek hızda 1 dakika santrifüj yapılır.
• Santrifüj sonunda toplama kabında bulunan süpernatant uzaklaştırılır.
• 700 μl yıkama solüsyonu II eklenir.
• Daha sonra en yüksek hızda 1 dakika santrifüj yapılır.
• Toplama kabındaki süpernatan uzaklaştırılır.
• Daha sonra tüp boş olarak en yüksek hızda 1 dakika santrifüj yapılır.
SAFLAŞTIRILAN PLAZMİD DNA’NIN ELÜSYONU
• Santrifüj sonunda toplama tüpünde kalan süpernatant uzaklaştırılır.
• Filtreli tüpün üzerine filtreye değmeyecek şekilde 100 μl elüsyon
tamponu eklenir.
• En yüksek hızda 1 dakika santrifüj yapılır.
• Santrifüj sonunda toplama tüpünde saflaştırılan plazmid DNA
bulunur.
ORGANEL DNA’SI İZOLASYONU
• Ökaryotlarda nükleus DNA’sından • Boyutu değişi organizmalarda
bağımsız kalıtım gösteren organel farklılık göstermektedir.
hücrelerinde
DNA’larının varlığı 1900’lü yılların • Hayvan
mtDNA’sı yaklaşık 16.5 kb
başlarında gösterilmiştir.
• Mitokondri DNA’sı (mtDNA) ve büyüklüğünde, buna karşılık
kloroplast DNA’sı (ctDNA) kendi maya hücrelerinde 17-84 kb
değişmektedir.
işlevleri için gerekli bütün RNA arasında
türlerini ve bazı proteinleri Bitkilerde ise minumum 100
şifreleyen
genetik
bilgiyi kb’den başlamıştır.
taşımaktadırlar.
• Mitokondri DNA’sı çift zincirli
halkasal bir moleküldür. (basit
yapılı birkaç ökaryotta doğrusal
olduğu saptanmışır.)
• Kloroplast
DNA’sı
da
mtDNA’sı gibi çift zincirli
halkasal bir moleküldür.
• Boyutu oldukça büyüktür.
• Gelişmiş bitkilerde yaklaşık
140 kb iken basit yapılı
olanlarda 200 kb’ ye kadar
olabilmektedir.
• Kloroplast genomunda bütün
rRNAve tRNA türleri ile RNA
polimerazı, bazı ribozomal
proteinleri ve birkaç yapısal
proteini şifreleyen yaklaşıl 50
kadar gen bulunmaktadır.
Organel DNA’sı izolasyonlarında en önemli aşama öncelikle
organelin parçalanmamış şekilde ayrılması olduğundan dolayı,
bu olay 2 aşamada gerçekleştirilir.
***Organelin izolasyonu
***Organel DNA’sının izolasyonu
Mitokondriyal DNA’nın
saflaştırılması
Mitokondri İzolasyonu
Materyal: Somatik hibritlerin çeşitli bitki
dokuları
Taze dokular (yaprak, çiçek
vb.) buzda soğutulmuş
uygun tampon içinde
parçalanır.
Plastitlerin uzaklaşması için
süpernatant 2600 ×g’de 15’
da 2 kez ve bir kez de 10’
santrifüj edilir..
mitokondrileri içeren
çökelti buzda soğutulmuş
uygun tampon içinde
çözündürülür.
Naylon bir membrandan (por
çapı yaklaşık 10µm) filtre
edildikten sonra büyük hücre
parçalarının uzaklaştırılması için
500×g’de 10’ dakika santrifüj
edilir.
lizis olmuş nükleus içeren üst
sıvı atılır ve mitokondrileri
çöktürmek için 14.500 ×g’de
15’ santrifüj edilir.
Mitokondri çökeltisi sıvı azotta
dondurulduktan sonra -80°C
saklanır yada doğrudan DNA
izolasyonu yapılabilir.
MİTOKONDRİ DNA İZOLASYONU
2.
1. MİTOKONDRİYAL VE DİĞER MEMBRANLARIN LİZİZ EDİLMESİ
PROTEİNLERİN FENOL/KLOROFORM GİBİ ÇÖZELTİLERLE UZAKLAŞTIRILMASI
3. ETANOL İLE DNA’NIN ÇÖKTÜRÜLMESİ
4. DNA’NIN SAFLIĞI VE KALİTESİNİN TESPİTİ
DNA ANALİZİ
• Nükleik asitlerin nanogram veya mikrogram düzeyindeki miktarlarının
belirlenmesi, moleküler biyoloji alanında çalışan araştırıcılar için temel
noktalardan biridir.
• Genellikle izole edilen DNA’ların miktar tayininde absorbsiyon temeline
dayanan spektrofotometrik yöntemler kullanılır.
• Nükleik asitlerin doğrudangörüntülenmesinde veya özgün dizilerde kesim
yapan restriksiyon endonükleaz enzimlerinin etkisi sonucu oluşan farklı
boyutlardaki DNA parçalarının saptanmasında elektroforetik yöntemler
kullanılır.
DNA ANALİZ YÖNTEMLERİ
SPEKTRAL YÖNTEMLER
ELEKTROFORETİK YÖNTEMLER
DNA’NIN ENZİMATİK KESİMİ
SPEKTRAL YÖNTEMLER
• Nükleotidlerin heterosiklik halkaları 260 nm dalga boyunda
maksimum absorbsiyon özelliği gösterir.
• Bu nedenle 260 nm’de ölçüler absorbsiyon değerleri (A260) oldukça
saf olarak izole edilen nükleik asitlerin mikrogram düzeyinde
miktarının belirlenmesinde kullanılır.
• Çift zincirli DNA molekülleri için, 1 optik dansitenin (OD) 50µg/ml’ye
karşılık geldiği bilinmektedir. Buna göre çift zincirli DNA
belirlenmesinde aşağıdaki formül kullanılır.
DNA (µg/ml) ₌ A260 x sulandırma oranı x 50
• 260 ve 280 nm dalga boylerında okunan değerler arasındaki oran
nükleik asitlerin saflığı hakkında bilgi vermektedir.
• Proteinlerde 280 nm de absorbans gösterirler.
• Saflaştırılmış DNA’ da A260/280 oranı yaklaşık 1.75-1.8’in üzerinde
olmalıdır.
Bu nedenle 280 nm’de ölçülen bir değerdeki artış bu oranda düşmeye
neden olur bu da safsızlığın bir karşılığıdır.
ELEKTROFORETİK YÖNTEMLER
• Tüm laboratuvarlarda rutin olarak kullanılan en basit
yöntemlerden biri jel elektroforezidir.
• Yöntemin avantajları basit ve hızlı olması ve ayrıcadiğer
yöntemlerle yeterli düzeyde ayrılmayan DNA fragmentlerinin
ayrılabilmesini sağlamasıdır.
• UV ışığı altında fluoresan etki gösteren etidyum bromür(EB)
boyasının kullanımı ile çok düşük konsantrasyonlarda ( 1- 10 ng )
olsa bile, DNA’nın jel üzerindeki yerini belirlemek mümkündür.
• DNA’nın elektroforetik analizinin temeli; bu molekülün elektriksel
bir alanda jel üzerindeki göçüne dayanır.
Bu göç hızı molekülün; büyüklüğüne, yapısına, jelde kullanılan
maddenin konsantrasyonuna, iyonik kuvvete uygulanan akıma bağlı
olarak değişmektedir.
ELEKTROFORETİK YÖNTEMLER
AGAROZ JEL ELEKTROFOREZİ
PULSE FİELD JEL ELEKTROFOREZİ
POLİAKRİLAMİD JEL ELEKTROFOREZİ
İKİ BOYULTU ELEKTROFOREZ
İZOELEKTRİK FOCUSİNG
KILCAL ELEKTROFOREZ
İMMÜNOELEKTROFOREZ
AGAROZ JEL ELEKTROFOREZİ
• Agaroz, bir kırmızı alg türü olan Agar agar’dan izole edilen doğrusal
bir polisakkarittir.
• Agaroz sıcak suda çözünür ve soğutulduğu zaman polimerde karşılıklı
hidrojen bağlarının oluşumu ile jel yapısı oluşur. Bu oluşum geri
dönüşümlüdür.
• Agaroz konsantrasyonu % 0.5- 1.5 arasında değiştirilerek jelin por çapı
ayarlanabilir.
• Düşük DNA fragmentleri için yüksek, büyük DNA fragmentleri için düşük
agaroz konsantrasyonu kullanılarak DNA’nın jelde uygun şekilde
yürümesi sağlanabilir.
• DNA’nın jelde görünğr hale gelebilmesi etidyum bromürün DNA bağları
arasına bağlanarak 300-360 nm’de ışığı absorblaması sonucu fluoresan
etki göstermesi ile olur (Bu etki DNA konsantrasyonuna bağlı
değişebilir).
İzole edilen DNA’nın genomik ya da plazmid DNA’sı omasına göre jeleki
görünümleri farklılık gösterir.
Genomik DNA keskin bir bant ile bu bandın aşağı ve yukarı kısmına doğru
yayılan bir görüntü verir.
Plazmid DNA’sının jeldeki görüntüsünde genellikle üç farklı biçimi gözlenir;
1. Süper sarmal biçim
2. Gevşek sarmal biçim
3. Doğrusal biçim
• Doğrusal biçim izolasyon sırasındaki kırılmalardan dolayı oluşur.
• Eğer saflaştırma işlemi doğru bir biçimde yapılmış ise jelde sadece süper
sarmal ve gevşek sarmal formlar gözükecektir.
• Molekül ağırlıkları aynı olmasına rağmen bu üç formun jeldeki göçleri
farklıdır. Bu farklılık; agaroz konsantrasyonuna, uygulanan akıma, tamponun
iyonik kuvvetine ve form I’in yoğunluğuna da bağlıdır.
• Optimize olmuş koşullarda form I genellikle diğerlerine göre daha hızlı
hareket eder.
AGAROZ JEL ELEKTROFOREZİ
Gerekli Malzemeler
Agaroz
TBE ( Tris- borat ) Tamponu
TAE ( Tris – asetat ) Tamponu
TE Tamponu
Yükleme Tamponu
( sükroz, bromfenol mavisi, su )
Elektroforez Gereçleri
Agaroz Jelin Hazırlanması
Agaroz jeller toz halindeki agar ile tampon çözeltilerin uygun miktarda
karıştırılması ile hazırlanır.
Agaroz oda ısısında çözünmez. Kaynatma yolu ile (
mikrodalga, otoklavlama veya ateş üzerinde ) çözdürülür.
Elle tutulabilecek sıcaklığa düştüğünde ( 55-50 °C ) 0.5
µg/ml etidyum bromür ilave edilir.
Kenarları kapatılmış cam veya özel yüzeyler üzerine, sızıntı
olmamasına dikkat edilerek dökülür.
Cepleri oluşturacak tarak yerleştirilerek donması beklenir.
Agaroz jel 30-35 dk polimerize olarak kullanıma hazır hale
gelir
Dikkatlice bantlar ve tarak çıkarılarak tanka yerleştirilir.
Yükleme Örneklerinin Hazırlanması
Jeldeki cebin büyüklüğüne göre izole edilen ve TE içinde bulunan DNA
solüsyonundan alınır.
üzerinde Bromophenol Blue (BB) eklenir. ( genellikle 1/6 hacimde )
10 saniye mikrosantrifüjde sıvının tüp dibine toplanması sağlanır.
Tüm sıvı mikropipet yardımıyla jele yüklenir.
5 V/cm olacak şekilde akım geçirilir.
DNA fragmentlerinin yükleme tankındaki hareketi.
Sürenin sonunda jel bir transilüminatör üzerine alınır ve UV
ışığı altında fragmentlerin boyutları standartlarla
karşılaştırılarak belirlenir.
PULSE FİELD JEL ELEKTROFOREZİ
• Yaklaşık 1 megabazdan (Mb) daha büyük doğrusal çift iplikli DNA
molekülleri agaroz jelde aynı hızda göç ederler. Bunun nedeni, jelin
por büyüklüğünün doğrusal DNA’nın jelde göç edebilmesi için yeterli
olmamasıdır.
• Bu problem 1984 yılında geliştirilen ve 5 Mb boyutundaki DNA
parçalarınıda ayırabilen ‘’pulse field ‘’ jel elektroforez tekniği ile
ortadan kaldırılmıştır.
• Bu yöntemde DNA molekülleri belirli zaman aralıkları da birbirlerine
farklı açıda iki elektriksel alan etkisinde bırakılır.
• Küçük moleküller elektriksel alan değişimlerine daha çabuk uyum
sağladıkları için daha hızlı hareket ederler.
• Bu sistemde dikey elektrodların yanında farklı konfigürasyonlarda
elektrodlar da kullanılmaktadır.
• Bu yöntemde kromozomları jelde ayrı ayrı görebilmek mümkündür.
DNA’NIN ENZİMATİK KESİMİ
• DNA’nın enzimatik kesimi restriksiyon endonükleazları (RE) kullanımı
ile yapılır.
• RE enzimleri, kısa DNA dizilerini özgül olarak tanıyan ve bu dizilimlere
yakın bölgelerden veya bu dizilimler içindeki spesifik bölgelerden
DNA’yı kesen yapılardır.
• Günümüzde 300’e yakın farklı DNA dizilimini tanıyan yaklaşık
3000’den fazla RE varlığından söz edilmektedir. RE enzimlerinin çok
büyük bir kısmı bakterilerden, çok az bir kısmı da virüs ve
ökaryotlardan izole edilmiştir.
• RE’ların doğal biyolojik fonksiyonu, bakteriyel savunma
mekanizmasında oynadıkları roldür. Bakteriye giren yabancı DNA’ları
da kesebildiklerinden, intrasellüler bakteriyel patojenleri inaktive
edebilmekte ve bakteriyi virüslerden ve yabancı DNA’lardan
korumaktadırlar.
DNA’NIN ENZİMATİK KESİMİ
• RE enzimleri, kısa DNA dizilerini özgül olarak tanıyan ve bu
dizilimlere yakın bölgelerden veya bu dizilimler içindeki spesifik
bölgelerden DNA’yı kesen yapılardır.
• Günümüzde 300’e yakın farklı DNA dizilimini tanıyan yaklaşık
3000’den fazla RE varlığından söz edilmektedir.
• RE enzimlerinin çok büyük bir kısmı bakterilerden, çok az bir kısmı
da virüs ve ökaryotlardan izole edilmiştir.
• 1970’li yıllardan sonra restriksiyon endonükleaz kullanımına bağlı
olarak rekombinant DNA teknolojisi hızla gelişmiş ve bu gelişme
seçilen bir genin çoğaltılmasını, genin kodladığı proteinin
üretilmesini, genin diziliminin belirlenmesini vb., mümkün hale
getirmiştir. Bu teknolojideki merkezi konumu nedeniyle, RE
enzimleri özellikle klonlama
çalışmaları yapan araştırma
laboratuvarlarında sıklıkla kullanılmıştır.
RE’lerin Kullanım Alanları
Rekombinant DNA elde edilmesi
DNA haritası çıkarılması
Polimorfizmlerin belirlenmesi
Probların hazırlanması
DNA modifikasyon durumlarının analizi
İSİMLENDİRME
• İsimlendirmede önce enzimin elde edildiği bakteri cinsinin
ilk harfi, daha sonra bakteri türünün ilk iki harfi ve son
olarak da soya ait bir harf ile ilk izolasyondan başlayarak
Romen rakamı ile enzimin izolasyon sırası belirtilir.
• EcoR I E = genus Escherichia
Hind
III
H
=
genus
Haemophilus
in = species influenzae
d = strain Rd
III = third RE to be isolated
from this species
• co = species coli
• R = strain RY 13
• I = first RE to be isolated from this species
RE’ların DNA’ya BAĞLANMA ve KESME
MEKANİZMALARI
• RE’lar DNA tanıma bölgesi ve katalitik alan olmak üzere iki
fonksiyonel alt birimden oluşmaktadır.
• DNA tanıma bölgesi spesifik bölgeyi tanır ve katalitik alanı
buraya yerleştirir.
• Tanıma sekansına yerleşen katalitik alan heliksin fosfodiester
bağlarını kırar.
• RE’lar,
çift
sarmal
DNA’ya
tanıma
bölgelerinden
bağlanabildikleri gibi, tanıma bölgeleri dışından da
bağlanabilmektedirler.
• Tanıma bölgeleri dışından bağlandıktan sonra bu enzimler,
çizgisel DNA boyunca kaymaktadırlar.
• Bu işlem esnasında DNA ile enzim arasını su molekülleri
doldurmaktadır. Enzim tanıma bölgeleri bulunduğu zaman su
moleküllerinin pek çoğu uzaklaştırılmaktadır.
• Enzim-DNA kompleks formunda, hem enzimde hem DNA
dizilerinde konformasyonel değişiklikler meydana gelmektedir.
• RE’lar sadece bazlar arasında yatay konumda bulunan fosfodiester
bağlarını kırarlar.
• Karşılıklı iki baz arasındaki hidrojen bağlarının kesilmesinden
sorumlu değildirler.
• Hidrojen bağları, fosfodiester bağlarının kırılmasıyla ve çözeltideki
termal hareketten doğan enerjinin etkisiyle kendiliğinden kırılırlar.
• Farklı RE’lar aynı tanıma sekansına sahip olabilirler. Aynı sekansı
tanıyan ve farklı organizmalardan elde edilmiş RE’lara izoşizomer
denir.
• İzoşizomerler sıklıkla farklı optimum reaksiyon koşullarına ve
stabiliteye sahiptirler.
• İzoşizomerler aynı sekansı tanımalarına karşın, kesimi sekansın
farklı bölgelerinden de yapabilirler. Bunlara ise neoşizomerler
denir.
RE’ların TEPKİME ŞARTLARI
• RE’lar gerek uzun süreli saklanırken, gerekse aktivite gösterirken
uygun şartlara ihtiyaç duymaktadırlar.
• Bir enzimden en iyi şekilde yararlanabilmesi için gerekli şartlar
üretici firmalar tarafından kullanıcıya bildirilmelidir. RE’larla
çalışırken, bu şartlara uyulmadığı takdirde sıkça problemlerle
karşılaşılır.
• Enzimlerin star aktiviteleri, DNA ve enzim konsantrasyonunun
uygun olmaması, pH ve iyonik dengenin uygun olmaması, çalışılan
enzimin diğer enzimlerle kontaminasyonu gibi problemler uygun
olmayan kesimlere neden olabilmektedir.
1. Tampon kompozisyonu: Tampon çözeltisinin fonksiyonu yeterli
iyonik gücü(tuz konsantrasyonu), major katyonları( sodyum,
potasyum ) ve uygun pH ortamını oluşturmaktır. Pek çok RE
genellikle pH8.0’de aktiftir. RE’ların çoğu 50-150 mM NaCl veya KCl
ortamında kesim yapmaktadır.
2. Enzim kofaktörleri: Ticari olarak mevcut RE’lar
kofaktörolarak sadece magnezyuma (Mg) ihtiyaç
duymaktadır. Diğer divalentkatyonların varlığı problemlere
neden olmaktadır.
3. Gliserol:RE’lar: -20°C’de saklanırken saklama tamponu
içerisine gliserol(%50) katılmaktadır. Bu, enzimin donmasını
engellemektedir. Böylece, enzimin dondurulup çözülmesi
sırasında göreceği zarar önlenmektedir. Çoğu RE için çalışma
sırasında son konsantrasyonda % 5’ten fazla gliserol
istenmemektedir.
4. İnkübasyon sıcaklığı: Çoğu RE maksimum aktivitesini 37
°C’degöstermektedir. Fakat daha düşük veya daha yüksek
sıcaklıklarda aktivitelerini gösteren RE’larda vardır. Ör: ApaI
→30 °C, BclI →50 °C, TaqI →65 °C
5. Enzim konsantrasyonu: 1 aktivite ünitesi, 1μg DNA’yı
50 μL total reaksiyon hacmi içinde 1 saatte hidrolize
edebilen
enzim
miktarıdır.
Kullanılan
enzim
konsantrasyonları substrata göre ayarlanmakla birlikte,
çok yüksek enzim konsantrasyonları star aktiviteye
neden olabilmektedir.
6. Substrat konsantrasyonu: Substrat olarak kullanılan
DNA’nın miktarı RE kesimini etkilemektedir. Az bir
hacim içerisinde çok miktarda DNA bulunması enzimin
difüzyonunu engellemekte ve etkinliğini düşürmektedir.
Çok düşük DNA konsantrasyonları da kesimin verimini
etkilemektedir.
VİDEO
STAR AKTİVİTE
• RE’ların özelliklerinden en dikkate değer olanı, bu enzimlerin
optimal şartlarda özgül DNA’yı en yakın dizilimden kesebilme
başarılarının optimal olmayan şartlarda oldukça değişmesidir.
Optimal olmayan şartlarda enzimin tanıma sekansına olan
spesifitesi değişmektedir.
Örneğin; BamHI enzimi için tanıma sekansı (G↓GATCC) iken,
optimalolmayan şartlarda (G↓GATCN) veya (G↓RATCC) şeklinde
benzer bölgelerden de kesim yapabilmektedir. Bu duruma “star
aktivite”veya “relaxedspecificity”denilmektedir.
• Bu durum, çalışmalarda oldukça önemli olmakta ve çalışmanın
başarısında belirleyici konuma gelebilmektedir. Bu nedenle,
kullanılan RE’ların star aktiviteye sahip olup olmadıkları bilinmeli,
Star aktiviteye neden olan durumlar
Yüksek gliserol konsantrasyonu ( > % 5 v/v )
Çok yüksek enzim konsantrasyonu (genellikle > 100 U/μg
DNA )
Düşük iyonik güç ( < 25 mM )
Yüksek pH ( genellikle > 8.0 )
Organik maddelerin varlığı (DMSO, etanol, dimetilasetamid
vb.)
Kofaktör Mg’un yerine diğer divalent katyonların varlığı (
Mn+2,Cu+2 vb.)
RE’ların SINIFLANDIRILMASI
RE’lar; metilaz aktivitelerine, alt ünite yapılarına, kesim
özgüllüklerine
ve
kofaktöri
htiyaçlarına
göre
sınıflandırılmışlardır.
Tip I RE’lar: Endonükleaz aktiviteleri için ATP, S-adenozilmetionin ve
Mg+2’a ihtiyaç duyarlar.
• Bilinen tüm tip I RE’lartanıma sekansındaki adenin rezidülerini
metilasyona uğratmaktadır.
• Bu enzimler tanıma sekanslarına bağlanmalarına rağmen, kesimleri
sekans dışında tesadüfi olarak gerçekleştirmektedirler. 3 alt
üniteden oluşurlar. Birincisi, tanıma sekansını tanır; ikincisi, adenin
rezidülerini metiller; üçüncüsü ise kesimden sorumludur.
Tip II RE’lar: RE’lar denildiğinde ilk akla gelen ve en çok çalışılan gruptur.
İzole edilen RE’ların çok büyük kısmı bu gruptadır. Çünkü tip II RE’lar, tam
hedef nükleotitten veya çok yakınından kesim yapma özellikleri
nedeniyle araştırmalar için ideal enzimlerdir.
• Mg+2 iyonlarının varlığında çift zincir DNA üzerindeki
palindromiksekansları tanır ve bu sekans içindeki özel bölgeden kesim
yaparlar.
• Kesimleri ATP’ye bağlı değildir.
• Restriksiyon fragmanları ve jelde bandpaternleri oluşturmaları
bakımından diğer tip RE’lara göre çok üstündürler ve hemen hemen
sadece bu grup RE’larla çalışılmaktadır.
Tip III RE’lar: Tip I RE’lar gibi metilasyon modifikasyon fonksiyonuna
sahip olup, Mg+2 ve ATP’ye bağlı kesim gerçekleştirirler.
• Çok altüniteli enzimlerdir ve tam bir kesim yapma özellikleri zayıftır.
• DNA’ya tanıma sekanslarından bağlanmalarına rağmen, kesimi tanıma
bölgesinden farklı bir yerden gerçekleştirirler.
Homing endonükleazlar: Protein yapıları bakımından diğer RE’lardan
farklılık gösteren, uzun ve asimetrik bölgeleri tanıyıp kesen, aktivitesi
için protein ve RNA’ya ihtiyaç duyan enzim grubudur.
• Daha az tanıma özgüllüğü göstermekte ve tanıma bölgelerindeki tek
baz değişimlerini tolere edebilmektedirler.
Nicking endonükleazlar: RE’lar çift zincir DNA’ya bağlanıp kesim
yaparlar. Tek zincire bağlanıp endonükleaz aktivitesi gösteren enzim
grubuna da “nicking” endonükleazlar denilmektedir.
DNA’nın Kısmi Kesilmesi
• Bu yöntem özellikle genom kitaplığı kurulması sırasında veya
istenilen boyuttaki DNA fragmentlerini elde etmek amacıyla
kullanılır.
• Kısmi kesilme, bir RE’nin bir DNA molekülündeki az sayıda hedef
noktalarını tanıması ile sağlanır.
• İstenen boyuttaki DNA fragmentlerini verecek enzim dozu ya enzim
konsantrasyonu sabit tutularak inkübasyon süresinin, ya da
inkübasyon süresi sabit tutularak enzim konsantrasyonunun
değiştirilmesi ile belirlenir.
DNA’nın Jelden Geri Alınması
DNA’nın jelden geri kazanılmasına yönelik oldukça farklı yöntemler
geliştirilmiştir.
Bu yöntemlerle istenilen boyuttaki DNA fragmentlerini saf olarak elde etmek
veya DNA’yı herhangi bir aşamada saflaştırmak olasıdır. Bunula beraber
uygulamada başarılı sonuç alınmasını güçleştiren bazı noktalar vardır.
Bu olumsuzluklar aşağıda açıklanmıştır.
1. Saf olmayan agaroz kullanımı. DNA’nın jelden geri kazanılması sırasında
agaroz içindeki yabancı maddelerin DNA solüsyonunda bulunması sonaki
asamalarda kullanılacak olan enzimleri inhibe etmektedir.
2. Büyük fragmentlerin jelden geri kazanılmasındaki güçlük. Genellikle 5
kb’den daha küçük fragmentlerin geri kazanımı başarılı olurken büyük
fragmentler aynı başarı ile izole edilemezler.
3. Düşük konsantrasyonda DNA kullanımı. Eğer az miktarda DNA jele
yüklenmişse geri kazanım sırasında önemli kayıplar olabileceğinden 500
ng’dan az miktardaki DNA ile işleme başlamamak yararlı olur.
DNA’nın geri kazanılmasına yönelik geliştirilmiş yöntemler şu
şekilde sıralanabilir:
1. Ticari olarak üretilen küçük ‘‘sepharacyl’’ seferasil kolonlarla
yapılan saflaştırma. Üretici firmanın önerdiği tamponlar
kullanılarak istenilen boyuttaki DNA’yı içeren jel parçaları kolona
yüklenir ve DNA’nın kolona bağlanması sağlanır. Daha sonra
elüsyon tamponu kullanılarak DNA kolondan geri alınır.
2. Düşük sıcaklıkta eriyebilen agaroz kullanılarak saflaştırma.
Agaroza hidroksietil grupları sokularak yaklaşık 30°C’da donması ve
65°C’ın altında erimesi sağlanır. Bu özellikle agaroz
kullanılarakistenen DNA’yı içeren jel parcası kesilip eritildikten
sonra fenol/kloroform ekstraksiyonu ve etanol çöktürmesi
sonucunda DNA saf olarak elde edilir.
3. Elektroelüsyon. DNA fragmentlerini içeren agaroz parçası, içinde
yürütme tamponu bulunan diyaliz tüpüne konur ve elektriksel alana
bırakılır. DNA’nın jelden ayrılıp tampona geçmesi bir süre beklenir.
DNA’nın tamamının tampona geçip geçmediği UV ışığı altında kontrol
edilir. Etidyum bromürün izoamil alkol kullanılarak uzaklaştırılmasını
izleyen çöktürmeden sonra DNA saf olarak elde edilir.(video)
4. Gene Clean yöntemiyle DNA’nın geri kazanılması. Oldukça başarılı
geri kazanımın yapıldığı bu yöntemde, DNA’nın içinde bulunduğu
agaroz jel eritilir ve toz halinde cam boncuk solüsyonu ‘’glass milk’’
örneğe eklenir. DNA cam boncuklara yapışır, diğer maddeler
santrifüjleme ile uzaklaştırılır. DNA elüsyon tamponu veya distile su
kullanılarak cam boncuklardan ayrılır ve etanol ile çöktürülür.