T.C.
Ege Üniversitesi
Dişhekimliği Fakültesi
Ağız-Diş ve Çene Hastalıkları
Cerrahisi Anabilim Dalı
YETERSİZ ALVEOLER KRETLERDE PREPROSTETİK
CERRAHİ İŞLEMLER
Bitirme Tezi
Stj. Dişhekimi Hurşit KULYA
Danışman Öğretim Üyesi: Doç Dr. Bahar SEZER
İzmir-2009
T.C.
Ege Üniversitesi
Dişhekimliği Fakültesi
Ağız-Diş ve Çene Hastalıkları
Cerrahisi Anabilim Dalı
YETERSİZ ALVEOLER KRETLERDE PREPROSTETİK
CERRAHİ İŞLEMLER
Bitirme Tezi
Stj. Dişhekimi Hurşit KULYA
Danışman Öğretim Üyesi: Doç Dr. Bahar SEZER
İzmir-2009
ÖNSÖZ
“Yetersiz Alveoler Kretlerde Preprostetik Cerrahi İşlemler” konulu bu çalışmanın
hazırlanmasında her konuda benden zamanını ve yardımlarını esirgemeyen Sayın Doç. Dr.
Bahar SEZER’e teşekkürü bir borç bilirim.
İZMİR, 2009
Stj.Dişhekimi Hurşit KULYA
İÇİNDEKİLER
1.GİRİŞ…………………………………………………………………………...…1
2.KEMİK REZORPSİYONU VE TAMİRİ………………………………………2
2.1. KEMİK REZORPSİYONUNU ETKİLEYEN FAKTÖRLER……….....….......2
2.2. KEMİK TAMİRİNİN BİYOLOJİK MEKANİZMASI.......................................4
2.2.1. Alveoler iyileşme.......................................................................4
2.2.2. Kemik tamiri ve hacmi..............................................................9
3.PREPROSTETİK CERRAHİNİN AMAÇLARI…………………………......11
4.HASTA DEĞERLENDİRMESİ………………………………………….........12
4.1. KEMİK DEĞERLENDİRMESİ…………………………………............12
4.2. YUMUŞAK DOKU DEĞERLENDİRMESİ…………………................13
4.3. TEDAVİ PLANLAMASI……………………………………….….........13
5.PREPROSTETİK CERRAHİNİN GELİŞİMİ………………………………..14
5.1. KONVANSİYONEL PREPROSTETİK CERRAHİ…………………….14
5.2. MODERN PREİMPLANT CERRAHİ…………………………………..17
6.YETERSİZ ALVEOLER KRETLERDE AGMENTASYON
TEKNİKLERİ……………………………………………………………………..20
6.1. KEMİK GREFT MATERYALLERİ…………………………………….20
6.1.1. Agmentasyonda kullanılan farklı biyomateryaller………...…26
6.2. MODERN KEMİK GREFTİ TEKNİKLERİ…………………………….30
6.3. ONLEY KEMİK GREFTLERİ…………………………………………..33
6.4. SİNUS LİFT………………………………………………………….......37
6.5. DİSTRAKSİYON OSTEOGENEZİSİ……………………………...........44
6.6. İNTERPOZİSYONEL KEMİK GREFTLERİ…………………………...47
6.7. HİDROKSİAPATİT AGMENTASYONU………………………............48
6.8. YÖNLENDİRİLMİŞ KEMİK REJENERASYONU…………………….49
6.9.TÜBEROPLASTİ…………………………………………………………51
7.YETERSİZ ALVEOLER KRETLERDE YUMUŞAK DOKU CERRAHİSİ.52
7.1. MODERN YUMUŞAK DOKU TEKNİKLERİ…………………………52
7.2. TRANSPOZİSYONEL FLEP VESTİBULOPLASTİSİ………………....54
7.3. VESTİBÜL VE AĞIZ TABANI EKSTENSİYON
TEKNİKLERİ……………………………………………………………………….54
7.4. SUBMUKOZAL VESTİBULOPLASTİ………………………………....55
8.SONUÇ…………………………………………………………………………...56
9.KAYNAKLAR…………………………………………………………………...57
10.ÖZGEÇMİŞ………………………………………………………………..…...70
1.GİRİŞ
Doğal dişlerin kaybı alt ve üst çenede hızla kemiksel değişimlerin başlamasını
tetikler. Bunun başlıca sebebi alveoler kemiğin dişler ve periodontal ligamentten
gelen streslerden yoksun kalmasıdır. Herhangi bir hastada rezorpsiyon şeklini
önceden tahmin edebilmek mümkün değildir. Birçok hastada rezorpsiyon süreci
belirli bir periyottan sonra durgunlaşır fakat bazı hastalarda bu süreç alveoler
kemiğin ve altındaki bazal kemiğin tamamen kaybına kadar sürebilir. Azalmış yüzey
alanı ve okluzal kuvvetlerin dağılımına bağlı olarak mandibuladaki rezorpsiyon
maksillaya kıyasla daha şiddetlidir.
2. KEMİK REZORPSİYONU VE TAMİRİ
2.1. KEMİK REZORPSİYONUNU ETKİLEYEN FAKTÖRLER
Alveoler kemik rezorpsiyonunun miktarını ve şeklini etkileyen genel sistemik
ve lokal sorumlu faktörler vardır.(1) Beslenme bozukluğunun varlığı ve osteopöröz,
endokrin disfonksiyonu gibi sistemik kemik hastalıkları genel faktörlerin kapsamına
girer. Diş çekimi sırasında uygulanan alveoplasti tekniği ve alveol kemik kaybıyla
ilişkili lokalize travma kemik rezorpsiyonunu etkileyen lokal faktörlerden
sayılmaktadır. Mevcut protezin uygun olmayan kret adaptasyonu, dengesiz dağılan
okluzal kuvvetlerin varlığı da alveoler rezorpsiyona sebep olur.(2) Yüz iskeletindeki
değişiklikler de rezorpsiyon şeklini iki yolda etkiler. Birincisi; alveoler kretlerdeki
kemik hacmi yüz formuna göre değişiklik gösterir. İkincisi; mandibuler düzlem açısı
düşük, gonial açısı yüksek bireyler daha yüksek ısırma kuvveti oluşturabilirler. Buna
bağlı olarak alveoler kret bölgesine daha fazla stres gelir.(2) Genel ve lokal
faktörlerin uzun dönem etkisi alveoler kemikte kayıplar, arklar arası mesafede artış,
çevreleyen yumuşak dokuların etkisinde artış, protezin retansiyon ve stabilitesinde
azalma olarak görülür.
Kemik kaybı lokal bir etyolojiye de sahip olabilir. Diş germinin gelişimiyle
ilgili sayısız kopyalama faktörü mutasyonları, diş gelişiminin herhangi bir erken
blokajı sonucu alveoler kemik yetersizliğinin ortaya çıktığını göstermiştir. Bu dental
organın bölgesel büyüme sahasında alveoler kemik gelişiminden sorumlu olması
teorisini tamamen destekler.(3)
Bu, dişsizlik vakalarında, kemik erimesinin zamanı ve kemik-kaybı görülen
kretin kronik internal strain stres kaybında formasyonunun gözlemlenmesiyle klinik
-2-
olarak kanıtlanmıştır. Bu kret mandibuler veya maksiler kemiğin üst kısmına ulaşana
dek rezorbe olacaktır. Bu aynı zamanda diş varlığı veya yokluğu ve alveoler kemik
hacmi arasında sıkı ilişkiyi gösteren BT taramalarında, parsiyel anadonti veya
multipl diş agenezisinde de incelenmiştir.(3) Bundan başka alveoler kemik ve
dişlerin kaybının görüldüğü genetik total anadonti vakaları, vertikal boyutsal
defektlerine yol açar.
Sağlıklı bir vakada, periostal yüzey pozitif dengeyle beraber devamlı bir
apozisyon içindedir ancak dental avülsiyon sonrası negatif dengeyle beraber
rezorpsiyon içine girer. Dental organın varlığı çiğneme, yutkunma veya basit dil
basıncı yoluyla alveoler kemik üzerinde çekme ve germe oluşturur bu da periostal
apozisyonun devamlılığını sağlar.(3) Diğer açıdan, dental organın ve oluşturduğu
yüklerin
eksikliği,
alveoler
kemikte
kayba
ve
periostal
kökenin
osseöz
rezorpsiyonunun uyarılmasına yol açar.
Bu nedenle, önceki bölümde belirtilen, büyüme çağlarında da devam eden
erken gelişme sinyallerinin, erişkinlikte de devam ettiğini ve alveoler kemiğin
anatomik devamlılığını sağlamada önemli bir rol oynadığını düşünüyoruz. Bu sinyal
yolları, diş çekiminde veya yaşlanmada görülen kemiğin anatomik modifikasyonları
üzerinde etkili olabilir. Gelişim sürecinde, Msx1 ve Msx2 gibi bazı proteinler farklı
OFE’lerin düzenlenmiş büyümesini ve fonksiyonel aktivitesini kontrol edebilir, aynı
proteinler
hala
gösterilebilir
ancak
OFE’lerin
fonksiyonel
bütünlüğünün
devamlılığından sorumludurlar. Buna rağmen, yaşla beraber, bu homoproteinlerin
gösterilmesi artan şekilde azalır bu da yaşlanma sırasında görülen yavaş kemik
kaybıyla sonuçlanır.(3)
-3-
Yakın gelecekte, bu varsayılan teori ispatlanırsa, kopyalama faktörlerinin lokal
uyarılmasını hedefleyen genetik tedavi, diş çekimi sonrası alveoler kemik kaybını
önleyebilir. Böylece implantolojideki en büyük konulardan birisi çözülmüş olacaktır.
2.2. KEMİK TAMİRİNİN BİYOLOJİK MEKANİZMASI
Aksiyal, appendiküler ve kraniofasiyal kemiklerle karşılaştırıldığında alveoler
kemik kendine özel bir durumu da ortaya koyar. Sonuncusu küçük lezyonları kemik
kaybı olmadan tamir edebilse de alveoler kemik tamirinde her zaman iki parametreye
dayanan kemik hacminde kayıp görülür. İlki diş çekimini takiben osseöz matriksle
internal kavitenin iyileşmesini kapsar. İkincisi ise alveoler kemik hacminin
devamlılığını içerir. İlk mekanizma iyi bilinen ve kemik kırıkları sonrası görülen
fizyolojik işlemlere küçük modifikasyonlarla kıyaslanabilir. İkinci mekanizma ise
kemik hacmi düzgünlüğüyle ilgilidir.(3)
2.2.1. ALVEOLER İYİLEŞME
Yetişkinlerde, kemik tamiri genellikle, osteogenez sırasında gözlenen farklı
embriyolojik basamaklar üreten olayları içeren biyolojik bir işlemi takip eder.
Bu basamaklar üç farklı iskelet düzeyinde beş grupta incelenebilir:
1. Travmaya ani cevap
2. Kondrogenez
3. Endokondral kemikleşme
4. Kemik formasyonu
5. Kemik remodelasyonu
-4-
İkinci ve üçüncü basamakların appendiküler ve aksiyal iskelette sadece
episodik biçimde varolduğunu fakat alveoler kemik iyileşmesinde veya yassı kranial
kemiklerin fizyolojik durumlarında hiçbir zaman gözlenmediğini belirtmek gerekir.
Bu yokluğun açıklaması kondrogenez basamağıyla ilişkilidir. Kondrogenez basamağı
kallus oluşumu sırasında kırık parçaların mobilitesiyle yakından ilişkilidir. Bu
vaskülarizasyonun bozulmasına ve kıkırdak hücrelerinin gelişimiyle lokal hücresel
hipoksiye yol açar. Bu kıkırdak doku fraktürü immobilize etmek amacıyla “yumuşak
kallus” adı verilen bir yapı oluşturur. Bu basamak gerçekleştiğinde, vaskülarizasyon
stabil biçimde gelişebilir ve endokondral ossifikasyondan başlayarak ossifikasyon
sürecine izin verir.(3)
Alveoler iyileşme sırasında, soket daima rijit immobil duvarlardan oluşur.
Duvarlardan birkaçı kırılırsa, kemik fragmanları sökestrum olarak elimine edilir.
Fiske edilmiş, bolca irrige edilen duvarlarda iyileşme sürekli devam edeceği için
kondrogenez meydana gelmez. Diğer yandan, mükemmel şekilde fiske edilmiş ve
immbolize kortikal kemik greftlerinde, bazı greftler kortikal tabaka/kemik grefti
arayüzünde
gerçekleşen
endokondral
ossifikasyon
mekanizmasıyla
iyileşme
gösterirler. Bu aşamada kondrogenezin orta fazı mobilite problemiyle ilişkide
değildir, ancak yetersiz vaskülarizasyon ve hipoksiyle karşılaşılır. Bu hücresel
hipoksi osteoblast farklılaşmasını durdurur ve kıkırdaksal farklılaşmayı teşvik eder.
Alveoler kemiğin iyileşmesi üç basamakta gerçekleşir
(1)Pıhtı oluşumu, büyüme faktörlerinin ve sitokinlerin salınımını içeren travmaya
verilen ani yanıt (2) osteoblastik farklılaşma (3) osseöz mimari ile lokal çekme
germe adaptasyonuyla kemik remodelasyonu
-5-
Travmaya verilen ani yanıt: pıhtı, büyüme faktörleri ve sitokinler
Diş avülsiyonu ile ortaya çıkan dental travma, alveoler soketteki farklı hücresel
elemanlara metobolik gıdaların ulaşımının engellenmesine ve vasküler yaralanmaya
yol açar. Lokal hücresel hipoksi, hücresel değişimler ve olası ölümle sonuçlanabilir
bu da lokal pH’ı arttıran lizozomal enzimlerin salınımına ve hücre nekrozuna yol
açar.
Ayrıca, bu vasküler yaralanma sayısız sitokin ve büyüme faktörlerinin
salınımıyla hücresel ve moleküler elemanların eksikliğine yol açar. Sitokinler,
büyüme faktörlerinin olduğu gibi tirosin kinaz aktivitesine sahiptir böylelikle
hematopoetik ve immun sistemin hücrelerinin proliferasyon ve farklılaşmasını
düzenlerler. Sitokinler ve büyüme faktörleri kırık neredeyse, kemik tamiri süresince
her zaman görülürler.(3) Bu hücre ölümlerine paralel olarak, plateletten zengin,
fibrin ağından oluşan, vasküler yaralanmaya yanıt olarak ortaya çıkan vasküler ve
ekstravasküler elemanlar içeren pıhtı meydana gelir. Pıhtı ve enflamatuar infiltrat
sitokinkler, çevreleyici endoteliyal prekursorların migrasyonu ve proliferasyonuyla
neo-vaskülarizasyonun indüklenmesini teşvik eder. İkinci bir adımda, endotelyal ve
infiltrat hücreler hızlı bir şekilde pıhtı plazminojenini plasmine çevirerek pıhtının
atılmasını sağlar.
Pıhtının erimesi neo-vaskülarizasyonuyla ilişkili ve sitokinlerin kemotaktik
mitotik hareketleriyle bağlıdır ve yeni hücrelerin bölgeye kolonize olmasına ve
granülasyon dokusunun formasyonuna yardımcı olur. Buna paralel, residüel kemik
sökestrını rezorbe eden ve alveoler duvarların yüzeylerini fizyolojik bağlanma için
hazırlayan osteoklast farklılaşması ortaya çıkar.
-6-
Osteoblast farklılaşması ve kemik formasyonu
Diş çekimi sonrası soket içinde görülen granülasyon dokusu lokal ve vasküler
hücresel birliktelik sonucu ortaya çıkar. Son zamanlarda sakin ve dolaşımdaki kök
hücreler
üzerinde
durulmaktadır.
Bütün
dokular,
prolifere
olabilecek
ve
osteoblastlara dönüşebilecek sakin kök hücrelere sahiptir.(3)
Tek tanımlanabilen kök hücreler totipotent olan ES hücreleridir. Bu hücreler
gelişim sırasında farklı yollarla prolifere olur ve birbirine bağlanır, sonra pluripotent,
daha sonra unipotent hale gelir ve son farklılaşmış halini alır. Hematopoetik
hücrelere istisna olarak, vasküler ve medullar sistemin farklı hücrelerine
dönüşebilme özelliğine sahiptir. Medullar boşluklarda pluripotent kapasiteye sahip
stromal hücreler gösterilmiştir. Günümüzde bütün dokuların erişkin kök hücrelerine
sahip olduklarının farkına varılmıştır. Ayrıca, bu kök hücreler pluripotent
aktivitelerini sürdürmektedir. Stromal kök hücreler, örnek olarak vasküler veya
serebral hücrelere farklılaşabilirler. Musküler kök hücreler kemik hücrelerine,
serebral kök hücreler de vasküler hücrelere gelişebilirler. Günümüzde, kemik
hücresine dönüşebilen kök hücreler izole edilebilmiştir. Birkaç örneğin gösterdiği
gibi, bu farklı hücreler yerlerine ve embriyolojik kökenlerine bakmaksızın
pluripotenttir. Bununla birlikte, şu anda mezenşimal kök hücreler olarak görülen
stromal hücreler yeterli desteği görmezlerse kemik hücrelerine farklılaşmazlar.
Örneğin, subkutanöz veya intramusküler mezenşimal kök hücresi enjeksiyonları,
hidroksiapatit veya kollojen sünger gibi non-rezorbe veya yavaş rezorbe olan
destekler olmadığı sürece kemik formasyonu oluşturamaz. Bu genel kavram dolaşan
ve sakin kök hücreler için de geçerlidir. (3)
-7-
Soketi dolduran kök hücreler genellikle meduller boşluklardan, periodontal
ligamet artıklarından ve neovaskülarizasyondan gelirler. Bu olaya periferal bağ
dokuları gibi periost da katılır fakat küçük bir rol oynar.
Residüel periodontal ligamet hücrelerine ek olarak, pıhtıdan periosttan,
enflamatuar infiltrattan ve meduller boşluklardan gelen kök hücreler soketi dolduran
granülasyon dokusunu oluştururlar. Alveoler kavitenin tam olarak dolmasında
granülasyon dokusunun boyutu en önemli faktördür. Bu nedenle, çekim sonrası
pıhtının mümkün olduğunca fazla yer kaplaması ve pıhtının devamlılığını sağlamak
için sütur ve cerrahi örtü yapılması tavsiye edilir.(3)
Alveoler osseöz duvarlar, granüler dokunun neovaskülarizasyon kadar,
osteojenik özelliklerde iyileşme dokusu oluşturmasına izin verir. Bu maturasyon,
ekstrasellüler matriksten salınan sitokinler, endoteliyal hücreler ve granülasyon
dokusunun hücreleri tarafından yönlendirilir. Bu maturasyon işlemi, transdüksiyon
yollarının farkı ligand-reseptörlerinin aktivasyonuna ve farklılaşma faktörlerine uyar.
İlk faz vasküler ve sahaya özel değilse ikinci fazın selüler ve sahaya özel olduğu
kayda değerdir. Bununla birlikte, şu andaki bilgi durumları farklı durumlar ve
reaksiyon kompleksi tarafından açıklanan moleküler ve selüler olayların tam
kronolojisini sıralamaya yetersizdir. Farklı durumlar çeşitli moleküler ve sellüler
reaksiyonlara yol açabilir. Örnek olarak, hücresel düzeyde, kendi formasyon
dinamikleri ve büyüme faktörleriyle kondroid doku adı verilen hibrid doku
formasyonuna yol açan ara basamakta birçok reaksiyon tanımlanmıştır. Moleküler
düzeyde, aynı faktör otokrin ve/veya parakrin fonksiyonuna sahip olabilir ve bu
reaksiyon farklılık olasılığını arttırır. Ligand-reseptör reaksiyon karmaşıklığı,
-8-
ligandın olup reseptörün olmaması veya tam tersi, reseptörün birkaç liganda sahip
olması, saha özgüllüğünden sorumlu olabilecek, dinamik çekişme ve reseptör
uygunluğunu ortaya çıkarır. Sonuç olarak, aynı bölgeden farklı lokal reaksiyonlar
gözlenebilir. Bununla birlikte, moleküler ve sellüler ajanların bu farklılıklarına ve
karışıklıklarına bakmaksızın, bu reaksiyonlar her zaman osteojenik sellüler kütlenin
başlamasına sebep olur.(3)
Osteojenik hücrelerin
osteoblastlara dönüşmesi osteoid bir matriksin
formasyonuna ve sonradan non-fonksiyonel hale dönüşen bir osseöz doku
oluşmasına yol açar. İmplant sahasının hazırlanmasından sonra bu dokudan yapılan
biopsiler, osteojenik hücrelerin yuva açma işleminden 10-12 gün sonra farklılaşmaya
başladığını, osseöz defektin büyüklüğüne bağlı olarak 3-5 hafta içerisinde de bir
iyileşme dokusunun oluştuğunu göstermiştir. Bu doku fonksiyonel olması için
remodele edilmelidir.
2.2.2. KEMİK TAMİRİ VE HACMİ
Kemik kaybına yol açan iki farklı iyileşme şeklinin farkını ortaya koymak
önemlidir: birisi iyileşme için yetersiz internal materyal sonucu ortaya çıkan kemik
kaybıyla ilişkiliyken diğeri eksternal duvarların yokluğuyla ortaya çıkar. İlk vakada,
doldurma için gerekli hacim limitlidir ve alveoler kemik duvarları ile açıklanır,
kemik kaybı yetersiz hücre sayısından ve hücre aktivitesinden ortaya çıkar. İkinci
vakada, kemik iyileşmesinin eksternal limitleri mevcut değildir ve bu nedenle ilk
olarak sinyalleşmeyle saptanmalıdır. Sonuncusu vestibuler duvar fraktürleri veya
alveolektomi ile görülen diş avülsiyonları vakalarında gözlenir. Bütün vakalarda,
-9-
vestibuler alveol duvarı kazara travma nedeniyle veya cerrahi harekete bağlı
değişime uğramıştır.(3)
Dış duvar üzerinde herhangi bir değişimin kemik kaybına yol açtığının, bunun
yanında iç duvarlarda meydana gelen değişimlerin böyle bir kemik kaybına yol
açmadığının altını çizmek gerekir. Bu gözlem, kemik hacminin belirlenmesinde
periostal yüzeylerin oynadığı rolle karşılaştırılmalıdır. İki parametrenin üzerinde
durmak gerekir(1)periostal yüzey sahaya özgü sinyal verici bir bölgedir(2)kökenine
bağlı olmaksızın, osteojenik nesile bağlı kök hücreler veya herhangi bir osteojenik
hücre orijinal anatomiyi yeniden oluşturmak için belirli bir desteğe ihtiyacı vardır.
Öyle görünüyor ki bu iki gözlem, kortikal tabakadaki değişimle alakalı kemik
hacminde görülen kayıba dikkat çeker. Osseöz hacmin yenilenmesinde görülen
iyileşme defektine sebep olan eksikler, periostal sinyalleşmenin ve yeterli desteğin
kaybıyla meydana gelir. Bu iki elementin de zorunlu olduğu, periostal hücre yapısını
koruyan tam kalınlıklı flep kaldırılsa bile rijit veya yarı-rijit destek yerleştirilmedikçe
tabakanın iyileşmeyeceği açıktır. Ayrıca, periostal hücre yapısını koruyan fakat
matriks desteği olmayan tam kalınlık flep uygulanması sinyallerde değişime ve
sonuç olarak kemik hacminde kayıba neden olur. Bu durum periodontal kemik
yüzeyleri için de görülür ama interdental veya inter-radiküler septum elimine
edildiğinde bu hacimsel kayıbı tahmin etmek daha zordur.(3) Bu sinyallerin internal
yeri dış kemik hacmi için daha az öneme sahiptir.
Bu gözlem, iyileşme işleminde görevli hücreler belirli olsa da eksternal yapının
iyileşmesi internal yapıya nazaran farklı sinyallere ihtiyaç olduğunu ortaya koyar.
- 10 -
Farklı kemik yapıları, trabeküler ve kortikal, doğru kemik hacmini restore
etmede tamamlayıcıdır. Bu nedenle, bu osseöz desteğin herhangi bir vestibuler veya
lingual tabaka defektiyle değişimi, sinyalde belirgin bir kayıba, iyileşme defektine ve
kemik hacminde kayba yol açar.(3)
En şiddetli rezorpsiyon vakalarında spontan mandibular fraktür riskinde
belirgin bir artış vardır.
3. PREPROSTETİK CERRAHİNİN AMAÇLARI
Belirgin alveoler rezorpsiyon görülen vakalarda protez bölgesini modifiye
etmek, hastanın fonksiyonel, estetik ve komfor ihtiyaçlarını karşılamak amaçlı daha
komplike cerrahi ve prostetik teknikler kullanılmalıdır.
Atrofik alveoler kretlerin tedavisinin temel görevleri bunları kapsamalıdır(4)
Geniş bir kenar sırt formunun yaratılması
Protezi taşıyan bölgede yeterli sert doku
Protezin tutuculuğu için yeterli vestibuler derinlik
Düzgün arklararası ilişki
Mandibuler kırık oluşabilecek bölgelerde güçlendirme
Sinir-damar paketinin korunması
Uygun damak kubbesi şekli
Düzgün posterior tüber çıkıntısı
Gerektiğinde implant yerleşimini karşılayacak uygun kemik desteği ve yapışık
yumuşak doku örtüsü sağlamak.
- 11 -
4. HASTA DEĞERLENDİRMESİ
İleri preprostetik cerrahi tekniklerine başvurmadan önce hastanın genel sağlık
durumunun değerlendirmesi önemlidir çünkü birçok yaklaşım; verici sahadan kemik
alınması, multipl cerrahi işlemler genel anestezi gerektirmektedir. İleri derece kemik
rezorpsiyonuna
sebep
olabilecek
sistemik
olası
rahatsızlıklar
gözden
geçirilmelidir.(2) Serum kalsiyum fosfat, paratiroid hormon ve alkalin fosfat
seviyelerinin kontrol edilmesi kemik rezorpsiyonunu etkileyebilecek metabolik
problemlerin fark edilmesine yardımcı olur.(1)
4.1. Kemik Değerlendirmesi
Bir klinik değerlendirme mutlaka mevcut alveoler kretin ve altındaki bazal
kemiğin yüksekliğini, genişliğini ve konturlarını içermelidir. Mandibulada posterior
kret bölgesinin palpe edilmesi konkavitelerin ve mental nörovasküler demetin tespit
edilmesine yardımcı olur. Maksillada ise damak kubbesi, kret formu, anterior nasal
çıkıntı, zigomatik kemik, posterior tüberler değerlendirilmelidir. Arklar arası ilişki
antero-posterior, transversal ve vertikal düzlemlerde değerlendirilmelidir. Kısmi
dişsiz vakalarda hipererüpte veya malpoze dişler not edilmelidir.(2)
Mandibuler
ve
maksiller
kemik
konfigürasyonunu
tespit
amacıyla
radyogramlara başvurulmalıdır. Her iki çenenin de kemik yapılarını ortaya koymada
en
faydalı
radyogram
tekniği
panaromik
filmlerdir.
Anterior mandibuler kret bölgesi ve kret ilişkilerinin incelenmesinde
sefalometrik radyogramlara başvurulabilir. Tomografi, bilgisayarlı tomografi (BT)
gibi daha sofistike radyografik çalışmalar daha ileri bilgiler sağlayabilir.(2) BT
maksillada kret formunu ve sinus anatomisini tespit etmede oldukça başarılıdır.
- 12 -
Mandibulanın kesitinin değerlendirilmesinde n. Alveolaris inferiorun yerinin tespiti
önemlidir.
4.2. Yumuşak Doku Değerlendirmesi
Preprostetik cerrahinin planlamasında yumuşak doku değerlendirmesinin
sonuçları önemlidir. Şüpheli patolojik lezyonlardan biyopsi örnekleri alınmalı ve
düzgün bir biçimde tedavi edilmelidir. Alveoler kret bölgesinde yapışık mukozanın
miktarı ve özellikleri değerlendirilmelidir. Bu özellikle implant çevresinde keratinize
doku sağlamada önemlidir.(2) Bukkal ve vestibuler bölgeler gibi protezin
stabilitesini etkileyebilecek yerler mukozal ve kassal yapışma yerleri açısından
değerlendirilmelidir. M. Mylohyoideus ve m. Genioglossusun yapışma yerleri
açısından mandibula lingual yönden değerlendirilmelidir.
4.3. Tedavi Planlaması
Aşırı derecede atrofinin görüldüğü durumlarda tedavi kemik bozukluklarının
düzeltilmesine ve ilişkili yumuşak dokuların değişimine yönelik olmalıdır. Atrofiye
rağmen yeterli kemik miktarının olduğu durumlarda protez bölgesi kemik miktarının
arttırılması veya yumuşak doku cerrahisi yoluyla düzeltilmelidir. Uygun tedavi
yönteminin seçiminde birçok faktör rol oynar. Örneğin hafif rezorpsiyon görülen
yaşlı hastalarda yumuşak doku cerrahisi yeterli olabilirken, ileri derecede atrofi
görülen genç bir hastada agmentasyon prosedürleri dikkate alınmalıdır. İmplantların
rolü de tedavi planlamasını etkiler. Hastanın uzun dönem iyileşme döneminde
protezsiz kalması konusunda bilgilendirilmesi gerekir.
Yumuşak doku cerrahisinden önce kemik agmentasyonu konusunda kesin bir
kararın verilmesi gerekir. Maksimal agmentasyon için greftin üzerini örtecek
- 13 -
gerilimsiz bir doku varlığı gereklidir. Sert doku greft uygulaması ve uygun iyileşme
oluşmadan yumuşak doku cerrahisine geçilmemelidir.(2)
5. PREPROSTETİK CERRAHİNİN GELİŞİMİ
5.1 KONVANSİYONEL PREPROSTETİK CERRAHİ
Preprostetik cerrahi 20. yüzyılın başlarında büyük anlamda Alman kökenli
olarak ortaya çıkmıştır. 1874te THIERSCH(6) tarafından bulunan derideki yaraları
örtmek için greft kullanılması bu tarzdaki ameliyatların gelişiminde önemli bir rol
oynamıştır. Greftleri sabitleyen birleşimin bir protez yardımıyla gerilmesi;
mandibulada lingual ve vestibül sulkusun derinleştirilmesinde uygulanan,
TRAUNER(7) ve OBWEGESER(8) tarafından ileri sürülmüş popüler bir yöntemdi.
Birçok uzman tarafından buna yararlı eklemeler yapılsa da genel amaç olan alveolar
çıkıntıdaki ve böylece mandibular kemik kaidesinin bir kısmında supraperiostal
disseksiyon yapılması ve daha sonra greft kullanarak protezi taşıyan bölgenin
arttırılması 1950 ve 1970ler arasında preprostetik cerrahinin ana hedefiydi.Bu
zamandan sonra greft kullanılmadan kazanılan sulkus derinliğinin önemli bölümünün
geri döndüğü biliniyordu.
Bu
tarzdaki
birçok
vestibuloplasti
ve
ağız
tabanının
derinleştirilmesi
operasyonlarının geçmişi ve gelişimi hakkında DAVIS(9) tarafından mükemmel bir
rapor sunulmuştur. Ayrıca bu prosedürlerin en önemli hedeflerini de ortaya
koymuşlardır.
- 14 -
Bunlar;
-Yerdeğiştirme kuvvetlerine karşı mekanik direnç
-stabil bir protez sahası
-yükü taşıyan doku olarak deri
Mukozal greftlerin kullanımına PROPPER tarafından(10) başlanmıştır ve daha
sonra STEINHAUSER(11), TIDEMAN(12), HILLERUP(13) sayesinde popülerliğini
kazanmıştır. Bu büyük oranda deri greftlerinin alınmasından kaçınmak arzusundan
meydana gelmiştir. Verici sahanın morbiditesinin yanında hastalar tarafından
herzaman kabul edilmeyen skarlar meydana gelmekteydi. Mukozal greftlerin deri
greftlerine göre dezavantajı olan limitli miktarlarda bulunabilmesi durumunun
üstesinden greft uygulanacak sahayı sınırlayarak gelinmiştir.
Yayınlarda herzaman yer almasa da, bahsedilen tekniklerde bazı önemli ters
etkiler de görülmüştür. DE KOOMEN(14) iki ana engeli belirten ilk kişiydi. Bunlar;
çenede çöküntü görülme riski ve mental bölgede duyu kaybı riskiydi. Çenede
çöküntü meydana gelme riski, labial sulkus derinleştirmesini kısıtlayarak ve mental
kasları sadece bölgesel olarak ayırarak azaltılabilir. Duyu kaybı riski ise; sinir
fibrillerinin açığa çıkarıldığı DAVIS tekniğine ters olarak mental sinir demetinin
epinöral kılıfını bırakarak azaltılabilir. HUYBERS(14), KOOMEN(15) tarafından
ortaya sürülen bu problemlerin üstesinden gelmede bu modifikasyonların
uygulanabilirliğini belirtmiştir. DAVIS de bu modifikasyonları onaylamıştır.(9)
Maksiller alveolar çıkıntıdaki rezorpsiyon miktarının mandibuladakine nazaran
4 kat daha az olmasına bağlı dikkatler anlaşılır bir biçimde alt protezin stabilitesini
- 15 -
ve retansiyonunu arttırmaya odaklanmıştır.(16) OBWEGESER(17) 1964’te bir üst
protezin stabilitesini ve retansiyonunu arttırmak için submuköz vestibuloplastiyi
tanıtana kadar bu böyle değildi. Bu fibröz doku ve kas dokusunun diseksiyonunu ve
bir protez yardımıyla mukozanın tespit edilmesini içeriyordu. Bir üst protezin
retansiyonunu arttırmak için uygulanan diğer yöntemler ise doku grefti kullanılarak
uygulanan bir “buccal inlay”,(18) tüber bölgesinin arka kısmında daha fazla
supraperiostal disseksiyona izin veren hamulusun kırılmasını ve greftin
yerleştirilmesini içeren “tüberoplasti”dir.(19)
Büyük olasılıkla yukarıda belirtilen yöntemlerin bazı ters etkilerinin ortaya
çıkması sonucu özellikle de aşırı rezorbe olmuş çenelerde uygulandığında, kemik
greft
materyalleriyle
kesin
augmentasyonu
yöntemleri
gelişmiştir.
CLEMMENTSCHISCH(20) rezorbe mandibulanın kemik miktarını arttırmak
amacıyla intraoral yolla serbest kaburga kemiği greftlerini kullanan ilk kişi olarak
düşünülmektedir. Bu yöntem DAVIS(21) sayesinde popülerleşmiş ve TERRY (22)
tarafından üst çenede de uygulanmıştır. Bu greftler daha sonra iyileşmede görülen
problemleri ve protez uygulandıktan sonra greftin ani rezorpsiyonunu önlemek
amacıyla tel yardımıyla tespit edilir. BELL(23) dişsiz hastalarda maksillanın
konumunu geliştirmek ve intermaksiller ilişkiyi eski haline geri getirmek için Le Fort
I osteotomi ve araya yerleştirilen kemik greftini kullanan ilk araştırmacı olmuştur.
Bu teknikler birçok modifikasyondan geçerek gelişmiş sonuçlara ulaşılmıştır.(5)
Hidroksiapatitin özellikle tanecik şeklinde gelişi konvensiyonel preprostetik
cerrahiye yeni bir boyut kazandırmıştır. KENT (24) alveolar sırtların miktarını
arttırmak için gerekli olan kemik grefti ihtiyacını halletmek amacıyla hidroksiapatit
- 16 -
kullanılmasını ortaya sürmüştür. Bu tekniğin ana problemi istenilen şekildeki
taneciklerin içeriğiydi. Diğer problemler ise mukoza üzerine yayılan mukozit ve
mental sinirle taneciklerin teması sonucu ortaya çıkan hassasiyetti. Otojen kansellöz
kemiğin hidroksiapatit kristalleriyle karıştırılması sonucu bu problemler azaltılmıştır.
Kısmen rezorbe olmuş mandibulada otojen kansellöz kemiğin hidroksiapatitle arka
bölgede onley gtreft olarak, simfiz bölgesinde ise interpozisyonel olarak kullanılması
gelişmiş sonuçlarda artışa yol açmıştır.(25) Ayrıca maksillanın ön bölgesindeki
alveolar çıkıntının augmentasyonunda hidroksiapatit kristalleri başarılı olmuştur.
Uzun gelişim hikayesine ve prostodontistler tarafından kabul edilmesine rağmen
preprostetik cerrahi kemikiçi implantlar tarafından bir miktar gölgede bırakılmıştır.
Preprostetik cerrahinin esas kavramlarından olan yumuşak dokunun durumunu
iyileştirmek ve kemik miktarını arttırmak hala geçerlidir.(5)
5.2. MODERN PREİMPLANT CERRAHİ
Konvansiyonel preprostetik cerrahiden farklı olarak preimplant cerrahide
kemik artışı ve yumuşak doku prosedürleri sonucu implant çevresinde artış
görülmektedir. Hedef prensip kemikiçi implantın optimum biomekanik fonksiyon
için uygun pozisyonda, uygun boyutta ve estetik bir biçimde yerleştirilebilmeleri için
yeterli bir implant sahası yaratmaktır.
Preimplant
cerrahinin
endikasyonları
olarak çene atrofisi, travma sonucu çenede görülen avulsiyon, tümör cerrahisi sonucu
çene kemiğinin zamanla azalması ve çenede görülen konjenital deformiteler
gösterilebilir.(5)
Dişin kaybını takiben alveolar kemikte görülen kayıp kullanılmayışa bağlı
atrofiden kaynaklanır. Başlangıçta kemik kaybı hızlıdır. 2-3 yıl sonra bu miktar azalır
- 17 -
ama sonsuza kadar devam eder.(16) Potensiyel implant sahasını oluşturan keratinize
ve non-keratinize mukozal örtüde kanıtlanmış bir azalma görülmektedir.(26)
Preimplant cerrahi sadece implant sahasının geliştirilmesi üzerinde durmaz
buna ek olarak alveolün genişliğindeki ve yüksekliğideki eksikliklerin düzeltilmesini
ve intermaxiller ilişkinin düzenlenmesini de planlar. Bunun sebebi dişsiz çenedeki
kemik kaybı ve kısmi diş eksikliği görülen çenede miktarın azalması maksillomandibuler ilişkide değişime, dişsiz alveolle ilişkili aşırı kas bağlantıları ve mukoza
yüzeyinin azalmasına yol açar. Bu değişikliklerin yaşlılık, ağız çevresinde hipotoni
ve çöküntülerle birlikte görülmesi sonucu yüz formunda ve görünümünde
değişiklikler gözlenir.(26)
Kemikiçi implantın başarılı uygulanışı;uygun anatomik formun ve çevrenin,
biouyumlu ve uzun dönemli uygun biomekanik durumun varlığına bağlıdır.
İmplantlar ağız tabanıyla, dille ve dudak hareketleriyle kesişmemelidir. Fonksiyonel
kuvvetlere dayanması ve fonksiyonel ve estetik ihtiyaçları anatomik oluşumlarla
kesişmeden (örneğin; “maksiller sinüsle”) karşılayarak optimum eğilmeye izin
vermesi için gerek yükseklikte gerek genişlikte yeterli kemik hacmine ihtiyaç vardır.
İmplant optimum kuvvetlere maruz kalacak ve maksimum yüzeyle temas edecek
şekilde yerleştirilmelidir. Vertikal, transversal ve antero-posterior ilişkiler yeterli
olmalıdır.(5) Eğer yukarıdaki şartlar geçerliyse kemik augmentasyonunu, yumuşak
doku prosedürlerini veya bir osteotomiyi içeren implant cerrahiye girişilebilir.
Cawood ve Howell’ın(27) dişsiz çene sınıflandırmalarına göre preimplant
cerrahiye bir tasarı geliştirilmiştir. Class IV, V ve VI dişsiz veya kısmi dişsiz
- 18 -
maksillada genellikle onley greftlerin kullanıldığı kemik augmentasyonu ile kombine
olarak kemikiçi implantlar uygulanır. Class IV maksillada alveolar genişliği eski
haline getirmek için genellikle kemik augmentasyonu gereklidir.(28) Class V’te ise
hem alveol yüksekliğini hem de alveol genişliğini arttırmak için kemik
augmentasyonu gereklidir. Class VI’da ise alveolar çıkıntıyı yeniden oluşturmak için
augmentasyona ek olarak antero-posterior interark ilişkisini geliştirmek için
osteotomi de gerekebilir.(29)(30) Posterior maksillada BOYNE ve JAMES,
TATUM(31) tarafından ileri sürülen tekniği bildirdiler. Bu teknik kemik içi
implantların yerleştirilmesi için posterior maksillada kemik hacminin arttırılması
amacıyla maksillanın destek kısmından açılan pencere yardımıyla greftin
yerleştirilmesini
ve
sinüs
membranının
yükseltilmesini
içerir.
Class IV mandibulada, kalan alveolar sırtların arttırılması veya azaltılması
protetik ihtiyaçlar tarafından etkilenmektedir. Anterior Class V dişsiz mandibulada,
implantlar ilave cerrahi operasyona gerek kalmadan yerleştirilebilir, bu da interark
ilişkinin korunması ve estetik sebeplerden ötürü gösterilebilir. Class VI dişsiz
mandibulada, kısmi olarak kalan kemik miktarının 10 mm’den daha az olduğu ve
yumuşak doku durumunun olumsuz olduğu durumlarda ilave yumuşak doku ve
kemik arttırımı gerekebilir. Class IV, V, VI kısmi dişli mandibulada, kemik arttırımı
ve yumuşak doku çoğaltımı prosedürleri genellikle gereklidir. Posterior mandibulada
daha uzun kemikiçi implantlar yerleştirmek amacıyla inferior alveolar sinirde yapılan
manipulasyonlar uzun süreli veya kalıcı sinirsel kayıplara yol açabilir.(32)
LONGMAN(33) tarafından 300 dişsiz hastada yapılan bir çalışmada çenedeki
atrofi incelendi. En sık karşılaşılan durum maksillada Class IV, mandibulada Class
V’tir. Buna göre, ilerleyen çene atrofisinde özellikle maksillada kemik arttırımı ve
- 19 -
yumuşak doku işlemlerinin kemikiçi implant yerleştiriminde öncülük teşkil ettiği
görülmüştür.(5)
Kemik greftinin seçimi greftin tipinden etkilenmektedir örneğin; blok greftler, özel
greftler. İhtiyaç duyulan kemik miktarı verici sahayı belirler.
6. YETERSİZ ALVEOLER KRETLERDE AGMENTASYON
6.1 KEMİK GREFT MATERYALLERİ
Mandibula ve maksilla için uygun olan greft tipleri otojen, allojen, alloplastik
ve ksenojenik olarak ayrılmaktadır. Otojen greftler aynı bireyden elde edilir.
Allojenik greftler aynı türün farklı bireylerinden elde edilir. Alloplastik greftler ise
sentetik yollarla elde edilir. Ksenojenik greftler de farklı türden canlılardan elde
edilen materyallerdir.(34)
Otojen Greftler:
Otojen greft için verici sahalar:
1- İliak kemik(anterosuperior veya posterosuperior çıkıntı)
2- Kaburga
3- Kalvarya
4- Anterior tibia
5- İntraoral verici sahalar
6- Serbest flepler
Kemik greft materyallerinin elde edilmesindeki temel prensip yüksek potansiyelde
pluripotent veya osteojenik prekursor hücreleri taşıyacak maksimum miktarda
kansellöz kemiğin sağlanmasıdır.(35) Bu hücreler harap olmuş kemik bölgelerinin
restorasyonunda etki göstermeleri amacıyla kullanılırlar.
- 20 -
Mevcut kemiğin duvarlarında da biraz pluripotent hücreler bulunsa da,
preosteoblastik ve pluripotent hücrelere sahip yüksek oranda osteojenik greft
materyalinin kullanılması başarı oranını ve oluşacak kemiğin kalitesini doğrudan
etkiler.(36)
Yüksek miktarda pluripotent hücreye sahip olması nedeniyle iliak çıkıntı greft
materyallerinin altın standartı olarak kabul edilir. Bu hücreler indükte edildiklerinde
osteoblastlara dönüşme potansiyeline sahiptirler.
Birçok verici saha olmasına rağmen posterior iliak çıkıntı 80cm³’e kadar
kemik hacmi sağlayabilmektedir. Buna rağmen kaburgalar çok küçük miktarda
kemik sağlayabilirler.
Ancak otojen kemik grefti elde etme sırasında anterior iliak çıkıntıdan kemik
alımı sonucu lateral femoral sinirde parestezi görülme olasılığı vardır. Yapılan bir
çalışmada 300 hastanın anterior iliak çıkıntısından kemik elde edilmiş ancak yalnızca
bir hastada bu probleme rastlanmıştır. İliak kret tekniğinde karşılaşılabilecek minör
komplikasyonlardan birisi de hematom oluşumudur.(34)
Ramus greftleri kortikal yapıdadır. Ramustan elde edilen greftlerin boyutu
simfizden elde edilenlere oranla uzunluk olarak daha fazla fakat derinlik olarak daha
azdır. Kalın greftler çapın arttırılması istenen dar bölgelerin agmentasyonunda
kullanılmaktadırlar. Mandibular ramustan yaklasık 40 mm uzunluğunda ve 10-15
mm derinliğinde greft elde edilebilmektedir. Greftin kalınlığı inferior alveol kanalın
eksternal oblik ridge yakınlığı ile sınırlı kalmaktadır.(37)
- 21 -
Simfiz bölgesinden elde edilen greftler kortikokansellöz yapıdadırlar.
Simfizden ramusa oranla daha kalın fakat anatomik limitasyonlardan dolayı daha
kısa greft elde edilebilmektedir. Mental foramen, anterior dislerin apeksi ve
mandibulanın alt sınırı greftin boyutunu sınırlandırmaktadır. Simfiz bölgesinde
osteotomiler 5 kuralına göre yapılmalıdır.
Buna göre osteotomi:
1. Anterior dişlerin 5mm apeksinden
2. Foramen mentalenin 5mm mezyalinden
3. Mandibula alt sınırının 5mm koronalinden yapılmalıdır.
Simfiz bölgesinin; ulaşabilirliğin kolay olması, yüksek konsantrasyonda
osteoblast içermesi ve alıcı bölgede kemik oluşumunu arttırması gibi avantajları
bulunmaktadır. Verici bölgede dudak, çene ve anterior disetinde duyu kaybı, anterior
dislerde uyuşukluk, dişlerde devitalite, vitalite kaybı nedeniyle renk değişikliği,
konuşma ve beslenmede zorluk, çene konturunda değişiklik, postoperatif ağrı, şişlik,
yara bölgesinin açığa çıkması ve enfeksiyon, hematom, kemikte kırık meydana
gelmesi ve kırık parçaların yer değistirmesi gibi komplikasyonlar meydana
gelebilmektedir.(37)
Bazı araştırma sonuçlarına göre PRP eklenmiş otojen greftlerinin kemik
oluşumunu hızlandırdığı da iddia edilmektedir.(38)
- 22 -
Allojen kemik grefti materyalleri, bir defekt alanında veya kavitede
osteoindüksiyon ve osteokondüksiyon sonucu kemik oluşturmak için göç etmek için
kemik hücrelerini yönlendiren bir yapı iskeleti görevi görür.(39)
Şu anda dental ameliyatlar için birçok biyouyumlu allojen ve ksenojen greft
materyali vardır. Bu materyallere örnek olarak demineralize dondurulmuş
kurutulmuş kemik allogreftleri, kalsiyum karbonat coral, PepGen-P-15 gösterilebilir.
Bu materyallerin tümü başarılı sonuçlar yaratabilen özelliklere sahiptir. Genelde
başarılı olmasına rağmen, bunlar ve diğer bütün kemik yedeği materyaller tahmin
edilemeyen yeni miktarda ve kalitede kemik formasyonu, hastanın kabul edebilirliği,
yavaş
rezorpsiyon
karakteristikleri
ve
maliyetleri
açısından
dezavantajlara
sahiptir.(40)
Mineralize kansellöz kemik materyalleri alveolar rekonstrüksiyon ve koruma
amacıyla dental ameliyatlara uygun hale getirilmiştir.(41)(42) Kemik morfojenik
proteinlerini ve osteoindüksiyon için gerekli mineralleri korumak ve konağın
hücresel reaksiyonunu minimize etmek için uygun preperasyon tekniği üretici
tarafından belirtilmiştir. Buna ek olarak, ürünün hızlı bir şekilde kemik
formasyonunu arttırdığı ve dental implantların 16-24 hafta gibi kısa sürede
yerleştirilmesine izin verdiği gözlenmiştir.(42)
Kemik Morfojenik Proteinin Greftlerle Kullanımı
Yıllardır ortopedik literatür BMP ve diğer greft materyallerinin yararlarını ve
başarılarını
inceledi.(43) Yakın zamanlı maksillofasiyal literatüre ait raporlar
BMP’nin dental implant yerleştirilmesinde alveol kemik rejenerasyonunda
- 23 -
başarılarını
ve
yararlarını
detaylandırdı.
Schwartz
DFDBA’nın
yanlız
kullanıldığından daha iyi sonuçlar elde etmek için rhBMP-2’nin eklenebileceğini
göstermiştir.(44) Boyne ve Shabahang rhBMP-2 ‘nin Bioplant HTR veya Bio-Oss
veya Bio-Core ile kombine kullanılmasıyla implant yerleştirmek için alveolar
kemikte uygun tamirin gerçekleştiğini belirtmişlerdir.(45)
Son günlerde, BMP ailesinden bir üye, rekombinant insan BMP’i
maksillofasiyal
iskeletteki
kemik
defektlerinin
rekonstrüksiyonunda
önem
kazanmıştır.(43) Bu Urist tarafından açıklanan BMPnin ailesindir ve ortopedik
cerrahide kemik gelişimini sağlamak amacıyla yıllardır kullanılır. RhBMP-2nin
özellikleri ve karakteristikleri heryerde detaylı bir biçimde belirtilmiştir. Özetle,
rhBMP-2 osteoindüksiyon
sonucu tahmin edilebilir ve hızlı bir biçimde kemik
oluşumunu sağlar.(46)
Genetik bir şekilde yaratılmış ürün olan, rhBMP-2 kemik formasyonunu
sağladığı görülmüştür.(43)(45) Bunu da andiferansiye mezenşim hücrelerini kemik
formasyonunda gerekli olan mezenşimal hücrelere dönüşmeye indükleyerek
gerçekleştirir.(45)
Mineralize insan kemik allogreftinin ve rhBMP-2’nin kombinasyonunun sinüs
tabanının augmentasyonunda kompozit greft olarak kullanılması otojen kemik
ihtiyacını minimize ederken maksillada yeterli miktar ve kalitede kemik elde etmede
kusursuz bir yöntem olduğu göstermiştir. Kemik-özü biopsisi allojen kemikle direk
ilişki içinde ve ona yapı iskeleti oluşturacak biçimde yeni kemik oluşumunu
- 24 -
göstermiştir. Sağ ve sol sinüslerde oluşan canlı kemik oranı farklıdır fakat klinik
olarak her ikisi de uygundur ve normal kemiğe çok benzer yapıdadır.(39)
BMP ürünleri mükemmel yeni kemik oluşturmasına rağmen kollajen süngerin
sinüs içinde sıkışmasından dolayı hastaya uygulanan tipik metod umulan yeni kemik
hacminin daha az olabileceğini gösteriyor. RhBMP-2 ye mineralize kemik greftinin
eklenmesi sonucu daha fazla hacimde kemik oluşmasını sağlayan bir yapı iskeletinin
oluştuğu görülür.
RhBMP-2’nin bir kemik rejenarasyon ürünü olarak gösterilen yararları
arasında hastalık bulaşma riskini ortadan kaldırması, birçok uygun taşıyıcıyla
kolayca uygulanabilmesi ve hızlı bir şekilde yeni kemik oluşturabilmesi gösterilebilir.
RhBMP-2’nin dezavantajları azdır fakat mevcut olanlar yüksek maliyet ve zor elde
edilebilirlik
ile
alakalıdır.
Şimdilik
rhBMP-2
sadece
ortopedik
amaçla
kullanılmaktadır, buna rağmen multipl çalışmalar onun maksilla ve mandibulayı
rekonstrükte etmede kullanılması destekler niteliktedir.(39)
Sonuç olarak benzer vakalarda kombine veya yanlız greftlerin hangi mantıkla
kullanılacağı
sorusu
ortaya
çıkıyor.
RhBMP-2
in
situ
olarak
kemik
indükleyebileceğini gösterdi. Birçok rapor her ikisini de başarılı bir greft operasyonu
için kullanabileceğimizi gösteriyor.(39)
- 25 -
6.1.1. Agmentasyonda kullanılan farklı biyomateryaller
Dondurulmuş Kurutulmuş Kemik Allogreftleri(DFDBA)
Demineralize dondurulmuş – kurutulmuş kemik allogreftleri ( DFDBA )
kolayca bulunabilmekte ve osteokondüktif özelliklerinden dolayı 1970lerden beri
kullanılmaktadır. 1996 yılında periodontal rejenerasyonun ilerletilmesi için en
önemli kriter olarak onaylanmıştır. Biocoral® ( Inoteb, St. Gonnery, Fransa ) genel
olarak aragonit şeklinde kalsiyum karbonat (%97 - %98 ), stronsiyum, florid,
magnezyum, sodyum ve potasyumdan oluşmaktadır. %45ten fazla poroziteye sahip
ve 250 µm ( 150 – 400 arasında ) çapında gözeneklerden oluşmaktadır ve bu şekilde
spongiyoz kemiği andırır.(47) Son zamanlarda Biocoralın® yetişkin periodontitis ile
ilgili kemik defektlerinin tedavisi için kemik yerleştirme materyali olarak
kullanılmıştır.(48) Aragonit kristallerin mimarisi koralin yapısına doğru granülasyon
dokuların girmesi ile gelişmeye izin verir. Açık gözeneklerde, hızlı bir şekilde
kemikle yerdeğiştiren fibrovasküler dokuların formasyonu mevcuttur. (49)
Biocam®
Biocam® SiO2 (%45), CaO (%24.5), NaO2 (%24.5) ve P2O5 ( %6)dan
oluşmaktadır.(46) Dokularla temasta spesifik histolojik yanıtları ortaya çıkarmaktadır,
bunların içinde yüzey – reaktif silikanın sağlaması, kalsiyum ve fosfat gruplar ve
alkalin pH seviyeleri yer almakta ve bundan dolayı güçlü bir implant bağı için
istenilen koşulları ve yüksek bioaktivite sağlanmaktadır.(51) Rezorbe olabilen
polilaktik ve poliglikoid asitlerin sentetik polimerleri, tek veya farklı özelliklerle
kombine olarak, kemik yerine koymada uygulanmaktadır.(52) Poliglikoid asit daha
hızlı parçalanır buna karşın polilaktik asit daha uzun bir süre için kalmaktadır.(53)
Birkaç çalışma hayvan ve insanlarda bu kopolimerlerin faydalı etkilerini
- 26 -
göstermektedir. Ticari olarak var olan bir greft materyali eşit oranlarda her iki
komponentin kombine olan polilaktik ve poliglikoid asidin bir kopolimeridir. (49)
Bioaktif camların sadece partiküllerin osteokonduktif özellikleriyle değil aynı
zamanda osteostimulatif potansiyeliyle kemik tamirini arttırdıkları gösterilmiştir.
Klinik çalışmalar bioaktif camın sinüs agmentasyonunda otojen kemikle kombine
kullanılmasını değerlendirmiştir. Tadjoedin ve ark. otojen kemiğin tek başına
kullanılarak veya 50% BioGran ve 50% otojen kemik karışımıyla bilateral sinüs
greftlemesi arasında herhangi bir fark saptayamamıştır. Farklı bir çalışma ise bioaktif
cam/otojen kemik kombinasyonunun tek basamaklı sinüs agmentasyonuyla
kullanılmasının, greft öncesi 3-5 mm kemik yüksekliği bulunan hastalarda aynı anda
implant yerleştirilmesi için tahmin edilebilir sonuçlar verdiği ve yeterli kalite ve
hacimde mineralize doku yarattığını desteklemiştir.(54)
Bu materyalin sinüs agmentasyonunda yalnız başına ve otojen kemikle
kombine
edilmeden
kullanılmasının
implant
tedavisindeki
sonuçlarının
değerlendirilmesi ilginç olur.(54)
PepGen P-15TM
PepGen P-15TM ( Densplay Friadent CeraMed, Lakewood; CO ) tip I kollagenin α-1
zincirin 766 – 780 kalıntısında varolan serilere benzer olan 15 – aminoasit serisi ile
yüksek derecede korunmuş bir lineer peptittir.(55) Bu madde sığır kemiğinin mineral
komponenti ( Osteograf [ Dentsplay Friadent CeraMed]/N 300) ile P -15’in
kombinasyonudur. Anorganik sığır kökenli kemik mineral komponenti gerekli
kalsiyum fosfat ve osteokondaksiyon için gerekli olan doğal anatomik matriks
sağlar.(56) P – 15 kollagen ataşmanı için hücre yüzeyleri ile yarışmaktadır ve yüzey
üzerinde immobilize olduğunda hücrelerin adeziyonunu ilerletir. Kollagene benzer
- 27 -
bir şekilde fizyolojik süreci kolaylaştırmaktadır, mekanik sinyalleri değiştirir ve
hücresel farklılaşmayı ilerletir.(57) Diğer kemik agmentasyon materyalleri gibi,
inorganik sığır – kökenli matriks ile ilişkide olarak P – 15, periodontal, alveolar
defektler veya sinus yükseltme süreçlerinin tedavisinde yardımcı olmaktadır.(58)
Kalsiyum Sülfat
Kalsiyum sülfat, sentetik kemik greft materyalleri gibi 100 yılı aşkın uzun bir
klinik geçmişle beraber en kolay uygulanan materyal olarak kullanma özelliklerine
sahiptir. Periodontal hastalıklar, endodontik lezyonlar, alveolar kemik kaybı ve
maksillar sinus agmentasyonun tedavisi için başarı ile kullanılmaktadır.(59)
Membran bariyer olarak kullanıldığında kalsiyum sülfat örtücü olarak görev
yapabilir yara iyileşmesini kolaylaştırabilir ve greft materyalinin kaybını önleyebilir,
ayrıca doku ile bağdaşabilir ve iyileşme sürecini önlemez.(60) Kalsiyum tozu direkt
kalsiyum kaynağı olarak görev yapmakta veya diğer materyallere göre kalsiyum
sülfatın daha hızlı rezorpsiyon oranı, osteoprognitor hücreleri daha erken
oluşturur.(50) Kalsiyum sülfat hızlı bir şekilde rezorbe olur bir kalsiyum sülfat kafes
bırakır ve buda osteojenik aktiviteyi artırır kemiğin mineral fazını taklit eder ve
kemik formasyon hızına orantılı rezorbe olur.(61) Ricci yaptığı çalışmalarda
kalsiyum sülfatın yeni kemik formasyonunu köpeklerde 2 haftada indüke ettiğini ve
1 aydan sonra tam olarak rezorbe olduğunu göstermiştir.
Kemik rejenerasyonu için kullanılan greftlerin yanında, kalsiyum sülfat
Sottosanti ve Rocci(62) tarafından belirtildiği gibi implantolojide yönlendirilmiş
kemik rejenerasyonunda başarıyla kullanılmıştır. Birkaç in vivo deneysel
çalışmalarda kalsiyum sülfatın kemik formasyonuna sebep olduğu gösterilmiştir.(63)
- 28 -
Kalsiyum sülfat kemik rejenerasyonunda fiziksel bariyer görevi görme
özelliğine sahip olduğu Pecora tarafından gösterilmiştir.(64) Bu yazarlar kritik
boyutta bir defektte 3 haftalık gözlem periodu sonucunda kalsiyum sülfatın tek
başına kemik rejenerasyonuna izin verdiğini göstermiştir.(62)
Bio - Oss®
Bio - Oss® ( Geistlich Farma AG, Wohlhusen, İsviçre ) deproteinize olmuş
sterilize edilmiş sığır kemiğidir, %75 ile %80 arası poroziteye ve kortikal granüller
şeklinde 10 µm kristal çapına sahiptir.(65) Bio–Oss’un® osteogenesizi ilerlettiği ve
düşük rezorbiliteye sahip olduğu rapor edilmektedir. Bio - Oss® genelde maksillar
sinus tabanının yükseltilmesi için kullanılmaktadır. (66)
Hidroksiapatit
Kalsiyum fosfataz gibi bioseramikler hidroksiapatit ile önemli ile ilişkiye
sahiptirler ve dikkate değer başarılar elde etmişlerdir.(67) Fingranule® ( FinSeramik; Faenza RA, İtalya ) bir hidroksiapatittir ( Ca/P = 1.67 ± 0.03 ), patates
şeklinde granüller olarak yapılır ve 250 ile 600 µm arasında çapa sahiptir. Bu
hidroksilapatit çok düşük densite ve kristaliteye sahiptir; mikroyapısal açıdan
parçacıklar nanometrik boyut göstermekteler ( 0.05 ile 0.1 µm arasında ). Materyalin
spesifik bir özelliği yüksek porozite derecesidir nano boyuttan 10 µm’e kadar ve 10
ile 60 µm arasındadır.(68) Büyük osteositik lakünlerle yeni şekillenen kemik,
lameller kemik ve havers sistemi mevcuttur. Yeni oluşan kemik hidroksiapatiti
çevreler ve zaman içinde kalan bu hidroksiapatit partikülleri oluşacak yeni kemikle
yer değiştirirler. Kemik – partikül birleşme yerinde hiçbir aralık yoktur ve kemik her
zaman partiküllerle yakın temastadır. Bazen hisroksiapatit partiküllerine yakın
osteoblastlar gözlenir. Histomorfometri yeni oluşan kemiği %32 ± %2.5, marrow
boşlukları %40 ± %1.6 göstermekte ve rezidüel hidroksiapatit %34 ± %1.6 dır.(49)
- 29 -
Fizyogreft
Fizyogreft® greft materyali 50 – 50 laktik – glikolidden oluşan sentetik rezorbe
olabilen bir süngerdir ve D – L laktid – glikoidden daha hızlı çöker, bunun polimer
çökmesi 50 – 60 gündür. Bu materyal düşük bir yoğunluğa sahiptir ve tam
rezorpsiyonu 4 ile 8 ay sürmektedir. Boşluk doldurucu olarak başarı ile kullanılır,
çevre kemiksel dokulara benzer yeni kemiğin oluşmasını indüke eder ve en hızlı
çökme oranını göstermektedir.(69)
6.2. MODERN KEMİK GREFTİ TEKNİKLERİ
Kemik greftleri preimplant cerrahide genel olarak 2 şekilde kullanılır, kortikokansellöz blok greftler olarak veya kansellöz parçalı greftler olarak. Kortikokansellöz greftler alveolar çıkıntının genişlik ve yükseklik kayıplarını gidermek
amacıyla kullanılır. Parçalı kortiko-kansellöz kemik greftleri ise 2 veya 3 duvarlı
kemik defektlerini doldurmak amacıyla kullanılır örneğin sinüs tabanının
augmentasyonunda. Bu greftleri kullanırken greftler arasındaki iyileşme farkı göz
önüne alınmalıdır.(5)
Blok kortiko-kansellöz kemik greftlerine nazaran, çoğu parçalı kansellöz
kemik grefti orjinal greftten meydana gelen yeni kemik formasyonu gösteren
bölgelerde canlı kalabilmektedir. Dehisens meydana gelse bile sadece az miktarda
greft kaybı görülür. Primer iyileşme sadece alıcı yüzün dış kemik yüzeyinden değil,
örtücü yumuşak dokudan meydana kapiller gelişmeye bağlıdır. Parçalı kansellöz
kemik greftlerinin başarı oranı yüksektir ve sonuçları önceden tahmin edilebilirdir.
Kontaminasyon probleminden dolayı parçalı greftleri onlay greftler olarak kullanmak
- 30 -
güçtür. Küçük miktarda alveolar defektlerin görüldüğü sınırlı vakalarda bariyer
membranların kullanımı yararlı olabilir. (70)
Kortiko-kansellöz blok greftler yeni kemikle yer değiştirmek için neredeyse
tamamen rezorbe olacak bir iskelet yapı ortaya çıkarır. Bu remodelasyon işlemi
karmaşık kemik değişimine bağlıdır.(71) Bu işlemin engellenmeden sonuçlanması
için kortiko-kansellöz greftin alıcı sahaya rijit bir biçimde fikse edilmesi gerekir.
Greftle alıcı yüzey arasında görülecek en ufak bir mikrohareket alıcı sahada kapiller
gelişimini tehlikeye atacak, bunun sonucu greftte kayıp ve avasküler nekroz
görülecektir. (5)
Herhangi bir mikrohareketi engellemek amacıyla kemiğin en az 2 vidayla fikse
edilmesi önerilir. Diğer önemli faktörler ise greftle alıcı yatak arasındaki yakın
adaptasyon ve yumuşak dokunun gerilimsiz bir şekilde örtülmesidir. Greftin
boyutuna bağlı olarak, revaskülarizasyon yaklaşık 2 hafta içinde gerçekleşecektir,
daha sonra remodelasyon süreci başlar. Kemikiçi implantların greftin yerleşimini
takiben en az 3 ay yerleştirilmemesi tavsiye edilir.(72)(73) Buna rağmen bazı
çalışmalar implantın erken yerleştirilmesini takiben başarılı sonuçlar alınabildiğini
göstermiştir.
Buna göre, preimplant cerrahide kemik greftlerinin başarısı; (1) rijit fiksasyona
(2) alıcı bölgenin vaskülaritesine (3) greftin kendisinin osteojenik özelliğine (4)
yumuşak doku örtüsünün kalitesine bağlıdır. Geçmişte atrofik mandibula ve
maksillada rijit fiksasyon uygulanmadan yerleştirilen greftlerde başarı oranında
düşüş kaydedilmiştir.(74)
- 31 -
Ayrıca küçük alveoler defektleri tamir etmek amacıyla allogreftler ve
yönlendirilmiş kemik rejenarasyonu teknikleri kullanılmaktadır günümüzde; otojen
kemik greftleri, kemik defektlerinin ve alveolar atrofinin iyileştirilmesinde altın
standart olarak görülür.(70) Alveoler defektlerin iyileştirilmesi için mandibular
simfiz veya ramus bölgesinden traşlanan lokal greftler uygundur.
Mandibuladan alınan lokal greftlerin avantajları:
-rahat cerrahi girişim
-zarlı kemik yapısı
-Verici ve alıcı sahaların yakınlığı
-Hastanın pre-implant cerrahisi için ideal metod
Simfiz bölgesinden kemik alınırken ortaya çıkan komplikasyonlar olarak
mental sinir zedelenmesine bağlı duyu kaybı ve yakındaki anterior dişin vitalitesinin
kaybı gösterilebilir.(75) Nkenke bu vitalite kaybı olasılığını azaltmak için osteotomi
bölgesinden 8 mmlik bir güvenlik sınırı önerir.(75) Simfiz bölgesinden alınan kemik
belirli kalınlıkta olması vurgulanmaktadır. Araştırmacılar simfiz bölgesinden tam
kalınlıklı kemik alımı sonucu üst solunum yolunun tehlikeye atılacağını ve bunun
ölümcül olabileceğini belirtiyorlar.(5)
Ramustan kemik kaldırma sırasında simfiz bölgesine göre daha az
komplikasyon ortaya çıktığı belirtilmiştir.(76) Buna rağmen Misch ramus bölgesinde
simfize kıyasla daha az değerli kemik sahasının olduğunu rapor etmiştir.(76)
CLAVERO ve LUNDGREN(77) mandibulanın ramus bölgesinden daha fazla işe
yarar kemik sağlaması için yöntemler ortaya sürmüştür.
- 32 -
Alveolar rekonstrüksiyon için daha fazla otojen kemiğe ihtiyaç duyulduğu
durumlarda, genellikle implant öncesi dişsiz çenelerde, iliak kemik gibi uzak verici
sahalara ihtiyaç vardır. BLOOMQUIST ve FELDMAN(78) ve daha sonra
NKENKE(79) anterior iliak bölgedense posterior bölgeden kemik alınmasını
savundular. Bunun sebebi ise morbidite oranı daha düşüktür ayrıca arka bölgede ön
bölgeye göre daha fazla değerli sahanın olmasıdır.(5)
Daha büyük defektler meydana çıktığında maksilla ve mandibulanın
rekonstrüksiyonu için revaskülarize kemik greftleri kullanıldı. Bunun bir dezavantajı
kontürdeki kesinliğin azlığı sebebiyle mimiklerde zorlanmadır. Sonuç olarak protezin
yapılmasına zorluk çıkartacak şekilde implantın yerleştirilmesi tehlikeye atılmış
oluyordu.(80)
şekillendirilmiş
Serbest
blok
yapıların
greftleriyle
içine
serbest
sıkıştırılması
özel
greftlerin
yumuşak
doku
önceden
çevresinin
vaskülarizasyonunu sağlamak açısından alternatif oluşturmaktaydı.(81)
Özetle, preimplant cerrahide otojen kemik greftlerinin uygulanması, tahmin edilebilir
ve güvenilir sonuçlar doğurduğu için kendini kabul ettirmeyi başardı. Greftin boyutu
ve tipi genel olarak alıcı sahanın şekline ve büyüklüğüne bağlıdır ve ayrıca cerrahın
tercihine bağlıdır. Otojen büyüme faktörlerinin kanıt olarak sunulması hala kesin
değildir.(82)
6.3. ONLEY KEMİK GREFTLERİ
Dişsiz atrofik maksillanın otojen kaburga kemiğiyle greftlenmesi ilk olarak
Terry Albright ve Baker tarafından açıklanmıştır.(83) Alveoler kret yüksekliklerinde
- 33 -
ve damak kubbesi formunda bozukluğa yol açacak kemik kayıplarında onley kemik
grefti ilk olarak düşünülecek uygulamalardandır.
Onley greftler intraoral ve ekstraoral bölgelerden elde edilebilmektedirler.
İliyak bölgeden, tibia,fibula, skapula, kalvarya, maksiller tüber,mandibular
retromolar, ramus ve simfiz bölgelerindenelde edilen otojen kemik greftleri kemik
defektlerinin tedavisinde kullanılmıştır.(34)
Bu tekniğin dezavantajları verici sahaya uygulanacak ikinci bir cerrahi işlem,
öngörülemeyen postoperatif rezorpsiyon, postoperatif sekonder yumuşak doku
işlemlerinin olması ve bazı vakalarda protez safhasının daha ileri bir tarihe
ertelenmesidir.(2)
İntraoral bölgeden elde edilen kemik greftleri uygun cerrahi teknikler ile
yerleştirildiğinde kret genişliğinde 4-7 mm, vertikal kret yüksekliğinde ise
2-3
mm kazanç elde edilebilmektedir.(37)
Elde edilen greft blokları mobiliteyi ve rezorpsiyonu azaltmak amacıyla alıcı
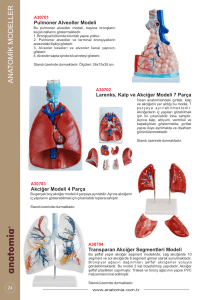
sahaya küçük vidalar yardımıyla fikse edilebilir.(Şekil 1) İmplantlar greftleme
işleminin
yapıldığı
seansta
veya
primer
iyileşme
görüldükten
sonra
yerleştirilebilir.(2)
Onley blok kemik greftleri cerrahi sonrasında genellikle rezorbe olarak
boyutsal değişiklik gösterebilmektedir. Onley greftlerde yaklaşık %25-47 oranında
- 34 -
kemik rezorbsiyonu meydana gelebilmekte ve ortalama kemik kazancı 5 mm’den az
olabilmektedir.(84)
Onley greftlerle ögmentasyon yapıldıktan sonra mandibulaya yerleştirilen
implantların 10 yıl sonra başarı oranı %89-97 iken maksillada bu oran %49-74 olarak
bulunmuştur.(85) Bununla birlikte blok formunda allojen greft materyallerinin hiçbiri
kemik olusumu ve iyilesme üzerine otojen blok greftleri kadar etkili değildir.
Onley kemik greftleri okluzal yüklere direnme becerisine sahiptir, özellikle de
anterior dentisyonda bir kemik labial korteks sağlar. Şimdiki bulgular gösterdi ki tek
diş alanı gibi kısa mesafelerin, 2-3 diş alanı gibi orta mesafelerin ve uzun mesafelerin
agmentasyonu için uygundur. Hem vertikal hem de horizontal agmentasyon başarı ile
sağlanır.(86) Misch ise sadece kısa mesafelerin intraoral blok kemik greftleriyle
agmente edilmesini önerir.
Şekil 1: Vida ile fikse edilmiş onley kemik grefti
- 35 -
BLOK KEMİK GREFTLERLE MANDİBULANIN 3 BOYUTLU
REKONSTRÜKSİYONU
Lokal anestezi sonrasında, klasik flep tekniği veya tünel tekniğiyle alıcı saha
ortaya çıkarılır. Retromolar veya çene ucu bölgesinden otojen kemik bloğu elde
edilir. Kortikal blok elmas diskle uzun aksı boyunca iki parçaya ayrılır. Böylelikle
kalınlık yarıya indirilmiş olur. Parçalardan birisi bukkal duvarın rekonstrüksiyonunda
diğeri ise palatal duvarın rekonstrüksiyonunda kullanılır arada kalan boşluk ise
kemik partikülleri ile doldurulur. Tünel preparasyonu tercih edildiğinde kretin
okluzal sınırlarını rekonstrükte etmek için ince bir blok kullanılır. Blok ve alveoler
kret arasında kalan boşluk ikinci blok bukkal sahaya vidalanmadan önce kemik
partikülleriyle
doldurulur. 4 aylık iyileşme
döneminden sonra
implantlar
yerleştirilir.(87)
1995 ve
2002 yılları arasında mandibular blok greftleriyle 3B
rekonstrüksiyonla 209 hasta tedavi edilmiştir. Otojen kemik retromolar bölgeden
elde edilmiştir. Postoperatif olarak 389 implant yerleştirilmiştir. Toplam yedi
komplikasyonla karşılaşılmıştır:dördü greftin açığa çıkması, üçü ise greft bölgesinde
yumuşak doku migrasyonu olarak görülmüştür. 8-9 yıl sonucu sadece üç implant
kaybedilmiştir. Diğer 386 implant herhangi bir ciddi hastalık görülmeden halen
yerindedir. Ortalama vertikal agmentasyon yaklaşık 7.8 mm’dir. Hacim kazancı ilk
postoperatif yılda 10-15 % rezorpsiyon göstermiştir. Takip eden yıllarda, hacimsel
bazda herhangi bir değişiklik gözlenmemiştir. 3B rekonstrüksiyon metodu, vertikal
defektlerin tek kortikal blokla veya membranlarla birlikte GBR tekniğiyle tedavi
edilmesine iyi bir alternatiftir. Düşük komplikasyon oranı, iyi kemik rejenerasyonu
ve 7.8 mm’lik vertikal agmentasyon cesaret vericidir.(87)
- 36 -
6.4. SİNÜS LİFT
Dişhekimliğinin modern çağına girildiğinde implant tedavisi mükemmel bir
tedavi seçeneği olarak karşımıza çıkmaktadır. İmplant tedavisi sadece kısmi diş
eksikliklerinin konservatif ve estetik bir alternatif olmasının yanında total diş
eksikliklerinin tedavisinde de stabil bir yapı sağlamaktadır. Dental implantlar yeterli
kalite ve miktarda kemiğin olduğu durumlarda uygulanabilir bir tedavi biçimi
olabilir.(88)
Buna rağmen, hastalar yetersiz alveoler kret miktarına sahip olduğu
durumlarda bu durum hastalara implant tedavisinin uygulanmasını tehlikeye
atabilmektedir. Bu problem özellikle kret rezorpsiyonu, sinüs pnömatizasyonu zayıf
kemik duvarlarının görüldüğü posterior maksillada görülmektedir. Bu anatomik
kusuru düzeltmenin prosedürü maksiller sinüs tabanının yükseltilmesinden
geçer.(88)
Tarihsel Geçmiş
Maksiller sinüs elevasyonu ilk olarak 1976 yılında Alabamada bir implant
konferansında Tatum tarafından açıklanmıştır ve 1980 yılında Boyne tarafından
yayınlanmıştır.(89) Bu ihtiyaç posterior maksillada implant uygulanabilmesinden
kaynaklanmaktadır. Prosedür günümüzde sıklıkla uygulanmakta olan preprostetik
cerrahi operasyonlardan biridir. İlk kez açıklanmasından itibaren, farklı greft
materyalleri, klasik tekniğe getirilen modifikasyonlar ve farklı tekniklerin
karşılaştırılması amacıyla birçok makale yayınlanmıştır.(90)
- 37 -
Sinüsün Anatomisi
Maksiller sinüs tabanı burun duvarına tepesi zygomaya bakan bir piramit
şeklindedir. Kalıcı dişler sürene kadar sinüsün boyutu önemsizdir. Yetişkin bir
bireyin ortalam sinüs boyutları 2,5-3,5 cm genişliğinde, 3,6-4,5 cm yüksekliğinde,
3,8-4,5 cm derinliğindedir.(91) Yaklaşık 12-15 cm3 hacme sahiptir.(92) Ön kısımda
kanin ve premolarlar bölgesine kadar uzanmaktadır. Sinüs tabanının en alt kısmı ise
birinci molar diş hizasındadır. Eğer ilgili bölge dişsiz ise yaşla beraber sinüsün
boyutları da artacaktır. Pnömatizasyon miktarı kişiden kişiye ve taraftan tarafa
değişmektedir. Bu olay posterior maksilladaki lateral ve okluzal alveolar kemiği
kağıt inceleğine getirebilmektedir.
Maksiller sinüs kemik kavitesi Schneiderian membranı olarak da bilinen sinüs
membranı ile çevrilidir. Bu membran diğer solunum bölgelerinde olduğu gibi silli
epitelden oluşmaktadır. Bu membran orta meatusta bulunan ostium sayesinde nazal
epitelle doğrudan bağlantıdadır. Membran yaklaşık 0,8 mm kalınlığa sahiptir. Antral
mukoza
nazal
mukozadan
daha
ince
ve
daha
az
vaskülarizedir.(86)
Maksiller sinüsün kanlanması her ikisi de maksiller arterin bir dalı olan
posterior superior arter ve infraorbital arter tarafından sağlanmaktadır. Lateral antral
duvar üzerinde bu iki arter arasında önemli anastamozlar vardır. Daha büyük palatin
arteri de sinüsün alt kısmını destekler.(93)
Maksiller sinüsün kan desteği terminal dallardan geldiği için sinüs lift
operasyonu sırasında kanama görülmesi nadirdir. Sinüsün sinir desteği trigeminal
sinir maksiller kısmına ait olan superior alveolar sinirden sağlanmaktadır.
- 38 -
Cerrahi Teknikleri
Günümüzde, literatürde maksiller sinüs elevasyonu ile ilgili 2 ana yaklaşım
vardır. İlki, Tatum tarafından ortaya çıkarılan ve daha yaygın olarak uygulanan
lateral antrostomidir. Daha güncel olarak Summers(94) ikinci bir yaklaşım
getirmiştir. Bu da osteotomların kullanıldığı kretal yaklaşımdır. Kretal yaklaşım
sinüs elevasyonunda daha konservatif bir metod olarak görülmektedir.(88)
Lateral antrostomi
Alveol sırtlarında kret üzerine yapılan bir insizyonla başlar. Bazen bu insizyon
daha sıkı yara kapanışı sağlamak ve yara dehisensini önlemek için daha geniş
keratinize bağlantılı gingivayı korumak amacıyla biraz palatinale kaydırılabilir. Daha
sonra lateral antral duvara girişi sağlamak amacıyla tam kalınlıklı bir flap kaldırılır.
Flap istenilen seviyeye ulaştığında, maksillanın yan desteğinde U şeklinde bir giriş
elde etmek için antrostomi uygulanır.(Şekil 2) Bu giriş ağzının yüksekliği yeni sinüs
tabanının son horizontal pozisyonuna izin vermesi için sinüs genişliğini
geçmemelidir. Daha sonra bir antral küret yardımıyla sinüs membranı kemik
tabandan yükseltilir.(Şekil 3) Marx ve Garg kanamayı sınırlandırmak, daha iyi
görüşü sağlamak ve daha ileri disseksiyonlar açısından oluşturulan boşluğa 5
dakikalığına 2% lidokain ile 1:100000 epinefrinle ıslatılmış pamuğun koyulmasını
önermektedirler. Giriş ağzını mediale kaydırmadan önce sinüs membranını her yönde
serbestlemek önemlidir.(88)
Sinüs membranı genişletilmiş giriş ağzı sayesinde yükseltildikten sonra bir
boşluk oluşmuş olur. Bu boşluk daha sonra implant yerleştirilmesine olanak
tanıyacak şekilde farklı greft materyalleri ile doldurulur.(Şekil 4) İmplantların farklı
- 39 -
greft materyalleri üzerinde prognozlarını incelemek üzere birçok araştırma
yapılmıştır. Otojen kemik kemik greftinde altın standart olarak kalmaktadır.(95) İliak
kret, çeneucu, ramusun ön bölgesi ve tüber bölgeleri maksiller sinüs lift
operasyonunda yaygın verici sahalardır. Tek başına veya otojen kemikle karıştırılmış
hidroksiapatit de uygulanabilir bir alternatif ortaya sunmaktadır.(96 Alıcı sahayı aşırı
doldurmamaya dikkat edilmelidir çünkü bu membran nekrozuna sebep olabilir.
İmplantlar greftle aynı zamanda veya greftin olgunlaşması için 12 aya kadar
süren periodlar sonunda yerleştirilebilir. Başlangıç alveoler sırt kalınlığı bu iki metod
arasında karar vermede güvenilir bir işaret olarak görülmektedir. Eğer kemik
kalınlığı 4mm veya daha az ise implantın stabilitesi tehlikededir. Bunun için 2
aşamalı lateral antrostomi ele alınmalıdır. Tek aşamalı prosedür hasta ve hekim
açısından daha az zaman alır. Ancak, tekniğe daha hassastır ve başarısı kalan kemik
miktarına bağlıdır.(88)
Kretal Yaklaşım
Lateral antrostominin bir dezavantajı da cerrahi giriş amacıyla geniş bir flepin
kaldırılması gerekliliğidir. Summers 1994 senesinde maksiller sinüs elevasyonunda
osteotomların
kullanıldığı
daha
konservatif
bir
teknik
ortaya
atmıştır.
Bu teknik kret üzerinden yapılan bir insizyonla başlar. Alveoler kreti açığa çıkarmak
için tam kalınlıklı flap kaldırılır. En küçük boyutta osteotom kemik içine yerleştirilir.
Osteotom uzantısı için gerekli derinliği ortaya çıkarmak için sinüs altında preoperatif
kemik yüksekliği ölçümü yapılmalıdır. Amaç araçları sinüs membranının altına
kadar uzatmaktır. Alveolü
genişletmek için artan boyutlarda osteotomlar
oluşturulmuştur. Her daha geniş osteotomun yerleştirilmesiyle birlikte kemik
sıkıştırılır, lateral ve apikale ittirilir. Summers’a göre bu tekniğin en önemli özelliği
- 40 -
normal olarak tip IV kemiğin bulunduğu posterior maksillada kemik yoğunluğunu
arttırmasıdır.(94En geniş osteotom implant sahasına yerleştirildiğinde hazırlanmış
kemik karışımı greft materyali olarak eklenir. Birçok miktarda greft materyali
kullanılmasına rağmen Summers %25 otojen kemik, %75 hidroksiapatit karışımını
önermektedir. Sinüs tabanı elevasyonunun son basamağı greft materyali yerindeyken
en geniş osteotomun yeniden yerleştirilmesidir. Bu sinüs membranına bir basınç
oluşturur ve onun yukarı kalkmasına sebep olur. İstenen yükselmeyi sağlamak
amacıyla ek olarak greft materyali kullanılabilir. Yeterli yüksekliğe gelindiğinde
implant sabitleyici yerleştirilir. İmplant sabitleyicinin çapı en geniş osteotomdan
daha fazla olmalıdır. Son osteotom görevi görür.
Kretal osteotom tekniğinin avantajı daha az invaziv olmasıdır. İmplantlara
daha fazla stabilite kazandıracak şekilde maksiller kemik yoğunluğunu arttırır.
Ayrıca daha az otojen greft materyali kullanma potansyeline sahiptir. Summers kretal
insizyonun otojen kemiğin traşlanabildiği tüber bölgesine doğru kaydırılmasını
önermiştir.(97 Kretal yaklaşımın dezavantajı ise artan kemik yüksekliği 6 mm’den az
ise implantın stabilitesinin sağlanamamasıdır.
Bu yaklaşım sayesinde osteotomi sırasında osteotomun uzun aksının yanlış
yerleştirilmesi olasılığı da yüksektir.(88)
Yapılan bir araştırmada PRP eklenmiş biogran ve otojen kemik greftlerin
Micro-CT incelemesi yapılmış; %48’den %68’e varan oranlarda Toplam Kemik
Hacmi ve Toplam Hacim’de pozitif etkisi olduğu görülmüştür. Sonuçta PRP
eklenmiş biogran ve otojen kemik karışımının greftin iyileşmesi için gereken süreyi
- 41 -
kısalttığı ve kısa sürede yüksek miktarda kemik oluşturarak yeni kemik
formasyonunu arttırdığı gösterilmiştir.(42)
Sonuç olarak; dişsizliği implant ile restore etmek dikkatli bir tedavi
planlaması gerektirmektedir. Bu özellikle pnömatize maksiller sinüsün implant
yerleştirirken alveol miktarını sınırladığı posterior maksillada geçerlidir. Maksiller
sinüs tabanı yükseltilmesi bu problemi çözmek için en yaygın çözümü ortaya sunar.
Lateral antrostomi daha büyük kemik oluşumu sağlarken daha fazla cerrahi girişim
gerektirmektedir. Kret yaklaşımı ise minimal invaziv bir yaklaşımdır fakat sınırlı
miktarda kemik oluşumu sağlar. Buna göre, uzmanlar klinik ihtiyaçlara göre uygun
olan yaklaşımı seçmelilerdir. Ek olarak, cerrahi komplikasyonları minimize etmek
amacıyla çevre anatomik oluşumlara dikkat edilmelidir.(93)
Yapılan bir başka çalışmada OsteoGraft/N’in sinüs elevasyonu işleminde
kullanılması araştırılmıştır. Araştırma 215 implantla 113 sinüs elevasyonu işlemini
içermekteydi.
6-9-12-15
Aylık
dönemlerde
yapılan
incelemeler
sonucu
OsteoGraf/N’in sinüs tabanı yükseltme prosedüründe etkili bir greft materyali olduğu
görülmüştür.(98)
Ayrıca non-rezorbabl e-PTFE membranın lateral pencerenin ötesine
yerleştirildiğinde membran kullanılmayan vakalara nazaran vital kemik oluşumunda
önemli artış gözlendi.(98)
Sinüs lift operasyonları sonucu sütur başarısızlıkları, akut sinüzit, greft
materyalinin absorpsiyonu gibi komplikasyonlarla karşılaşılabilir.
- 42 -
Papa F. ve arkadaşlarının yapmış olduğu bir çalışmada 50 sinüs lift vakası
incelenmiştir. Bunlardan coral hidroksiapatit ile greftlenmiş vakaların 6%’sında,
otolog kemikle greftlenmiş vakaların 17%’sinde, heterolog kemikle greftlenmiş
vakaların 40%’ında yeterli kemik agmentasyonunda eksik tespit edilmiştir.(99)
Andreana S. ve arkadaşlarının gerçekleştirmiş olduğu bir çalışma sonucu
sinüs lift işleminde kalsiyum sülfatın yalnız başına veya DFDBA ile birlikte başarılı
şekilde kullanılabileceğini göstermişlerdir. Buna rağmen histolojik deliller kalsiyum
sülfatın DFDBA ile kombine kullanıldığı durumlarda son partiküllerin yeni oluşan
kemikte ameliyattan birkaç ay sonra bile bulunabildiğini gösterir.(62)
Şekil 2:Lateral antrostomi
Şekil 3:Sinüs membranın elevasyonu
Şekil 4:Boşluğun greftle
doldurulması
- 43 -
6.5. DİSTRAKSİYON OSTEOGENEZİSİ (OSTEODİSTRAKSİYON)
Alveoler kret agmentasyonu için kemik grefti, GBR, farklı alloplastik
materyaller kullanılmaktadır. Fakat bu teknikler için hala birtakım zorluklar
mevcuttur. Kemik grefti uygulamada verici saha gereksinimi, greftin rezorpsiyonu
gibi durumlar buna örnek gösterilebilir.(100)
Uzun kemikler için distraksiyon osteogenezisi teknikleri gösterilmiş olmasına
rağmen bunlar kraniofasiyal kemiklere de uygulanabilir.(101) Ilizarov yeni oluşan
kemiğin distraksiyon vektörüne paralel olarak meydana geldiğini göstermiştir.(102)
Bu araştırma periodontal hastalık, travma, kist, tümörler ve konjenital deformitelere
bağlı alveoler defektlerin distraksiyon osteogenezisi yoluyla agmentasyonunun olası
olduğunu göstermiştir.(100)
Gelişmiş
minyatürize
distraksiyon
aletleri
sayesinde
alveoler
kemik
distraksiyonu kret agmentasyonu için bir tedavi modeli olarak görülmektedir.
Alveoler Kret Distraksiyonu
Öncelikle agmentasyon sahasında mukoperiostal flep kaldırılır ve hareketli
alveoler kemik segmenti oluşturan U-şeklinde alveoler kemik osteotomisi
gerçekleştirilir. Alveoler rekonstrüksiyon hareketli kemik segmentinin özel bir
distraktör yardımıyla hareket ettirilmesi esasına dayanır.
Alveoler kret agmentasyonu 2 kategoriye ayrılabilir: alveoler segmentin
vertikal yönde hareket ettirildiği, yüksekliğinin arttırıldığı vertikal agmentasyon ve
hareketli segmentin horizontal yönde hareket ettirildiği, genişliğin arttığı horizontal
agmentasyon. Atrofik alveoler kretlerin görüldüğü çoğu vakada sadece vertikal
distraksiyon yeterli olmaktadır.(100)
- 44 -
Vertikal Alveoler Distraksiyonu
Alveol kret veya vestibuler mukozal insizyon yoluyla alttaki kemikten aşırı
ayrılmasından kaçınarak mukoperiostal flep kaldırılır. Fissür frez yardımıyla
osteotomiye başlanır. Karşılıklı veya sagital testere yardımıyla vertikal ve horizontal
alveoler kesiler gerçekleştirilir ve hareketli segment oluşturulur. İlk olarak,
distraktörün yerleştirilmesinde hareketli segmentin stabilitesi amacıyla vertikal
osteotomi
yalnızca
bukkal
kortikal
kemiği
içerir.
Distraksiyon
aletinin
bağlanmasından sonra osteotom yardımıyla vertikal osteotomi lingual kortekste
sonlandırılır. Tavsiye edilen minimum hareketli segment yüksekliği 5mm’dir.(Şekil
5)
5-7 günlük bekleme periodundan sonra günlük 0,5-1,0mm’lik oranda alveoler
distraksiyona başlanır. Distraksiyon aleti genelde günde birden üçe kadar sayıda
aktive edilir. Distraksiyon tamamlandığında 6-12 hafta arası pekiştirme periodu
önerilir. Yeni oluşan kemiğin radyografik kontrolünden sonra distraktör lokal
anestezi altında çıkarılır. Kısa pekiştirme periodları relaps riskini arttırır. Relapsı
önlemek amacıyla 1-2 mm fazla distraksiyon yapılması değerlendirilebilir.(100)
Horizontal Alveoler Distraksiyon
Yumuşak doku ensizyonundan ve mukoperiostal flep preperasyonundan sonra
alveoler kemiğin vertikal split osteotomisi uygulanır ve horizontal distraksiyon
vidaları yerleştirilir.(103) Lingual kortikal kemiğin penetrasyonunu önlemek
amacıyla distraksiyon vdalarının ucu kör olmalıdır. Vertikal agmentasyona benzer
şekilde 5-7 gün beklemeden sonra distraksiyon vidalarını günlük aktive ederek
distraksiyona başlanır. 12 haftalık pekiştirme sürecinin ardından distraksiyon vidaları
çıkartılır ve distrakte edilmiş kemiğe implantlar yerleştirilebilir.(100)
- 45 -
Endikasyonları
Periodontal hastalık, travma veya konjenital deformiteler sonucu oluşmuş
atrofik alveoler kemikler osteodistraksiyon için endikasyon oluşturabilir. Bu teknik
ayrıca kist veya tümör nedeniyle marjinal kemik rezeksiyonu görmüş hastalara da
uygulanabilir. Bu vakalarda önceden greft uygulanmış bölgelere de distraksiyon
uygulanabilir. Özellikle ankiloza uğramış dişle birlikte, diş segmentlerinde görülen
vertikal malpozisyonların sebep olduğu open-bite vakaları da ortodontik bir
endikasyon oluşturur.
Çok kısa intermaksiller mesafe görülen vakalarda vestibuloplasti veya sinus
lift amacıyla osteodistraksiyon uygulanabilir.(100)
Kontrendikasyonları
İleri derece atrofik mandibulada, ileri osteoporoz görülen kişilerde, aşırı yaşlı
bireylerde, fraktür riski görülen, distraktörün yerleştirilmesine engel taşıyan
durumlarda osteodistraksiyon kontrendikedir.(100)
Distraksiyon Aletleri
Distraksiyon
aletleri
iki
kategoriye
ayrılırlar:
endoosseöz,
ekstraosseöz(subperiostal). Alveoler kretin atrofisi, yumuşak dokuların durumu,
distraksiyon miktarı ve distraktörün spesifik özellikleri hangi tipin seçileceğini
etkileyen faktörlerdir.(Şekil 6)
- 46 -
Ekstraosseöz (subperiostal) Distraktör
Subperiostal distraktörler alveoler kemiğin yan yüzeyine yerleştirildikleri için
dişlere sahip alveoler segmentlerin hareket ettirilmesi için daha uygundurlar. Diğer
taraftan distraktörü örten mukoperiostal flepin gevşek olması enfeksiyon riskini
arttırır. En bilinen ekstraosseöz alveoler distraktörlerden birisi de Vertikal
Distraktördür.(KLS Martin, Jacksonville, FL)
Endoosseöz Distraktör
Distraktörün büyük bir kısmı alveoler kretin içine yerleştirildiği endoosseöz
distraktörler implant tedavisinin ilk basamağı olarak alveoler kret agmentasyonuna
daha uygundur. Bu endoosseöz distraktör halen kullanılmaktadır.:ACE OsteoGenic
Distractor, DISIS Distraction Implant ve LEAD (Leibirger Endoosseous Alveolar
Distraction) System(100)
Şekil 5:Distraktörün aktive edilmesi
Şekil 6:Distraksiyon aleti
6.6. İNTERPOZİSYONEL KEMİK GREFTLERİ
Bu teknik en çok maksiller anterior bölgede endikedir. 3-8 mm. Orta derecede
atrofi görülen bölgelerde vertikal hareket gerekliliğinde kullanılır. Buna göre alveol
segment hareket ettirilerek istenen vertikal yükseklikte fikse edilmelidir.(Şekil 7)
Cerrahi uygulanacak bölgenin daha küçük kaldırılan flepin daha az olduğu için onley
- 47 -
blok greftlerine göre daha basit bir işlemdir. Posterior mandibulada uygulanabilmesi
için sinirin üzerinde en az 4mm kemik olması gerekmektedir.
Bu tekniğin dezavantajları hospitalizasyon, genel anestezi, verici sahada
cerrahi bir işlem gereksinimi ve operasyon sonrası 3-5 ay protez uygulanamamasıdır.
Birçok hastada post-operatif nörosensörel bozukluklar tespit edilmiştir.(2)
Şekil 7: İnterpozisyonel kemik grefti
6.7. HİDROKSİAPATİT AGMENTASYONU
Atrofik mandibula ve maksillanın rezorpsiyon, verici saha morbiditesi ve
hospitalizasyon ihtiyacı gibi problemlerden kurtularak tedavisi amacıyla alloplastik
materyaller üzerine araştırmalar yapılmıştır. HA sentetik olarak veya biyolojik
kaynaklardan elde edilebilen aşırı biouyumlu bir materyaldir. Subperiostal olarak
yerleştirildiğinde fiziksel ve kimyasal yollarla kemiğe tutunur.
Histolojik olarak her partikül vasküler doku infiltrasyonu ile birlikte fibröz
doku kapsülüyle çevrili olarak görülür. HA partiküllerinin bu enkapsülizasyonu
herhangi bir enflamasyon görülmeden meydana gelir.(104) HA’in agmentasyon
amacıyla kullanım endikasyonları kemik greftlerine yakındır.
- 48 -
Bu tekniğin uygulanmasında subperiostal tünel tekniğinden yararlanılır. Buna
göre nörovasküler demetlere dikkat ederek kemikte agmentasyon sağlanır. Tünel
hazırlandıktan sonra önceden HA partikülleri yerleştirilmiş bir şırınga yardımıyla
istenilen yükseklik ve kontur elde edilene kadar enjekte edilir. Bazı araştırmacılar
HA’in postoperatif yerdeğiştirmesini minimize etmek amacıyla splintlemeyi uygun
görmektedir.(2)
Vestibuloplasti ve deri grefti uygulamaları operasyondan 8-12 hafta sonra
uygulanabilir. Bu süreçte HA partikülleri bağlayıcı doku sayesinde fikse edilir. HA
agmentasyonu sayesinde verici saha cerrahi işlemi elimine edilmiştir. HA rezorbe
olmayan, post operatif greft kaybı göstermeyen ve daha sonra uygulanacak yumuşak
doku greftlerine iyi bir vasküler yatak sağlayabilen bir materyaldir.
Bu tekniğin dezavantajı ise HA’in tünel içine yerleştirilmesi ve istenilen
konturun sağlanmasında ortaya çıkmaktadır. Yapılan araştırmalar atrofik kemiklerde
HA’in kullanımının kemiğin gücünü arttırdığı fakat kemik greftleri kadar başarılı
olmadığını ortaya koymuştur.(2)
6.8. YÖNLENDİRİLMİŞ KEMİK REJENERASYONU (GBR)
Yönlendirilmiş kemik rejenerasyonunda (GBR) kemik greftinin iyileşmesi,
kemik oluşumu arzulandığı bölgeler bir membran yardımıyla örtülenir.(Şekil 8)
Osteopromosyonun temel amacı epitelial hücreler veya fibroblastlar gibi hücreleri
kemik oluşumu istenilen bölgeden uzak tutmaktır.(2)
- 49 -
1982 yılında Nyman periodontal ligament rejenerasyonu arzu edilen bölgede
membran bariyerler yardımıyla istenmeyen hücreleri uzak tutmayı başarmıştır.(105)
Dahlin de aynı tekniğin implant çevresinde gelişen kemik bölgesine de
uygulanabileceğini göstermiştir.
Günümüzde membran örtüsü olarak birçok materyal kullanılmaktadır.
Bunlardan yaygın olanlarından birisi polytetrafloretilen (EPFTE)’dir. Bu membran
rezorbe olmaz ve istenilen iyileşme sağlandığında çıkartılması gerekir. Bunun
yanında ikincil bir cerrahi işlemden kurtulmak amacıyla rezorbe olabilen membran
bariyerler de mevcuttur.
Membran materyali kemik greftin uygulandığı defekt veya kret konturları
bölgesine uygulanabilir. Rezorbe olmayan membran materyali iyileşme başlığının
takılacağı ikinci aşama cerrahi işlem sırasında çıkarılabilir.
Bazı vakalarda kemik grefti uygulamadan yalnızca membran kullanılması
yeterli olabilir.(106) Bu tip vakalarda membran vidalar yardımıyla kemiğe fikse
edilir ve altında oluşacak yeni kemik için boşluk yaratılır. Daha sonra bu boşluğun
kanla dolmasıyla osteoblastlar kemik oluşumunu başlatır.(2)(Şekil 9)
- 50 -
Şekil 8:Bariyer membran uygulanması
Şekil 9:Kemik oluşumu
6.9. TÜBEROPLASTİ
Maksiller tüberositeler yerleştirilen protezin tutuculuğu açısından önemli
bölgelerdir. Alveoler kretlerin ve damak kubbesinin yeterli formda olduğu fakat
tüberlerin yetersiz olduğu durumlarda cerrahi bir işlemle protezin retansiyonu
arttırılabilir. Bu teknikte pterygoid duvarın ve hamulusun posterior yönde
rezorpsiyonu sayesinde hamular derinlik arttırılır.(107)
Uygulama sırasında pterygoid duvarların fraktürü sonucu hemorajiyle
karşılaşılması bu işlemin riskleri arasındadır. Buna ek olarak iyileşme sonrası
öngörülemeyen derinlik artışı da ayrı bir risktir.(2)
- 51 -
7. YETERSİZ ALVEOLER KRETLERDE YUMUŞAK DOKU CERRAHİSİ
7.1. MODERN YUMUŞAK DOKU TEKNİKLERİ
Preimplant cerrahi tarafından da kabul edilen birçok preprostetik yumuşak
doku tekniği mevcuttur. Yumuşak doku cerrahisinin ana hedefi mobil mukoza veya
inflamatuar hiperplaziyi ortadan kaldırmak için implant çevresini geliştirmektir.
İnflamatuar hiperplazi daha önce vestibuloplasti geçirmiş hastalarda implantın
deriden yerleştirildiği durumlarda görülebilir. Bu sebepten ötürü damaktan alınan
mukozal greftler kullanılır. Mukozal greftler mukotom yardımıyla şeritler şeklinde
alınır.(5)
Buna alternatif olarak mukozal greftler bistüri yardımıyla alınıp suture
edilebilirler. Bistüri yardımıyla alınan greftler inceltilmek zorundadır. İmplantın
dışarı çıkabilmesi için greftte açıklıklar yaratılır. Alıcı ve verici sahalar iyileşmenin
bozulmaması için kaplanırlar.
Bağlayıcı doku greftleri implantın çevresindeki mukogingival defektleri
ortadan kaldırmak ve ayrıca artan yumuşak doku defektlerini geri çevirmek amacıyla
genelde damaktan alınır. Bağlayıcı doku greftleri alıcı sahanın durumuna göre
vaskülarize veya nonvaskülarize olabilir.(108) Doku greftlerinin ana hedefi implant
çevresinde
stabil
bir
yumuşak
doku
çevresi
oluşturmak
ve
implant
restorasyonlarında daha doğal bir yumuşak doku mimarisi ortaya çıkarmaktır.
PALACCI(109) implantların çevresini keratinize mukoza ile kaplamak için küçük
rotasyonel fleplerin kullanıldığı bir tekniği açıklamıştır. Bu teknik interdental
papillanın yeniden şekillendirilmesinde de kullanılabilirdi.(109)
- 52 -
Bazı durumlarda dudakta, dilde ve yanakta yumuşak doku kayıpları görülebilir.
Böyle durumlarda geleneksel preprostetik cerrahi teknikler kullanılabilir. İmplantın
çevresindeki greftte hiperplastik reaksiyon gelişme riskini azaltmak için deri grefti
kullanmak yerine mukozal greft kullanılması uygundur. STEINHAUSER tarafından
greft
kullanmadan
ağız
tabanını
mandibuladan
serbestleme
yöntemleri
belirtilmiştir.(110) Bu teknik dilin mobilitesini arttırır ve mandibula üzerindeki
hareketli mukoza elimine edildikten sonra implantın doğru yerleştirilmesini
sağlar.(111)
Mandibular bukkal vestibuler bölgesi sığ olan veya mental kasların yukarıda
bağlantı gösterdiği hastalarda KAZANJAN(112) tarafından ortaya sunulan dudak
çevirme tekniği uygulanabilir. Teknik implantların yerleştirilmesiyle beraber
kullanılabilir ve protezin kenarının geleceği derinleşen sulkusta artış sağlayabilir.
İntraoral deri tümör cerrahisini takiben preimplant cerrahisi gereken hastalarla
karşılaşılabilir. Bu hastalar genellikle deriyi, kasları ve kemiği içeren kompozit
fleplerle rekonstrükte edilirler. Yumuşak dokunun; genellikle bir sulkoplastiyi
takiben ve kemik içi implantın yerleştirilmesinden önce greft uygulanarak yeniden
hacimlendirilmesi gerekir. Bir deri greftinin periimplantitisle ilişkili olduğu
durumlarda lokal eksizyon ve mukozal greftle yerdeğiştirilmesi gerekir.(5)
Ueda M. ve arkadaşlarının yapmış olduğu araştırmaya göre kültürlenmiş
epitel hücreler kullanılarak da yumuşak doku oluşturmak mümkündür. Buna göre
işlemden 10 gün sonra normal mukoza oluşumu gözlenir.(113)
- 53 -
7.2. TRANSPOZİSYONEL FLEP VESTİBULOPLASTİ
Yeterli mandibuler yüksekliğin olduğu durumlarda bu teknik sayesinde anterior
vestibuler bölgede artış sağlanabilir. Bu teknikte lingual yönde mukozal bir flep,
labial yönde ise transpozisyonel bir flepten yararlanılır. Bu tekniğin başlıca
endikasyonu yeterli miktarda mandibuler kemik yapısının olduğu fakat vestibülde
mukozal ve kassal yapışma bölgelerinden itibaren yeterli derinliğin olmadığı daha
fazla vestibuler derinliğe ihtiyaç duyulan olgulardır.
Bu teknik hospitalizasyon, sekonder cerrahi işlem, verici bir saha, protezsiz
geçecek bir periyod gerektirmez. Vestibuler derinliğin tahmin edilemeyen relapsı,
vestibül derinlikte görülen skar, protezin vestibuler bölgedeki uyumsuzluğu bu
tekniğin dezavantajlarındandır.(2)
7.3. VESTİBÜL ve AĞIZ TABANI YÜKSELTME TEKNİKLERİ
Mandibulanın lingual bölümüne bağlanan mylohyoid ve genioglossus kasları
ağız tabanının derinliğini azaltabilir. Traumer böyle durumlarda mylohyoid kasın
mylohyoid
çıkıntıdan
daha
aşağıya
bağlanması
yoluyla
ağız
tabanının
derinleştirilmesi işlemini açıklamıştır. Daha sonra bu tekniğe ek olarak Macintosh ve
Obwegeser labial derinleştirme işleminin etkisinden de yararlanmak amacıyla bukkal
ve labial uzatmayı sağlamak için Clark tarafından gösterilen supraperiostal flep
tekniğini modifiye etmiştir.(114)
- 54 -
Bu teknik en az 15 mm mandibuler kemik mevcut olduğu durumlarda
uygulanabilir. Mevcut kemiğin konturları operasyon sonrası ortaya çıkacak alveoler
kretler için uygun olmalıdır. Büyük kemiksel düzensizliklerin bulunduğu durumlarda
greftler yardımıyla düzeltmeye gidilebilir.
Alveoler kretin greftlenmesinde deri dışında dokular da kullanılmaktadır. Sıkı,
rezilyent bir doku oluşturmada palatal dokunun potansiyel avantajlarından
yararlanılabilir.(115)
7.4. SUBMUKOZAL VESTİBULOPLASTİ
Bu teknikte orta seviyede bir insizyon yapılır daha sonra mukoza altında
kalan kısım submukozal dokudan ayrılır. Kassal ve submukozal bağlantıların
periosttan ayrılmasıyla supraperiostal bir tünel oluşturulur. Bu kassal ve submukozal
bağlantıların yerleri değiştirilebilir veya eksize edilebilir. Bu teknik vestibuler
derinlik artışı ve protez sahasındaki mukozanın bağlantısı hakkında tahmin edilebilir
sonuçlar verir.(2)
- 55 -
8.SONUÇ
Sonuç olarak dişhekimliğinde atrofik maksilla ve mandibulanın vertikal ve
horizontal yönde iyileştirilmesi amacıyla birçok teknik ve materyal mevcuttur. Bu
teknik ve materyaller her geçen gün gelişmektedir. Bunların uygulanması sırasında
veya sonrasında bazı komplikasyonların görülmesi olasıdır. Bu sebeple tedavi
şekline karar vermeden önce agmentasyonu istenilen bölgede gerekli kemik miktarı,
hastanın beklentisi, sosyoekonomik durumu, sistemik durumu, tedaviyi kabul etmesi,
hekimin beceri ve deneyimi gözden geçirilmelidir.
- 56 -
9.KAYNAKLAR
1- Bays RA: The pathophysiology and anatomy of edentulous bone loss. In
Fonseca R. Davis W, editors: Reconstructive preprosthetic oral and maxillofacial
surgery, Philadelphia, WB Saunders, 1985.
2- Ellis p, Tucker H. Contemporary Oral and Maxillofacial Surgery
3- Khoury F, Jean Nefussi R. Bone Augmentation in Oral Implantology.
Quintessence, 2007; 1-24
4- Beumer J et al: Prosthodontic and surgical aspects of treatment planning for
reconstructive surgery. In Fonseca R. Davis W. Editors: Reconstructive
preprosthetic oral and maxillofacial surgery, Philadelphia, WB Saunders, 1985
5- J. I. Cawood, P. J. W. Stoelinga, T. K. Blackburn. The evolution of preimplant
surgery from preprosthetic surgery. Int. J. Oral Maxillofac. Surg. 2007; 36:377385
6- Thiersch C. Uber die feineren anatomischen Veranderungen bei aufheilung
von Haut auf Granulationen. Arch LinChir 1874
7- Trauner R. Alveoloplasty with ridge extensions on the lingual side of the
lower jaw to solve the problem of a lower dental prosthesis. Oral Surg Oral
Med Oral Pathol 1952: 5: 340–346
8- Obwegeser H. Die Totalen Mundbodenplastik. Schweiz Mschr Zahnheilk
1963: 73: 565–571
9- Davis WH, Davis CL, eds: Reconstructive preprosthetic oral and maxillofacial
surgery. Philadelphia: W.B. Saunders Co. 1986 p. 69–116
10- Propper RH. Simplified ridge extension using free mucosal grafts. J Oral
Surg 1964: 22: 469–474
- 57 -
11- Steinhauser EW. Free transplantation of oral mucosa for improvement of
denture retention. J Oral Surg 1969: 27: 955–961
12- Hillerup S. Preprosthetic mandibular vestibuloplasty with buccal mucosal . A
2-year follow-up study. Int J Oral Surg 1982: 11: 81–88
13- Tideman H. A technique of vestibular plasty using a free mucosal graft from
the cheek. Int J Oral Surg 1972: 1: 76–80
14- de Koomen HA. A prosthetic view on vestibuloplasty with free mucosal
graft. Int J Oral Surg 1977: 6: 38–41
15- Huybers TJ, Stoelinga PJ, de Koomen HA, Tideman H. Mandibular
vestibuloplasty using a free mucosal graft. A 2–7 year evaluation. Int J Oral Surg
1985: 14: 11–15.
16- Tallgren A. The continuing reduction of the residual alveolar ridges in
complete denture wearers: a mixed-longitudinal study covering 25 years. J
Prosthet Dent 1972: 27: 120–132.
17- Obwegeser H. Surgical preparation of the maxilla for a prosthesis. J Oral
Surg Anesth Hosp Dent Serv 1964: 22: 127–134
18- Gillies HD. Plastic surgery of the face. Hodder & Stoughton 1920: p. 193–
208
19- Celesnik F. Die Tuberplastik. Oest Z Stomat 1954: 51: 584
20- Clementschisch F. In: Pichler H, Trauner R, eds: Mund- und KieferChirurgie. 1948 p. 524
21- Davis WH, Delo RI, Weiner JR, Terry B. Transoral bone graft for atrophy
of the mandible. J Oral Surg 1970: 28: 760–765
22- Terry BC, Albright JE, Baker RD. Alveolar ridge augmentation in the
edentulous maxilla with use of autogenous ribs. J Oral Surg 1974: 32: 429–434
- 58 -
23- Bell WH, Buche WA, Kennedy III JW, Ampil JP. Surgical correction of the
atrophic alveolar ridge. A preliminary report on a new concept of treatment.
Oral Surg Oral Med Oral Pathol 1977: 43: 485–498
24- Kent JN, Quinn JH, Zide MF, Finger IM, Jarcho M, Rothstein SS. Correction
of alveolar ridge deficiencies with nonresorbable hydroxylapatite. J Am Dent
Assoc 1982: 105: 993–1001
25- Vanassche BJ, Stoelinga PJ, de Koomen HA, Blijdorp PA, Schoenaers JH.
Reconstruction of the severely resorbed mandible with interposed bone grafts and
hydroxylapatite. A 2–3 year follow-up. Int J Oral Maxillofac Surg 1988: 17:
157–160
26- Cawood JI, Howell RA. Reconstructive preprosthetic surgery. I. Anatomical
considerations. Int J Oral Maxillofac Surg 1991: 20: 75–82
27- Cawood JI, Howell RA. A classification of the edentulous jaws. Int J Oral
Maxillofac Surg 1988: 17: 232–236
28- Richardson D, Cawood JI. Anterior maxillary osteoplasty to broaden the
narrow maxillary ridge. Int J Oral Maxillofac Surg 1991: 20: 342–348
29- Cawood JI, Stoelinga PJ, Brouns JJ. Reconstruction of the severely resorbed
(Class VI) maxilla. A two-step procedure. Int J Oral Maxillofac Surg 1994: 23:
219–225
30- Nystrom E, Lundgren S, Gunne J, Nilson H. Interpositional bone grafting and
Le Fort I osteotomy for reconstruction of the atrophic edentulous maxilla. A twostage technique. Int J Oral Maxillofac Surg 1997: 26: 423–427
31- Tatum Jr H. Maxillary and sinus implant reconstructions. Dent Clin North
Am 1986: 30: 207–229
- 59 -
32- Cawood JI, Stoelinga PJ. International academy for oral and facial
rehabilitation-Consensus Report. Int J Oral Maxillofac Surg 2006: 35: 195–198
33- Longman L. A survey of alveolar ridge morphology in the edentulous patient.
Proceedings of the European Prosthodontic Association 17th Annual Meeting.
1993: 43
34- Boyne P J. Osseous Reconstruction of the Maxilla and the Mand.
35- Friedenstein AJ. Determined and inducible osteogenic precursor cells. In:
Sognnaes RF (ed). Proceedings of the CIBA Foundation Syposium No.11 on
Hard Tissue Growth, Repair, and Remineralization. Amsterdam: Elsevier
Excerpta Medica-North Holland, 1973:169-182
36- Boyne PJ. Induction of bone repair of various bone graft materials. In:
Sognnaes RF (ed). Proceedings of the CIBA Foundation Syposium No. 11 on
Hard Tissue Growth, Repair, and Remineralization. Amsterdam: Elsevier
Excerpta Medica-North Holland, 1973:121-141
37- Bernstein S, Cooke J, Fotek P, Wang HL. Vertical bone augmentation:
Where are we now? Implan Dentistry . 2006 15: 219
38- Trisi P, Rebaudi A, Calvari F, Lazzara RJ. Sinus graft with biogran,
autogenous bone, and PRP: a report of three cases with histology and micro-CT.
Int. J. Periodontics Restorative Dent. 2006 Apr;26(2):113-25
39- Whitesides, Lee M., Radwan, Alaaaldin, Sharawy, Mohamed. Sinus Floor
Augmentation Using a Composite Graft of Bone Morphogenic Protein-2 and
Allogenic Cancellous Bone (Puros): Case Report. Journal of Oral Implantology.
2006;32(5):259-264
- 60 -
40- Spagnoli DB, Mazzonetto R, Marchena JM. Clinical procedures currently
using bone grafting with guided tissue regeneration techniques. Clin Oral
Maxillofac Surg. 2001;13:423-436
41- Keith JD. Clinical and Histological Analysis of Puros Cancellous Chip
Allografts in Humans. Part 1: Clinical Use of Puros Cancellous Chip Allograft
and Treatment of Human Periodontal Defects. Carlsbad, Calif: Zimmer Inc; 2004
42- Minichetti JC, D’Amore JC, Hong AY, et al. Human histologic analysis of
mineralized bone allograft (Puros) placement before implant surgery. J Oral
Implantol. 2004;3:74-82
43- Burkus JK, Heimse SE, Gornet MF, Zdeblick PA. Is INFUSE bone graft
superior to autograft graft bone? An integrated analysis of clinical trials using the
LT-CAGE, lumbar tapered fusion device. J Spinal Disord Tech. 2003;16:113-122
44- Schwartz Z, Somers A, Mellonig JT, et al. Addition of human recombinant
bone morphogenetic protein-2 to inactive commercial human demineralized freze
dried bone allograph makes an effective composite bone inducted implant
material. J Periodontol. 1998;69:1337-1345
45- Boyne PJ, Shabahang S. An evaluation of bone induction delivering materials
in conjunction with root-form implant placement. Int J Periodontics Restorative
Dent. 2001;21:333-343
46- Cochran DL, Jones AA, Lily LC. Fiorellini JP, Howell H. Evaluation of
recombinant human bone morphogenetic protein-2 in oral applications including
the use of endosseous implants: 3-year results of a pilot study in humans. J
Periodontol. 2000;71:1241-1257
- 61 -
47- Yukna RA. Clinical evaluation of coralline calcium carbonate as bone
replacement graft material in human periodontal osseous defects. J Periodontol.
1994;65:177-185
48- Yukna RA, Yukna CN. A 5-year follow-up of 16 patients treated with
coralline calcium carbonate (Biocoral) bone replacement grafts in intrabony
defects. J Clin Periodontol. 1998;25:1036-1040
49- Scarano A, Degidi M, Iezzi G et al. Implant Dentistry. 2006 Jun 15(2) 197207
50- Piattelli A, Scarano A, Piattelli M, et al. Bone regeneration using Bioglass:
An experimental study in rabbit tibia. J Oral Implantol. 2000;26:257-261
51- Nasr HF, Aichelmann-Reidy ME, Yukna RA. Bone and bone substitutes.
Periodontol 2000. 1999;19:74-86
52- Leenslag JW, Pennings AJ, Bos RRM, et al. Resorbable materials of poly(LLactide). VI. Plates and screws for internal fracture fixation. Biomaterials.
1987;8:70-73
53- Piattelli A, Scarano A, Russo P, et al. Evaluation of guided bone regeneration
in rabbit tibia using bioresorbable and non-resorbable membranes. Biomaterials.
1996;17:791-796
54- Antoun H, Chemaly C, Missika P. Bone Augmentation in Oral Implantology.
Quintessence, 2007 347-348
55- Bhatnagar RS, Qian JJ, Gough CA. The role in cell binding of a beta-bend
within the triple helical region in collagen alpha1 (I) chain: Structural and
biological evidence for conformational tautomerism on fiber surface. J Biomol
Struct Dyn. 1997;14:547-560
- 62 -
56- Qian JJ, Bhatnagar RS. Enhanced cell attachment to anorganic bone mineral
in the presence of a synthetic peptide related to collagen. J Biomed Mater Res.
1996;31:545-554
57- Bhatnagar RS, Qian JJ, Wedrychowska A, et al. Design of biomimetic habitat
for tissue engineering with P-15, a synthetic peptide analogue of collagen. Tissue
Eng. 1999;5:53-65
58- Yukna RA, Callan DP, Krauser JT, et al. Multi-center clinical evaluation of
combination anorganic bovine-derived hydroxyapatite matrix (ABM)/cell
binding peptide (P-15) as a bone replacement graft material in human periodontal
osseous defects. 6-month results. J Periodontol. 1998;69:655-663
59- Guarnieri R, Bovi M. Maxillary sinus augmentation using prehardened
calcium sulfate: A case report. Int J Periodontics Restorative Dent. 2002;22:503508
60- Maragos P, Bissada NF, Wang R, et al. Comparison of three methods using
calcium sulfate as a graft barrier material for the treatment of Class II mandibular
molar furcation defects. Int J Periodontics Restorative Dent. 2002;22:493-501
61- Ricci JL, Alexander H, Nadkarni P, et al. Biological mechanisms of calcium
ed. Bone Engineering. Toronto, Canada: Em Squared Inc; 2000:332-344
62- Andreana S, Cornelini R, Edsberg E et al. Implant Dentistry. 2004; 13(3)
270-277
63- Beeson W. Plaster of Paris as an alloplastic implant in the frontal sinus. Arch
Otolaryngol. 1981;107:664-669
64- Pecora G, Andreana S, Covani U, et al. Bone regeneration with calcium
sulfate barrier. Oral Surg Oral Med Oral Pathol. 1997;84:424-429
- 63 -
65- Berglundh T, Lindhe J. Healing around implants placed in bone defects
treated with Bio-Oss. Clin Oral Implants Res. 1997;8:117-124
66- Piattelli M, Favero GF, Scarano A, et al. Bone reactions to anorganic bovine
bone (Bio-Oss) used in sinus lifting procedure: A histologic long-term report of
20 cases in man. Int J Oral Maxillofac Implants. 1999;14:835-840
67- Hallman M, Lederlund A, Linsskog S, et al. A clinical histologic study of
bovine hydroxyapatite in combination with autogenous bone and fibrin glue for
maxillary sinus floor augmentation. Results after 8 months of healing. Clin Oral
Implants Res. 2001;12:135-143
68- Nanci A, Zalzal S, Fortin M, et al. Incorporation of circulating bone matrix
proteins by implanted hydroxyapatite and at bone surfaces: Implications for
cement line formation and structuring of biomaterials. In: Davies JE, ed.
Proceedings of the International Workshop on Bone Engineering. Toronto,
Canada: Em Squared Inc.;2000:305-311
69- Chu CC. Hydroltic degradation of polyglycolic acid: Tensile strength and
crystallinity study. J Appl Polym Sci. 1981;26:1727-1734
70- Buser D, Bragger U, Lang NP, Nyman S. Regeneration and enlargement of
jaw bone using guided tissue regeneration. Clin Oral Implants Res 1990: 1: 22–
32
71- Feinberg SE, Fonseca RJ. In: Fonseca RJ, Davis WH, eds: Reconstructive
preprosthetic oral and maxillofacial surgery 2nd ed. Philadelphia: W.B. Saunders
Co 1995: 62–64
72- Keller EE. Reconstruction of the severely atrophic edentulous mandible with
endosseous implants: a 10-year longitudinal study. J Oral Maxillofac Surg 1995:
53: 305–320
- 64 -
73- Keller EE, Van Roekel NB, Desjardins RP, Tolman DE. Prosthetic-surgical
reconstruction of the severely resorbed maxilla with iliac bone grafting and
tissue-integrated prostheses. Int J Oral Maxillofac Implants 1987: 2:155–165
74- Fazili M, Overvest-Eerdmans GR, Vernooy AM, Visser WJ, van Waas MA.
Follow-up investigation of reconstruction of the alveolar process in the atrophic
mandible. Int J Oral Surg 1978:7: 400–404
75- Nkenke E, Schultze-Mosgau S, Radespiel-Troger M, Kloss F, Neukam FW.
Morbidity of harvesting of chin grafts: a prospective study. Clin Oral Implants
Res 2001: 12: 495–502
76- Misch CM. Comparison of intraoral donor sites for onlay grafting prior to
implant placement. Int J Oral Maxillofac Implants 1997: 12: 767–776
77- Vincente J, Stoelinga PJW. Toepassing van bottransplantaten uit het corpus
mandibulae voor preimplantologische chirurgie. Ned Tijdschr Tandheelkd 2005:
112: 211–215
78- Bloomquist DS, Feldman GR. The posterior ilium as a donor site for maxillofacial bone grafting. J Maxillofac Surg 1980: 8: 60–64
79- Nkenke E, Weisbach V, Winckler E, Kessler P, Schultze-Mosgau S,
Wiltfang J, Neukam FW. Morbidity of harvesting of bone grafts from the
iliac crest for preprosthetic augmentation procedures: a prospective study. Int
J Oral Maxillofac Surg 2004: 33: 157–163
80- Hayter JP, Cawood JI. Oral rehabilitation with endosteal implants and free
flaps. Int J Oral Maxillofac Surg 1996:25: 3–12
81- Leake DL. A new alloplastic tray for osseous contour defects. J Maxillofac
Surg 1974: 2: 146–149
82- Boyne PJ, Lilly LC, Marx RE, Moy PK, Nevins M, Spagnoli DB, Triplett
- 65 -
RG. De novo bone induction by recombinant human bone morphogenetic
protein-2 (rhBMP-2) in maxillary sinus floor augmentation. J Oral Maxillofac
Surg 2005: 63: 1693–1707
83- Terry BC, Albright JE, Baker RD: Alveolar ridge augmentation in the
edentulous maxilla with use of autogenous ribs, J Oral Surg 1974;32:429
84- Enislidis G, Fock N, Klug C et al. Analysis of complications following
alveoler distraction osteogenezis and implant placement in the partially
edentulous mandible. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. Oral Endod.
2005;100-25
85- Reinert S, Konig S, Bremerich A et al. Stability of bone grafting and
placement of implants in the severely atrophic maxilla. Br J Oral Maxillofac.
Surg. 2003; 41:249
86- Devorah S, Levin L, Sigal L. Surgical Success of Intraoral Autogenous Block
Onlay Bone Grafting for Alveolar Ridge Augmentation. Implant Dentistry
2005;14;2:131-138
87- Khoury F. Bone Augmentation in Oral Implantology. Quintessence, 2007;
176-183
88- I. Woo, B. T. Le. Maxillary Sinus Flor Elevation: Review of Anatomy and
Two Techniques. Implant Dentistry 2004; 13(1) 28-30
89- Tatum OH. Maxillary and sinus implant reconstruction. Dent Clin North Am.
1986;30:207-229
90- Cordioli G, Mazzocco C. Maxillary sinus floor augmentation using bioactive
glass granules and autogenous bone with simultaneous implant placement.
Clinical and histological findings. Clinical Oral Implants Research. 2001 ;
12:270-278
- 66 -
91- Van den Bergh JPA, ten Bruggen-kate CM. Anatomical aspects of sinus floor
elevations. Clinical Oral Implants Resources. 2000;11:256-265
92- Chanavaz M. Maxillary sinus: anatomy, physiology, surgery and bone
grafting related to implantology. Eleven years of surgical experience (19791990). Journal of Oral Implantology. 1990;16:199-209
93- Solar P, Geyerhofer U. Blood supply to the maxillary sinus relevant to sinus
floor elevation procedures. Clinical Oral Implants Research. 1999;10:34-44
94- Summers RB. A new concept in maxillary implant surgery: the osteotome
technique. Compend Contin Educ Dent. 1994;15:152-162
95- Block MS, Kent JN. Sinus augmentation for dental implants: the use of
autogenous bone. J Oral Maxillofac Surg. 1997;55:1281-1286
96- Smiler DG, Holmes RE. Sinus lift procedure using porous hydroxyapatite: a
preliminary clinical report. Journal of Oral Implantology. 1987;13:239-253
97- Summers RB. Sinus floor elevation with osteotomes. Journal of Esthetic
Dentistry. 1998;10:164-171
98- Stuart J. Froum, Stephen S. Wallace, Sang Choon Cho. Sinus Flor Elevation
Using Anorganic Bovine Bone Matrix (OsteoGraf/N) with and without
Autogenous Bone: A Clinical Histologic, Radiographic, and Histomorphometric
Analysis- Part 2 of an Ongoing Prospective Study
99- Papa F, Cortese A, Maltarello M. C. Et al. British Journal of Oral and
Maxillofacial Surgery. 2005; 43, 309-313
100- Samchukov M, Cope J, Cherkashin A. Craniofacial Distraction
Osteogenezis
101- Karp NS, Thorne CHM, McCarthy JG, Sisson HA:Bone lengthening in the
craniofacial skeleton. Ann Plast Surg 1990;24:231
- 67 -
102- Ilızarov GA. The tension-stress effect on the genesis and growth of tissues:
part I: the influence of stability of fixation and soft-tissue preservation. Clin
Orthop 1989;238:249
103- Chin M. Alveolar distraction: endosseous, self-retaining devices. In Diner
PA, Vasquez MP, editors:2nd International Congress on Cranial and Facial Bone
Distraction Processes, Paris, France, Bologna, Italy, Monduzzi Editore 1999
104- Kent JN, Jarcho M. Reconstruction of the alveolar ridge with
hydroxyapatite. In Fonseca R Davis W. Editors: Reconstructive preprosthetic oral
and maxillofacial surgery. Philadelphia. WB Saunders 1985
105- Nyman S et al. New attachment following surgical treatment of human
periodontal disease. J Clin Periodont 1982;9:290
106- Buser D et al. Localized ridge augmentation using guided bone
regeneration. I. Surgical procedure in the maxilla. Int J Periodont Restor Dent
1993;13:29
107- Obwegeser HL. Surgical preparation of the maxilla for prosthesis. J Oral
Surg 1964;22:127
108- Langer B, Calagna LJ. The subepithelial connective tissue graft. A new
approach to the enhancement of anterior cosmetics. Int J Periodontics Restorative
Dent 1982: 2: 22–33
109- Palacci P. Ame´nagement des tissus pe´ri-implantaires:inte´reˆt de la
re´ge´ne´ration des papilles. Real Clin 1992: 3:381–387
110- Steinhauser EW. A method of detaching the tongue following tumor
resection. Dtsch Zahnarztl Z 1987: 42: 707–711
111- Kwakman JM, Voorsmit RA, Freihofer HP. Improvement in oral function
following tumour surgery by a combination of tongue plasty by the Steinhauser
- 68 -
technique and osseointegrated implants. J Craniomaxillofac Surg 1997: 25: 15-18
112- Kazanjian VH. Surgical operations as related to satisfactory dentures. Dent
Cosmos 1924: 66: 387–395.
113- Hata K, Kagami H, Ueda M et al. The chracteristics of cultured mucosal cell
sheet as a material for grafting; comparison with cultured epidermal cell
sheet.Ann Plast Surg. 1995 34: 530-538
114- MacIntosh RB. Obwegeser HL. Preprosthetic surgery: a scheme for its
effective employment. J Oral Surg 1967;25:397
115- Mercier P, Lafontant R. Residual alveolar ridge atrophy: classification and
influence of facial morphology. J Prosthet Dent 1979;41:90
116- Suba Z, Takacs d, Matusovitz D et al. Clinical Oral Implants Research.
2006 Feb. 17(1) 102-108
117- Ueda M, Sumi Y, Mizuno H et al. Tissue engineering: applications for
maxillofacial surgery. Materials Science and Engineering 2000 C 13; 7-14
118- Malden N. J. Implant Dentistry. 2005 Jun 14(2) 154-156
- 69 -
10.ÖZGEÇMİŞ
12 Ekim 1985 yılında İzmir’de doğdum. Eğitimime 1996 yılında Emlak
Bankası İlkokulunda başladım,1996-2003 yılları arasında Karşıyaka Anadolu
Lisesinde okudum.2003 yılında Karşıyaka Anadolu Lisesinden mezun oldum. 2003
yılında Ege Üniversitesi Dişhekimliği Fakültesine kayıt oldum.
- 70 -