FAZ DİYAGRAMLARI
Malzeme özellikleri görmüş oldukları termomekanik işlemlerin sonucunda oluşan
içyapılarına bağlıdır. Faz diyagramları mühendislerin içyapı değişikliği için
uygulayacakları ısıl işlemin tasarımı ve kontrolüne yardımcı olduğundan önemlidir.
Ayrıca alaşımlara ait ergitme, döküm, kristalleşme gibi olaylarla ilgili değerli bilgiler
içerirler.
TEMEL KAVRAMLAR: Bileşen bir alaşımı oluşturan saf metal ve/veya bileşikleri ifade
eder. Örneğin, pirinç alaşımında bileşenler bakır (Cu) ve çinko (Zn)’dir.
Bileşenlerden biri çözen diğeri çözünen olarak da ifade edilebilir. Katı çözeltide
çözünen atomların çözen kafes içinde erişebileceği üst konsantrasyon (doyma)
değeri sıcaklığa bağlı olup buna çözünürlük sınırı denir.
Faz, bir sistemin (malzemenin sahip olduğu özel durum veya kimyasal bileşimden
bağımsız olarak aynı alaşım elementleri tarafından oluşturulan olası alaşımlar,
örneğin Fe-C sistemi) homojen fiziksel ve kimyasal özellikler gösteren parçasıdır. Saf
malzemeler ve katı/sıvı/gaz çözeltiler birer fazdır. Örneğin, çözünürlük sınırı aşılmış
bir şeker-su çözeltisinde şerbet bir faz, katı şeker ise diğer bir faz olarak düşünülür.
bir sistemde iki farklı faz bulunuyorsa, fazlar arasında fiziksel veya kimyasal
özelliklerin ani olarak değiştiği faz sınırları bulunur. Örneğin, buzlu su kimyasal
özellikleri aynı fiziksel özellikleri farklı iki fazlı bir sistemdir.
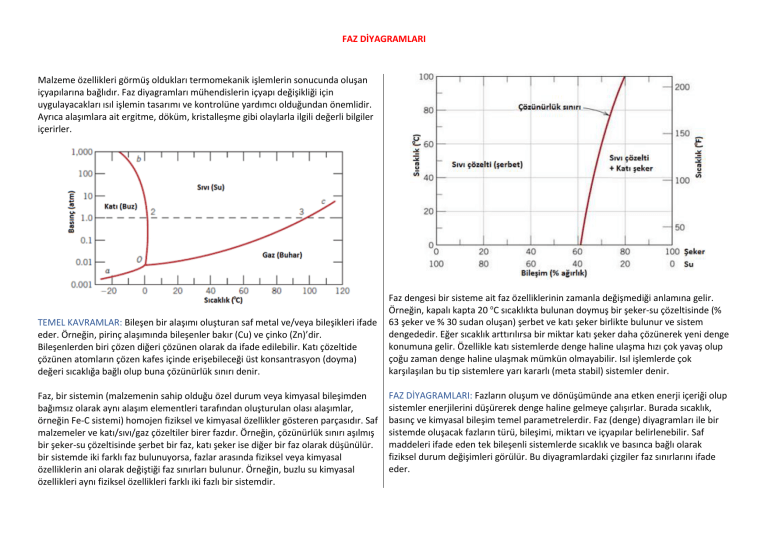
Faz dengesi bir sisteme ait faz özelliklerinin zamanla değişmediği anlamına gelir.
Örneğin, kapalı kapta 20 oC sıcaklıkta bulunan doymuş bir şeker-su çözeltisinde (%
63 şeker ve % 30 sudan oluşan) şerbet ve katı şeker birlikte bulunur ve sistem
dengededir. Eğer sıcaklık arttırılırsa bir miktar katı şeker daha çözünerek yeni denge
konumuna gelir. Özellikle katı sistemlerde denge haline ulaşma hızı çok yavaş olup
çoğu zaman denge haline ulaşmak mümkün olmayabilir. Isıl işlemlerde çok
karşılaşılan bu tip sistemlere yarı kararlı (meta stabil) sistemler denir.
FAZ DİYAGRAMLARI: Fazların oluşum ve dönüşümünde ana etken enerji içeriği olup
sistemler enerjilerini düşürerek denge haline gelmeye çalışırlar. Burada sıcaklık,
basınç ve kimyasal bileşim temel parametrelerdir. Faz (denge) diyagramları ile bir
sistemde oluşacak fazların türü, bileşimi, miktarı ve içyapılar belirlenebilir. Saf
maddeleri ifade eden tek bileşenli sistemlerde sıcaklık ve basınca bağlı olarak
fiziksel durum değişimleri görülür. Bu diyagramlardaki çizgiler faz sınırlarını ifade
eder.
Bu diyagramda B noktasına ait eş sıcaklık doğrusunun likidüs çizgisini kestiği
noktanın yatay izdüşümü ( Cs ) sıvı fazdaki Ni konsantrasyonunu, solidüs çizgisini
kestiği noktanın yatay izdüşümü ( C ) katı fazdaki Ni konsantrasyonunu ve B
İkili faz diyagramları alaşımların bulundukları sıcaklıkta ve sahip oldukları kimyasal
bileşimde içyapılarında denge halinde bulunan fazlar, bu fazların mikroyapıya
dağılım oranı ve fazların kimyasal bileşimleri hakkında bilgiler içeren haritalardır.
İKİLİ İZOMORFİK SİSTEMLER: Birbiri içinde tam çözünürlüğe sahip elementlerin
oluşturduğu ikili izomorfik sistemlere ait 1 atm sabit basınçta scaklık ve kimyasal
bileşim değişkenlerine sahip diyagramlar yaygın olup, anlaşılması ve yorumlanması
kolaydır. Her ikisi de YMK kristal yapılı, atom yarıçapları ve elektronegatiflikleri
yakın ve valans özellikleri benzer olduğundan birbirleri içinde tamamen çözünebilen
bakır (Cu) ve nikel (Ni) bu tip diyagramlara iyi bir örnektir. Saf bakırın ergime
sıcaklığı 1085 oC, saf nikelin ergime sıcaklığı ise 1455 oC’dir. Diyagramda % 45 nikel,
% 55 bakır içeren 1270 oC’deki alaşım B noktasıyla gösterilmiş olup katı ve sıvı fazlar
dengededir. Bu noktadan çizilen yatay eş sıcaklık doğrusunun likidüs çizgisini kestiği
noktanın yataydaki izdüşümü (% 37) sıvı fazdaki Ni konsantrasyonunu, solidüs
çizgisini kestiği noktanın yataydaki izdüşümü ise (% 50) katı fazdaki Ni
konsantrasyonunu verir. Diyagramda % 45 nikel, % 55 bakır içeren 1050 oC’deki
alaşım ise sadece katı faz içerir.
noktasının yatay izdüşümü ( Co ) ise toplam Ni konsantrasyonunu verir. Buna göre
sıvı fazın ağırlık oranı;
WS
C Co
S
R S C CS
şeklinde, katı ( ) fazın ağırlık oranı ise;
W
C CS
R
o
R S C CS
şeklinde hesaplanır.
ve fazlarından oluşan bir sistemde fazların hacimsel oranları ( V V 1
olmak üzere) ise sırasıyla;
W
W
V
W
W
ve V
W
W
şeklinde hesaplanır. Benzer şekilde ağırlık oranları da sırasıyla;
W
V *
V *
ve W
V * V *
V * V *
şeklinde hesaplanır.
İzomorfik Cu-Ni alaşımının 1300 oC sıcaklıktan dengeli yani çok yavaş soğutulması
durumunda a noktası tamamen sıvı fazda ağırlıkça % 35 Ni ve % 65 Cu içeren
bileşime sahiptir ve likidüs çizgisine yani b noktasına kadar yapı ve bileşim
değişmez.
Yaklaşık 1260 oC’deki b noktasında ağırlıkça % 46 Ni ve % 54 Cu içeren ilk katı faz
oluşmaya başlar ancak sıvı fazda bileşim yaklaşık % 35 Ni ve % 65 Cu oranını korur.
Devam eden soğumayla birlikte her bir fazın oranı ve bileşimi değişmeye başlar.
1250 oC’deki c noktasında sıvı faz ağırlıkça % 32 Ni ve % 68 Cu içermekte, katı faz ise
ağırlıkça % 43 Ni ve % 57 Cu içermektedir.
Yaklaşık 1220 oC’de katılaşma tamamlanırken son sıvı faz ağırlıkça % 24 Ni ve % 76
Cu bileşimindedir. e noktasında ise tamamen katı faz bulunduğundan bu faz doğal
olarak % 35 Ni ve % 65 Cu içermektedir.
Birbirini sınırlı oranda çözen bileşenlerden oluşan sistemlerin belirli bir bileşimdeki
alaşımları sabit sıcaklıkta katılaşırken ötektik reaksiyon sonucu sıvı faz aynı anda iki
ayrı kata faza dönüşür. Bu duruma ilk örnek bileşenlerinin diğer atomu kendi
kafesine almadığı tam çözünmezlik için verilebilir.
TAM ÇÖZÜNMEZ ÖTEKTİK SİSTEMLER: Düşük sıcaklıklarda iki faz içyapıda ayrı ayrı
bulunur. Diyagrama adını veren ötektik nokta, soğuma sırasında sıvı fazın sabit
sıcaklıkta iki katı faza dönüştüğü noktadır.
SINIRLI ÇÖZÜNÜR ÖTEKTİK SİSTEMLER: Alaşımlarda en yaygın görülen durum sınırlı
çözünürlüktür. Her iki bileşen belirli oranlarda diğer bileşen atomlarını kafesi içinde
çözebilir.
Şekilde bakır (Cu) ile gümüş (Ag) alaşımının ötektik faz diyagramı görülmektedir.
Burada fazı Cu atomunca zengin olup içinde bir miktar Ag atomu bulunmaktadır.
fazı ise Ag atomunca zengin olup içinde bir miktar Cu atomu bulunmaktadır.
A ve B bileşenlerinden oluşan sistemde A ve B birbiri içinde çözünmediğinden
katılaşma her iki bileşen için ayrı ayrı gerçekleşmekte ve fazlar ayrı ayrı
oluşmaktadır. Katılaşmanın tamamlandığı sıcaklık ötektik sıcaklık ve bu bileşim de
ötektik bileşim olarak adlandırılır. Ötektik yapılar ince taneli olup fazlar yan yana
istiflenir ve mekanik özellikleri iyidir.
ÖTEKTOİD SİSTEMLER: Ötektik sistemlere benzer olmakla birlikte ötektoid sıcaklıkta
bir katı çözelti iki ayrı faza ayrışır.
PERİTEKTİK SİSTEMLER: Sabit bir sıcaklıkta biri sıvı olan iki faz reaksiyona girerek
yeni bir katı faz oluşturur.
PERİTEKTOİD SİSTEMLER: Sabit bir sıcaklıkta iki katı faz reaksiyona girerek yeni bir
katı faz oluşturur.
GIBBS FAZ KANUNU: Faz diyagramlarının oluşturulmasında kullanılan esaslar ve
fazların denge durumuna ait prensipler termodinamik kanunlarına dayanır. Gibbs
faz kuralı sistemde dengede bulunan fazların sayısını belirlemekte kullanılır ve
basitçe;
PF CN
şeklinde ifade edilir. Burada; P , sistemde bulunan faz sayısını; F , sistemin
serbestlik derecesini yani dışarıdan kontrol edilebilen değişken sayısını (basınç,
sıcaklık, kimyasal bileşim); C , bileşen sayısını ve N ise kimyasal bileşim dışında
kalan değişkenlerin sayısını ifade eder. İkili izomorfik Cu-Ni sistemi örnek verilecek
olursa, sabit 1 atm basınç söz konusu olduğu için kimyasal bileşim dışında kalan tek
değişken sıcaklık olduğundan P F C 1 , sistem iki bileşenden oluştuğundan
P F 2 1 3 , yani F 3 P yazılabilir. Buna göre tek fazlı bölgelerde
alaşımın özelliklerini tanımlayabilmek için 2 (sıcaklık ve kimyasal bileşim), iki fazlı
bölgelerde ise 1 (sıcaklık veya kimyasal bileşim) parametrenin bilinmesi gerekir.
DEMİR KARBON SİSTEMİ: Demir karbon alaşımı olan dökme demir ve çelikler en
yaygın kullanılan mühendislik malzemeleri olması nedeniyle Fe-C faz diyagramı
önem arz etmektedir. Saf demir ısıtıldığında ergimeden önce iki kez kristal yapı
değişikliğine uğrar. Oda sıcaklığında HMK yapılı demiri (ferrit) iken, 912 oC
üzerine çıkıldığında YMK yapılı demirine (ostenit) dönüşür. 1394 oC üzerine
çıkıldığında ise HMK yapılı demirine (ferrit) dönüşerek 1538 oC üzerinde sıvı faza
dönüşür. Bu durum daha önce bahsedildiği üzere allotropi olarak bilinir.
Fe-C faz diyagramı yatay ekseninde karbon oranı (% 100 sementite karşılık gelecek
şekilde) maksimum % 6,67 olarak belirtilir. Yaklaşık % 2’nin altında karbon içeren
sistemler çelik, % 2’nin üzerinde karbon içeren sistemler ise dökme demir olarak
adlandırılır. Çeliklerin içyapısında bulunan karbon uygulamadaki soğuma hızlarında
demir karbür (sementit: Fe3C ) fazında bulunduğundan faz diyagramına demirsementit ( Fe - Fe3C ) diyagramı da denir.
Karbon, demir içinde bir arayer elementi olup -ferrit, -ferrit ve -ostenit
fazlarıyla katı çözeltiler oluşturur. HMK yapılı -ferrit içinde karbonun çözünürlüğü
oldukça düşük olup 727 oC’de en fazla % 0,022 C çözünür. Ostenit fazının en fazla C
çözünürlüğü ise 1147 oC’de % 2,14 oranındadır. Bu büyük çözünürlük farkının ana
nedeni YMK kafesin HMK kafese göre daha büyük boyutlu olmasıdır. -ferrit
sadece çok yüksek sıcaklıklarda denge konumunda bulunduğundan teknik açıdan
fazla önem arz etmez. Sementit fazı çok sert ve gevrek olduğundan çeliklerin
dayanımını artıran temel unsurdur. Dökme demirler uygulamada % 2,14 ile % 4,5
arasında C içerirler.
% 0,022 ile % 0,76 arasında C içeren ve ötektoid noktanın solunda bulunan çelikler
ötektoid altı, % 0,76 ile % 2,14 arasında C içeren ve ötektoid noktanın sağında
bulunan çelikler ötektoid üstü olarak adlandırılır.
SORU: Ağırlıkça % 40 kalay (Sn) ve % 60 kurşun (Pb) içeren bir lehim alaşımının 150
o
C’de hangi fazları içerdiğini belirleyerek fazların bileşimlerini ile kütlesel ve
hacimsel oranlarını hesaplayınız. 150 oC’de kurşunun yoğunluğu 11,23 gr/cm3,
kalayın yoğunluğu 7,24 11,23 gr/cm3 olarak verilmiştir.
Fazların hacimsel oranlarını belirlemek için öncelikle fazların yoğunluklarının
belirlenmesi gerekir.
100
100
10,59 gr / cm3
CSn ( ) CPb ( )
11
89
7, 24 11, 23
Sn
Pb
100
100
7, 29 gr / cm3
CSn ( ) CPb ( )
98
2
7, 24 11, 23
Sn
Pb
Buna göre fazların hacimsel oranları;
W
0, 67
10,59
V
0,58
0, 67 0,33
W W
10,59 7, 29
W
0,33
7, 29
V
0, 42
0, 67 0,33
W W
10,59 7, 29
Şekle göre B noktasında ve fazları bulunmaktadır. Bağ çizgisinin yatay
eksendeki izdüşümlerine göre fazının bileşimi % 11 Sn ve % 89 Pb, fazının
bileşimi ise % 98 Sn ve % 2 Pb şeklindedir.
Fazların kütlesel oranları;
W
C C1
C C
C C 40 11
98 40
0,33
0, 67 ; W 1
C C 98 11
98 11