4.2.13
SUT maddesi
1
1
Genel
1
1
4.2.13.B
4.2.13.A - Kronik Hepatit B tedavisi
4.2.13.f.2
1.a
Tedaviye
başlama
koşulları
5.a
123456-
5.b
5.a
6.a
6.a
6.b
6.a
Oral
antiviral
kullanım
koşulları
7-
6.a
6.c
6.ç
3
2
İnterferon
kullanım
koşulları
8-
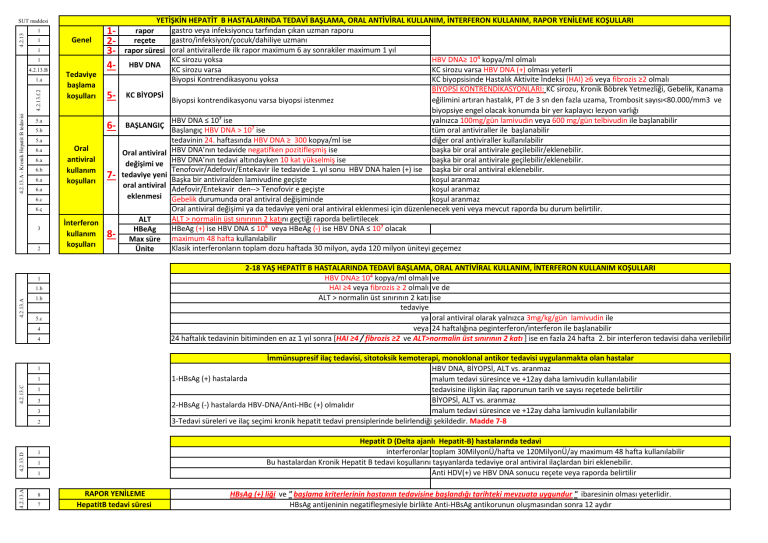
YETİŞKİN HEPATİT B HASTALARINDA TEDAVİ BAŞLAMA, ORAL ANTİVİRAL KULLANIM, İNTERFERON KULLANIM, RAPOR YENİLEME KOŞULLARI
gastro veya infeksiyoncu tarfından çıkan uzman raporu
rapor
gastro/infeksiyon/çocuk/dahiliye uzmanı
reçete
rapor süresi oral antivirallerde ilk rapor maximum 6 ay sonrakiler maximum 1 yıl
KC sirozu yoksa
HBV DNA≥ 10⁴ kopya/ml olmalı
HBV DNA
KC sirozu varsa
KC sirozu varsa HBV DNA (+) olması yeterli
Biyopsi Kontrendikasyonu yoksa
KC biyopsisinde Hastalık Aktivite İndeksi (HAI) ≥6 veya fibrozis ≥2 olmalı
BİYOPSİ KONTRENDİKASYONLARI: KC sirozu, Kronik Böbrek Yetmezliği, Gebelik, Kanama
KC BİYOPSİ
eğilimini artıran hastalık, PT de 3 sn den fazla uzama, Trombosit sayısı<80.000/mm3 ve
Biyopsi kontrendikasyonu varsa biyopsi istenmez
biyopsiye engel olacak konumda bir yer kaplayıcı lezyon varlığı
HBV DNA ≤ 10⁷ ise
yalnızca 100mg/gün lamivudin veya 600 mg/gün telbivudin ile başlanabilir
BAŞLANGIÇ
Başlangıç HBV DNA > 10⁷ ise
tüm oral antiviraller ile başlanabilir
tedavinin 24. haftasında HBV DNA ≥ 300 kopya/ml ise
diğer oral antiviraller kullanılabilir
başka bir oral antivirale geçilebilir/eklenebilir.
Oral antiviral HBV DNA’nın tedavide negatifken pozitifleşmiş ise
HBV
DNA’nın
tedavi
altındayken
10
kat
yükselmiş
ise
başka bir oral antivirale geçilebilir/eklenebilir.
değişimi ve
Tenofovir/Adefovir/Entekavir ile tedavide 1. yıl sonu HBV DNA halen (+) ise başka bir oral antiviral eklenebilir.
tedaviye yeni
Başka bir antiviralden lamivudine geçişte
koşul aranmaz
oral antiviral Adefovir/Entekavir den--> Tenofovir e geçişte
koşul aranmaz
eklenmesi Gebelik durumunda oral antiviral değişiminde
koşul aranmaz
Oral antiviral değişimi ya da tedaviye yeni oral antiviral eklenmesi için düzenlenecek yeni veya mevcut raporda bu durum belirtilir.
ALT > normalin üst sınırının 2 katını geçtiği raporda belirtilecek
ALT
HBeAg (+) ise HBV DNA ≤ 10⁹ veya HBeAg (-) ise HBV DNA ≤ 10⁷ olacak
HBeAg
Max süre maximum 48 hafta kullanılabilir
Klasik interferonların toplam dozu haftada 30 milyon, ayda 120 milyon üniteyi geçemez
Ünite
2-18 YAŞ HEPATİT B HASTALARINDA TEDAVİ BAŞLAMA, ORAL ANTİVİRAL KULLANIM, İNTERFERON KULLANIM KOŞULLARI
HBV DNA≥ 10⁴ kopya/ml olmalı ve
HAI ≥4 veya fibrozis ≥ 2 olmalı ve de
ALT > normalin üst sınırının 2 katı ise
tedaviye
ya oral antiviral olarak yalnızca 3mg/kg/gün lamivudin ile
veya 24 haftalığına peginterferon/interferon ile başlanabilir
24 haftalık tedavinin bitiminden en az 1 yıl sonra [HAI ≥4 / fibrozis ≥2 ve ALT>normalin üst sınırının 2 katı ] ise en fazla 24 hafta 2. bir interferon tedavisi daha verilebilir
1
4.2.13.A
1.b
1.b
5.c
4
4
İmmünsupresif ilaç tedavisi, sitotoksik kemoterapi, monoklonal antikor tedavisi uygulanmakta olan hastalar
HBV DNA, BİYOPSİ, ALT vs. aranmaz
1-HBsAg (+) hastalarda
malum tedavi süresince ve +12ay daha lamivudin kullanılabilir
tedavisine ilişkin ilaç raporunun tarih ve sayısı reçetede belirtilir
BİYOPSİ, ALT vs. aranmaz
2-HBsAg (-) hastalarda HBV-DNA/Anti-HBc (+) olmalıdır
malum tedavi süresince ve +12ay daha lamivudin kullanılabilir
3-Tedavi süreleri ve ilaç seçimi kronik hepatit tedavi prensiplerinde belirlendiği şekildedir. Madde 7-8
1
4.2.13.C
1
1
3
3
4.2.13.A
4.2.13.D
2
Hepatit D (Delta ajanlı Hepatit-B) hastalarında tedavi
interferonlar toplam 30MilyonÜ/hafta ve 120MilyonÜ/ay maximum 48 hafta kullanılabilir
Bu hastalardan Kronik Hepatit B tedavi koşullarını taşıyanlarda tedaviye oral antiviral ilaçlardan biri eklenebilir.
Anti HDV(+) ve HBV DNA sonucu reçete veya raporda belirtilir
1
1
1
8
7
RAPOR YENİLEME
HepatitB tedavi süresi
HBsAg (+) liği ve " başlama kriterlerinin hastanın tedavisine başlandığı tarihteki mevzuata uygundur " ibaresinin olması yeterlidir.
HBsAg antijeninin negatifleşmesiyle birlikte Anti-HBsAg antikorunun oluşmasından sonra 12 aydır