Kanser Oluşumu ve Risk Faktörleri
advertisement

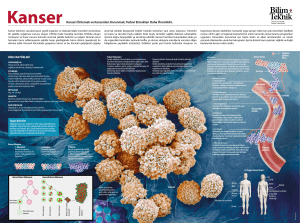
Kanser Oluşumu ve Risk Faktörleri Doç. Dr. Mustafa Benekli Gazi Üniversitesi Tıp Fakültesi Tıbbi Onkoloji Bilim Dalı 1 Kanser: Genel Etiyoloji ve Patogenez • Etyolojik ajanlar: – Çevresel (kimyasal, fiziksel, ve biyolojik) – Kalıtsal (ailesel kanser sendromları) • Genel mekanizmalar: – Edinsel kabiliyetler (Kendi kendine replikasyon, daha uzun yaşam, genetik instabilite, neoangiogenez, invazyon ve metastaz) – Onkojen aktivasyonu, TSG inaktivasyonu, etkisiz DNA tamiri 2 Çevresel ve Kalıtsal Kanser 100 85 80 60 40 15 20 0 Canceretiyolojisi Etiology Kanser Environmental Çevresel Hereditary Kalıtsal 3 4 Çevresel Karsinogenez • Kansere sebep olan bir ajan vardır. • Üç ana tip: – Kimyasal – Fiziksel (radyasyon) – Biyolojik (virüsler vs) 5 Kimyasal Karsinogenez • İlk kez 1775’te Sir Percival Pott tarafından tarif edilmiş – Baca temizleyicilerinde skrotal kanser gelişmesi – Baca kurumuna mesleki maruziyet ve skrotal kanser riski arasındaki ilişki ortaya konmuş 6 Kimyasal Karsinogenez • Doğrudan etkili – Nitrogen mustard – Nitrosomethylurea – Benzyl chloride • Dolaylı etkili (aktif metabolite çevrilmesi gerekir) – Polisiklik aromatik hidrokarbonlar (PAH) – Organik ürünlerin tam yanmaması sonucu üretilir – Baca kurumunda, mangalda ızgara etlerde, otomobil egzozlarında ve sigarada vardır 7 Çevresel Karsinojenler • • • • • Aflatoksinler Asbestos Benzen Kadmiyum Kömür tozu • • • • DDT PAH Radon Güneş ışığı 8 Karsinojen İlaçlar • • • • • • Adriamisin (doxorubicin) Androjenik steroidler Chlorambucil Cisplatin Cyclophosphamide Cyclosporin A • • • • Diethylstilbestrol Ethylene oxide Melphalan Tamoxifen 9 Fiziksel Karsinojenler • Ultraviolet ışık • İyonize radyasyon (X-ray) • Asbestos 10 11 Cilt kanseri en sık görülen ve en önlenebilir kanserdir • Yılda yaklaşık 10 milyon cilt kanseri vakası • Bütün diğer kanserlerin toplamından fazla • Bunların çoğu UV radyasyona bağlı 12 Asbest • Batı ülkelerinde inşaat, izolasyon ve gemi endüstrisinde kullanılır • Ülkemizde çevresel karsinojen 13 İyonize Radyasyon • Rasyasyon araştırmacılarının kanserden ölümleri üzerine araştırılmış • 1940’lı yıllarda radyologlar arasında sık lösemiler • Radyum ile saat kadranı boyacıları arasında sık osteosarkom 14 Viral Karsinogenez • Viral infeksiyonlar tüm kanserlerin 1/7’sinden sorumludur • Bunların çoğunluğu 2 DNA virüs infeksiyonuna bağlıdır: – HBV - hepatosellüler kanser – HPV – serviks kanseri 15 Onkojenik Virüsler • • • • • • Human papillomavirüsü - HPV Epstein-Barr Virüsü (EBV) Human herpesvirüs 8 (HHV8) Hepatitis B virüsü - HBV Hepatitis C virüsü - HCV HTLV-I, HTLV-II 16 Virüsler Nasıl Kanser Yapar? • Çok küçük virüsler • Viral DNA’larını konakçı genomuna yerleştirebilirler • Yeni oluşan DNA viral proteinler sentezler: – Tümör supressor proteinler bloke edilir – Onkogen olarak tümör başlatılır 17 Helikobakter pilori • Gastrik infeksiyon – lenfoma ve mide kanseri ile ilişkili • Mide lenfomalarının çoğunda H pylori vardır • Bu lenfomaların tedavisi antibiyotiklerle yapılabilir 18 Kanser Biyolojisi 19 Moleküler Kanser Yolakları 20 Kanser çok basamaklı bir hastalıktır Değişik genlerdeki sayısız mutasyonlar normal hücrelerin kanserleşmesi için gereklidir Bu mutasyonların birikimi kanserin neden geç yaşlarda daha sık görüldüğünü de açıklar Kanserler klonaldir Bir tümördeki bütün hücreler tek bir kök hücreden oluşur Kanserler genetik olarak stabil olmadıklarından, tümördeki bütün hücreler aynı genotipe sahip değildir Bu nedenle bir seçicilik vardır Klonal seçicilik sonucunda en kuvvetli büyüme özelliklerine sahip hücreler öne çıkarlar 21 Kanser Oluşumu 22 Genetik Kanser Mekanizmaları • Tek “büyük” genetik anormallikler – Translokasyonlar • Malign lenfomalar • Sarkomlar Aktive edici mekanizmalar • Çoklu “noktasal” genetik değişiklikler • Karsinomlar • Malign melanom – Mutasyonlar – LOH Aktive/inaktive edici mekanizmalar 23 Tümörlerdeki Genetik Mekanizmalar • Aktive ve inaktive edici olabilir • Dominant / Resesif / Dominant negatif • Somatik veya germline • Genetik hedefler (onkogenler, tümör supresör genler, mismatch tamir genleri) • Telomer kısalması / telomeraz 24 Tümörlerdeki Genetik Mekanizmalar • Gen delesyonları / amplifikasyonları • Mutasyonlar • • Insertional • Nokta mutasyonları Genetik instabilite • Mikrosatellit instabilite (MSI) • Kromozomal instabilite (CIN) 25 Kanserde Spesifik Hücresel Fonksiyonlar: Genetik Değişiklikler Genetik instabilite DNA Tamiri KANSER Tümör Supresör Genler Interstisyel Delesyon İnaktive edici Mutasyon Hipermetilasyon Onkogenler Gen Amplifikasyonu Gen Overekspresyonu 26 Aktive edici Mutasyon Kanserde Hücresel Fonksiyon Değişiklikleri DNA Repair Tümör Supresör Genler Onkogenler İnaktivasyon Aktivasyon Diferansiasyon Apoptoz/Proliferasyon KANSER 27 Mismatch Tamir ve Mikrosatellitler 28 Telomerler ve hücre yaşlanması 29 Somatik Mutasyonlar • Sık görülür • 1 mutasyon/hücre bölünmesi • Normalde bir sonuca yol açmaz • Gelecek kuşağa aktarılmaz • Vücutta 1 hücrenin anormal olması önemli değil 30 Mutasyonların çok küçük bir bölümü doğuştandır (germinal mutasyonlar) – Etkilenen bireylerin tüm somatik hücrelerinde vardır – Kanser sadece spesifik dokularda gelişir – Kanser riskinde artış gelecek kuşaklara da aktarılır 31 Hücre büyümesini kontrol eden 7 protein Onkogenler: Büyüme faktörleri (I) Büyüme faktörü reseptörleri (II) Sinyal iletim proteinleri (III) Transkripsiyon faktörleri (IV) Tümör supresörler: Pro- veya anti-apoptotik proteinler (V) Hücre siklusu kontrol proteinleri (VI) DNA tamir proteinleri (VII) 32 Proto (onkogen) ler • 50’den fazla tespit edilmiştir • Mutasyon ile kalıcı aktive olurlar – dominant özellik gösterirler • Önemli hücresel yolaklarda rol alırlar (hücre siklusu, apoptoz, anjiogenez, vs) • Mutasyona uğramış onkogenlerde “gain-offunction” değişiklikleri vardır – Nokta mutasyonları – Kromozom rearranjmanları – Gen amplifikasyonları 33 Onkogenler • RAS – çeşitli kanserlerde aktif (özellikle kolon) • c-MYC – kolon ve akciğer kanserleri, lenfoma • RET - MEN 2a • MET - herediter papiller renal kanser • CDK4 - familial melanoma • BCR/ABL - KML • BCL2 - folliküler lenfoma 34 Tümör Supresör Genler Hücre bölünmesinde fren görevi görür “GUARDIAN OF THE GENOME” PROBLEM: Tümör supresör genlerde mutasyon = frenler çalışmıyor, veya mutasyon birikimi var (DNA tamir enzimlerinde) 35 Tümör Supresör Genler “örnekler” •p53 – çeşitli tümörler •RB1 - retinoblastoma geni •WT1 - Wilm's tumörü geni •NF1 - neurofibromatosis type 1 geni •NF2 - neurofibromatosis type 2 geni •DCC – kolon kanseri •BRCA1, BRCA2 – meme kanseri 36 Tümör Supresör Genler • Ailesel kanser sendromları • Sık görülen kanserlerde inaktivasyon – Loss of Heterozygosity • Hücresel düzeyde “resesif” • “Two-hit” hipotezi 37 Tümör Supresör Genler “Two-Hit” Hipotezi İlk mutasyon ebeveyn germline İlk mutasyon çocukta germline İkinci mutasyon (tümör) 38 Tümör Supresör Genler: p53 39 Kanserin Temel Biyolojik Özellikleri Diferansiasyon Anormal Proliferasyon Angiogenez İnvazyon Onkojenik lezyon (ör, RAS, MYC, E2F Aktivasyonu) Apoptoz Yaşlanma 40 Çok Basamaklı Tümorigenez 41 Kanser Hücrelerinin Özellikleri • Kendi kendine yenilenme • Daha uzun yaşam • Genetik instabilite • Yeni damarlar oluşturabilme • İnvazyon ve metastaz yapma – Apoptoz downregulasyonu – İnhibitör faktörlere cevapsızlık – Kendi kendine çoğalma 42 Kanser Hücrelerinin Özellikleri • Kendi kendine yenilenme • Daha uzun yaşam • Genetik instabilite • Yeni damarlar oluşturabilme • İnvazyon ve metastaz yapma – Apoptoz downregulasyonu – Telomeraz reaktivasyonu 43 Kanser Hücrelerinin Özellikleri • Kendi kendine yenilenme • Daha uzun yaşam • Genetik instabilite • Yeni damarlar oluşturabilme • İnvazyon ve metastaz yapma – Genetik hasar – Mutajenik ajanlar – Bozuk tamir sistemleri 44 Kanser Hücrelerinin Özellikleri • Kendi kendine yenilenme • Daha uzun yaşam • Genetik instabilite • Yeni damarlar oluşturabilme • İnvazyon ve metastaz yapma 45 Adhezyon Molekülleri 46 Metastaz Kaskadı 47 İnfiltrasyon Basamakları 48 Metastaz Kaskadı 49 Tümör Mikroçevresi 50