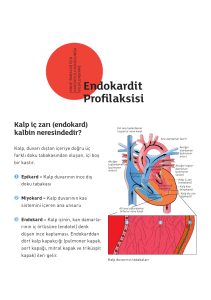
sol kalp infektif endokarditli hastalarda n
advertisement

T.C. SAĞLIK BAKANLIĞI KARTAL KOŞUYOLU YÜKSEK İHTİSAS EĞİTİM VE ARAŞTIRMA HASTANESİ KOŞUYOLU KALP MERKEZİ KARDİYOLOJİ KLİNİĞİ KLİNİK ŞEFİ: Doç.Dr.YELDA BAŞARAN SOL KALP İNFEKTİF ENDOKARDİTLİ HASTALARDA N-TERMİNAL B-TİP NATRİÜRETİK PEPTİD’İN PROGNOSTİK DEĞERİ UZMANLIK TEZİ Dr. GÖKHAN KAHVECİ İSTANBUL 2006 İÇİNDEKİLER 1. Özet/Summary...................................................................3 2. Genel Bilgiler 2.1.İnfektif Endokardit…………..........................7 2.2. B-Tip Natriüretik Peptid...............................41 3.Giriş ve Amaç.....................................................................43 4. Metodlar............................................................................43 5. Bulgular.............................................................................46 6. Tartışma.............................................................................54 7. Çalışma kısıtlılıkları…………………………………….56 8. Sonuç..................................................................................56 9. Kaynaklar..........................................................................57 1. ÖZET SOL KALP İNFEKTİF ENDOKARDİTLİ HASTALARDA N-TERMİNAL B-TİP NATRİÜRETİK PEPTİD’İN PROGNOSTİK DEĞERİ 2 Giriş İnfektif endokardit (İE) tanı ve tedavideki büyük gelişmelere rağmen, hala ölüm oranı yüksek, hayatı tehdit eden bir kalp hastalığıdır. Başvuru sırasındaki risk değerlendirmesinde faydalı olabilecek yeni laboratuvar belirteçlerine ihtiyacımız vardır. Bu prospektif çalışmanın amacı N-Terminal B-Tip natriüretik peptid’in (NT-proBNP) , sol kalp endokarditi olan hastalardaki prognostik değerinin belirlenmesidir. Metodlar ve Bulgular Modifiye Duke kriterlerine göre kesin sol kalp infektif endokarditi tanısı almış 42 ardışık hasta ( 33 erkek, ortanca yaş 44 [9-75]) prospektif olarak çalışmaya dahil edildi. Başvuru NT-proBNP serum düzeyleri, bazal fonksiyonel, ekokardiyografik parametreler ve klinik sonlanım ile birlikte değerlendirildi. Hastalar erken cerrahi (ilk 30 gün) ve kardiyovasküler ölümden oluşan bileşik sonlanım noktası için takip edildiler. 32 (%76) hastada olumsuz klinik olaylar gözlendi. Hastaların 29’na erken cerrahi girişim (0 ile 30. günler arası, ortanca 6.gün) uygulandı ve 6’sında operasyon sonrası olmak üzere toplam 9 hastada ölüm gerçekleşti. Olumsuz klinik olaylar için yapılan ünivaryant analizde, log Nt-proBNP, New York Heart Association (NYHA) fonksiyonel sınıf III-IV, sol atriyum çapı ve ileri kapak tetersizliği prediktif faktörler olarak tespit edildi. Multivaryant analizde ise, log Nt-proBNP (Risk oranı=[HR]=1.54; 95% [CI] 1.2 to 1.9, p<0.001) olumsuz klinik olayların tek bağımsız prediktörü olarak bulundu. Log Nt-proBNP’nin olumsuz klinik olayları belirlemedeki yeterliliği receiver operating curve (ROC) analizi ile değerlendirildi. Log Nt-proBNP’nin en yüksek sensitivite (%94) ve spesifisite (%72) gösterdiği değer 7.3 ve bunun pg/mL cinsinden karşılığı 1500 3 olarak bulundu. Olaysız sağkalım oranının Nt-proBNP seviyeleri 1500 pg/mL üstünde olan hastalarda anlamlı olarak daha düşük olduğu görüldü. Sonuç Sol kalp endokarditlerinde NT-proBNP, klinik ve ekokardiyografik değerlendirmenin ötesinde önemli prognostik bilgi vermektedir. Bundan dolayı sol kalp endokarditi olan hastalarda , risk derecelendirmesinde faydalı bir belirteç olarak kullanılabilir. 4 1. SUMMARY PROGNOSTIC IMPORTANCE OF N-TERMINAL PRO B-TYPE NATRIURETIC PEPTIDE IN LEFT-SIDED INFECTIVE ENDOCARDITIS Introduction Infective endocarditis (IE) is a life-threatening clinical condition that has still higher mortality rate despite the great progress made in the diagnosis and treatment. We need new laboratory markers for risk stratification on admission. The aim of this prospective study was to determine the prognostic value of NT-proBNP serum levels in patients with left-sided İE. Methods and Results Fortytwo consecutive patients ( 33 men, median age 44 years [9-75]); who fulfilled the modified Duke’s criteria for definite IE were prospectively included in the study. NT-proBNP serum level on admission was evaluated with baseline functional and echocardiographic parameters as well as clinical outcome. Patients were followed for clinical endpoints defined as a composite of early surgery (within 30 days) and cardiovascular death. 32 patients (%76) experienced clinical endpoints. Of the 32 patients with IE, 29 underwent early surgery (between 0-30. days, at a median time of 6 days) and in-hospital death occured in 9 patients. Variables associated with an increased hazard of clinical endpoints in univariate analysis were log Nt-proBNP, NYHA functional class III-IV, left atrium diameter and severe valvular regurgitation. Multiple logistic regression analysis revealed that log NT-proBNP (Hazard ratio [HR]=1.54; 95% confidence interval [CI] 1.2 to 1.9, p<0.001) was the only significant independent predictor of clinical outcome on admission. The best value of log Nt-proBNP with the highest sensitivity (%94) and spesificity (%72) was 7.3, equivalent to a level of 1500 pg/mL. The event free survival was found to be significantly lower in patients with NtproBNP levels ≥1500 pg/mL. 5 Conclusions NT-proBNP provide important prognostic information beyond clinical and echocardiographic evaluation in left-sided endocarditis. NT-proBNP may serve as useful laboratory marker for stratification of high-risk patients. 6 2. GENEL BİLGİLER 2.1. İNFEKTİF ENDOKARDİT 2.1.1.Tanım İnfektif endokardit (İE) kalbin endotelyal yüzeyinin mikrobik infeksiyonu ile oluşan hastalıktır. Genellikle kalp kapaklarının üzerinde oluşan ,ancak endokardın herhangi bir alanını da tutabilen ‘vejetasyon’ karakteristik lezyonudur. Bazen büyük arterlerin iç yüzeyinde endotelden kaynaklanan nidus üzerinde de infeksiyon oluşabilir ki bu da ‘infektif endarterit’ adını alır. Ayrıca intrakardiyak yabancı cisimlerde ( pacemaker veya intrakardiyak defibrilatör (ICD) lead’i, cerrahi conduit’ler vs.) de mikrobiyal infeksiyon bu tanım altında toplanabilir. Her nekadar klinik bulgular ve tedavi açısından infektif endokardite uysa da; intravasküler veya intrakardiyak yerleştirilen ancak endokard ile teması olmayan girişim aygıtlarında oluşan mikrobiyal infeksiyon ‘polimer ile ilişkili infeksiyon’ olarak tanımlanmaktadır. Karakteristik lezyon olan vejetasyon; trombosit, eritrosit, fibrin, inflamatuvar hücre ve mikroorganizma topluluğundan oluşur. Vejetasyonun izlenmediği durumlarda lezyon, ülserasyon, abse veya destrüksiyon şeklinde gözlenir (1). 2.1.2.Epidemiyoloji İE insidansı 1950-1987 yılları arasında sabit iken, 80’li yıllardan sonra artış göstermiştir. Özellikle batı toplumlarında yapılan prospektif çalışmalarda yıllık 1,96,2/100000 olarak tespit edilmiştir (2). Ancak ülkemizdeki insidansı bilinmemektedir. Gelişmekte olan ülkelerde daha çok romatizmal kalp hastalığı (RKH) olan çocuk ve gençlerde daha fazla görülürken, ortalama ömrün uzamasıyla özellikle batı ülkelerinde yaşlılığa bağlı dejeneratif kalp hastalığı (DKH) olanlarda daha fazla izlenmektedir. 2.1.3.Sınıflandırma ve Terminoloji Günümüzde sınıflandırma artık akut, subakut şeklinde yapılmamaktadır. Hastalığın aktivasyonu, anatomik lokalizasyonu ve mikrobiyolojik etkene göre yapılmaktadır. 7 1) Hastalığın aktivasyonuna göre: aktif İE , iyileşmiş İE , tekrarlayan IE 2) Hastalığın tanımlanmasına göre: kesin IE , şüpheli IE , olası IE 3) Hastalığın patolojisine göre: nativ kapak İE , protez kapak IE (erken ve geç) 4) Lezyonun yerleşimine göre: sağ kalp İE, sol kalp IE 5) Hastalığa neden olan mikroorganizmanın üremesine göre: mikrobiyolojik açıdan pozitif, mikrobiyolojik açıdan negatif gibi. Nozokomiyal infektif endokardit hastanın hastaneye kabulünden itibaren 72 saat içinde ya da son 6 ay içinde hastanede uygulanmış bir girişim sonrasında gelişen hastane kökenli endokardit için kullanılır. Görülme oranı %5-29 ‘dur ve ensık etken S.aureus’ tur (3). Aktif endokardit terimi cerrahi için önemlidir. Eğer tam doz ve süre antibiyotik tedavisi bitmeden hasta opere olduysa ‘aktif endokardit sırasında cerrahi’ ya da ‘erken cerrahi’ olarak isimlendirilir. 2.1.3.1.Nativ Kapak Endokarditi (NKE) Epidemiyolojik özellikler yaşam süresinin uzamasıyla değişmektedir. Protez kapak replasmanlarının, hastane kökenli vakaların ve uyuşturucu madde kullanımının artmasıyla birlikte hastalığın profili değişmektedir. Gelişmiş ülkelerde NKE’i en sık mitral kapak prolapsusu olanlarda görülürken, gelişmekte olan ülkelerde muhtemel en sık neden romatizmal kalp hastalığıdır. NKE’i gelişimi için risk faktörleri; kötü dental hijyen, uzun süreli diyaliz, diyabetes mellitus, uyuşturucu madde bağımlılığı ve AIDS’tir. Uyuşturucu madde bağımlılarında insidans yıllık 150-2000/100000’dir. AIDS hastalarında ise ensık etken S.aureus’ tur ve bunlarda mortalite oldukça yüksektir (4). 8 2.1.3.2.Protez Kapak Endokarditi (PKE) Gelişmiş ülkelerdeki endokardit olgularının %7-25’ni oluştururlar. PKE riski operasyon sonrası ilk 12 ayda %1 iken, 60 ayda %2-3’tür (4). Operasyon sonrası ilk 12 ay içinde PKE gelişen olgular daha çok hastane kökenlidir ve erken PKE olarak adlandırılırlar. 12 aydan sonraki olgularda etkenler toplum kökenlidir ve geç PKE olarak adlandırılırlar (1). 2.1.4.Mikrobiyolojik Etkenler Streptokoklar NKE’nin %30-65’inden sorumludurlar (Tablo 1). Normal orofarenks mukozasında bulunurlar. Ensık izole edilen streptokok türleri ise Strep.sanguis, Strep.bovis, St.mutans ve Strep.mitis’ tir. St.bovis, streptokoklara bağlı NKE’nin %25-40’nı oluşturur ve yaşlılarda kolonik kanserle ilişkili endokardite neden olabilir. Ayrıca son yıllarda sınıflandırmaya yeni eklenen, yavaş üreyen streptokok türleri Abiotrophia adı altında toplanmışlardır. B grubu streptokoklar (St.agalactiae) , G grubu streptokolar, St.milleri ve St.pneumonia hasar verici, ciddi NKE’ne neden olurlar. Abiotrophia hariç diğer viridans streptokoklar çopu zaman penisiline duyarlıdır (minimum inhibe edici konsantrasyon [MİK]≤0.1 µg/mL) (5). Yeni serilerde İE’in en sık etkeni olarak stafilokoklar özellikle de S.aureus, viridans streptokokları geçmiştir. S.aureus akut, toksik tabloyla giden, %30-50 oranında kalp yetersizliği (KY) ve santral sinir sistemi (SSS) komplikasyonlarıyla seyreden endokardite yol açar. S.aureus endokarditine bağlı %16-65 oranında ölüm gözlenir. S.aureus olgularının %90’ı beta laktamaz üretir ve penisilin, ampisilin ile üreidopenisilinlere dirençlidirler. Koagulaz negatif stafilokoklar (KNS) (öz. S.epidermidis) erken PKE’nin ensık etkenidirler (5) (Tablo 2). KNS olan Staphylococcus lugdunensis ağır kapak hasarıyla giden, ciddi NKE’e yol açmaktadır (6) 9 Tablo 1. NKE’de Mikrobiyolojik Etkenler ve Altta Yatan Kalp Hastalıkları (%) Hastalık Yenidoğan 2 ay-15 yaş 15-60 yaş >60 yaş RKH - 2-10 25-30 8 KKH 28 75-90 10-20 2 MVP - 5-15 10-30 10 DKH - - Nadir 30 UMB - - 15-35 10 Diğer - - 10-15 10 Yok 72 2-5 25-45 25-40 Streptokoklar 15-20 40-50 45-65 30-45 Enterokoklar - 4 5-8 15 S.aureus 40-50 25 30-40 25-30 KNS 10 5 3-5 5-8 GNB 10 5 4-8 5 Mantarlar 10 1 1 Nadir Polimikrobiyal 4 - 1 Nadir Diğer - - 1 2 Kültür Negatif 4 3-10 5 Etken 0-15 KKH,konjenital kalp hastalığı; MVP, mitral kapak prolapsusu; UMB,uyuşturucu madde bağımlılığı; GNB, gram negatif basil 10 Tablo 2. PKE’ de Mikrobiyolojik Etkenler Cerrahi sonrası (%) Etken <2 ay 2-12 ay >12 ay Streptokoklar 1 9 31 Pnömokoklar - - - Enterokoklar 8 12 11 S.aureus 22 12 18 KNS 33 32 11 HACEK - - 6 Gram(-) basiller 13 3 6 Mantarlar 8 12 1 Polimikrobiyal 3 6 5 Difteroidler 6 - 3 Kültür negatif 5 6 8 KNS, koagülaz negatif stafilokoklar; HACEK, Hemophilus, Actinobacillus, Cardiobacterium, Eikenella ve Kingella 11 Enterokokkal bakteriyemisi olan hastaların %10’ unda endokardit gelişebilir, çoğunlukla hastane kaynaklıdır ve antibiyotiklere dirençlidir (4). Ensık etken E.faecalis’ tir. Enterokoklar sefalosporinler, oksasilin, nafsilin ve terapötik dozdaki aminoglikozidlere dirençlidirler (5). Gram negatif bakterilerden, Hemophilus, Actinobacillus, Cardiobacterium, Eikenella ve Kingella, HACEK grubu olarak adlandırılır ve endokardit nedenidirler. Vurgulanması gereken besiyerinde yavaş üremeleridir (7). Coxiella burnetti infeksiyonları hayvanların çıkartılarının inhalasyonu ile bulaşır. Coxiella endocarditi subakut tabloyla seyreder. Tanısı tipik olarak antifaz-1 IgG antikorlarının serolojik yöntemlerle belirlenmesiyle konur (8). Son olarak mantarlardan ensık Candida albicans, Histoplasma ve Aspergillus türleri endokardite yol açar. Çoğunlukla hastane kökenlidirler ve immünsüprese bireylerde gelişirler. Tanısı kültür ve direk histolojik inceleme ile konur (5). 2.1.5.Patogenez Hasarlı endokardiyuma tutunan steril mikrotrombüsler endokarditin asıl çekirdeğini (nidus) oluşturmaktadır. Buna nonbakteriyel trombotik endokardit (NBTE) te denir. Hemodinami (mekanik stres ) ve immun sistem, endokardiyal hasar ve NBTE oluşumunda büyük rol oynamaktadır. Özellikle kapakların kapanma çizgileri bu şartlara çok uygundur. Mikroorganizmanın hasarlı endotele adezyonunda, memeli hücresinin önemli yüzey glikoproteini ‘fibronektin’ temel rol alır. Konakçı immün sistem mekanizmasının zayıflaması adezyonu trombüs arttırır. Bundan sonra bakteri sadece çoğalmakla kalmaz, aynı zamanda yeni oluşumunu ve nötrofil kemotaksisini tetikler. Gram (+) bakteriler serumun bakterisidal özelliğine karşı dirençli olmalarına karşın gram (-)’ lerde bu daha zayıftır. Gram (+) bakterilerin neden olduğu endokarditin sık olmasının nedeni de budur. NKE, lokal (valvüler ve perivalvüler destrüksiyon) ve distal (vejetasyon embolizmi, septisemi ve 12 metastatik enfeksiyon) olarak patolojik sınıfa ayrılır. Ekstrakardiyak embolik komplikasyonlar sanıldığından daha sık gözlenmektedir (%22-45). Metastatik enfeksiyon sonucu menenjit, miyokardit, piyelonefrit ortaya çıkmakta; septisemi ise dissemine intravasküler koagülopatiye neden olmaktadır. İmmün kompleks depolanmasına bağlı olarak diffüz ya da fokal glomerulonefrit oluşur. Mikotik anevrizma geniş ve orta çaplı arterlerin ; osler nodülü ise küçük damarların nekrotizan vaskülitidir (1,5). Vejetasyon yerleşimi atriyo-ventriküler kapakların atriyal yüzeyi, semilunar kapakların ise ventiküler yüzeyindedir. Özellikle tutulan kısım kapakların kapanış çizgileridir. Stafilokok endokarditinde harabiyet daha fazla olup; küspis ya da leaflet perforasyonu, kordal yapılarda rüptür sonucunda da kapak yetersizliğine bağlı KY kaçınılmaz sonuçtur. İnfeksiyonun aort duvarında lokal yayılımı sonucunda; sinüs Valsalva anevrizması, ring absesi, psödoanevrizma ,kalp boşluklarına fistülizasyon, perikardiyal efüzyon veya kalp tamponadı gibi komplikasyonlar oluşur. Ayrıca mitral-aortik fibröz bileşke tutulumu, aortik vejetasyonun mitral kissing vejetasyon oluşturması infeksiyonun lokal yayılımı sonucunda gelişen major komplikasyonlardır (1). Mekanik protez kapak varlığında infeksiyonun tutulum yeri perivalvüler dokulardır. Ayrıca periprostetik kaçak yada dehisens (ayrışma), ring absesi, ileti sistemi bozuklukları ve pürülan perikardit gibi komplikasyonlar eşlik eder. Daha nadir ancak ciddi komplikasyonlardan protez kapak obstrüksiyonu hastalığın prognozunu kötü yönde etkiler. Biyoprotez kapaklarda, kapakların mobil kısmı dokudan oluşur. Gluteraldehit fiksasyonuna rağmen enfeksiyonun başlangıç yeri burası olabilir ve kapak perforasyonu olabilir (1). 2.1.6.Klinik Özellikler İE hastası çoğu zaman kalp içi infeksiyonun yayılımının bir sonucu olan kalp dışı bulgular ile karşımıza gelir. Ensık görülen bulgu ateştir ancak KY, kronik renal yetersizlik, 13 kronik karaciğer hastalığında, önceden antibiyotik almış hastalarda ve virulansı az olan bakterilerle olan endokarditlerde ateş olmayabilir. Diğer semptomlar; zayıflama, gece terlemeleri, eklem ağrıları, halsizlik ve nefes darlığı olabilir. Hastaların %80-85’ de üfürüm duyulur. Triküspit kapak endokarditlerinde üfürüm genelde duyulmaz. Yeni ya da değişen üfürümler subakut NKE’de daha az iken, akut İE ve PKE’de daha sıktır. Splenomegali hastaların %15-50’ de görülür ve daha uzun süreli endokarditlerde gözlenir. İE’in periferik bulguları günümüzde daha azdır. Peteşiler en sık görülenidir; konjonktiva, oral mukoza ve extremitelerde olabilir. Splinter (subungual) hemorajiler tırnak yataklarında, Osler nodülleri parmaklarda, Janeway lezyonları avuç içi ve ayak tabanlarında ve Roth lekeleri retinada gözlenir. Sistemik emboliler hastaların %40’ında saptanır. Antibiyotik alımıyla birlikte emboli riski azalır. Nörolojik semptomlar, hastaların %30-40’ında izlenir ve yüksek mortalite ile ilşkilidir. S.aureus endokarditinde sıktır. Embolik inme, serebral hemoraji, mikotik anevrizmalar, serebral apseler ve pürülan menenjitler bu semptomlara yol açabilirler. İmmünkompleks glomerülonefritine bağlı akut böbrek yetersizliği hastaların %15’inde izlenir. Fokal glomerülonefrit ve böbrek infarktları hematüriye neden olabilir (4,5). 2.1.7.Tanı İE tanısı, klinik, laboratuvar ve ekokardiyografik bilgilerin bir arada değerlendirilmesiyle konur. Anemi, lökositoz, C-reaktif protein (CRP) ve sedimentasyon hızı (ESR) tanı için nonspesifik bulgulardır. İE tanısı için henüz optimal bir tanı yöntemi yoktur. 1994 yılında Duke ve ark. şüpheli hastalar için tanı kriterlerini standardize etmişlerdir (9). İE tanısında Duke kriterlerinin güvenilirliği birçok kez test edilmiştir. Çalışmalarda spesifisitesi %99, negatif prediktif değeri %92 olarak saptanmıştır (10,11). Kültür negatif endokarditlerin 14 (KNE) yanlış sınıflandırılması, transözofageal ekokardiografinin (TEE) kullanımının artması ve S.aureus endokarditinde artmış olan endokardit riski gibi nedenlerden dolayı Duke kriterlerinin yeterliliği sorgulanmıştır. ‘Modifiye Duke Kriterleri’ günümüzde tercih edilen tanı kriterleridir (12). Klinik kriterlerden 2 majör, 1 majör 3 minör ya da 5 minör kriter tanı için gereklidir (Tablo 3). 2.1.7.1.Ekokardiyografi Tanı ve tedavide ekokardiyografi en önemli basamaktır. Hareketli intrakardiyak kitle (vejetasyon), apse, yeni oluşmuş valvüler kaçak ve protez kapağın kısmen ayrışması ekokardiyografik tanı kriterleridir. Şüpheli tüm hastalarda transtorasik ekokardiyografi (TTE) yapılmalıdır. TEE ise; şüpheli endokarditte, görüntü kalitesi kötü olan hastalarda, protez kapak hastalarında, komplikasyon şüphesi yüksek hastalarda (S.aureus endokarditi), TTE ‘de bulgu saptanamayan ancak yüksek klinik şüphenin olduğu durumlarda endikedir (13). VejetasyonlarTTE ile %50 oranında saptanır. Tespiti zorlaştıran faktörler; kötü eko penceresi, protez materyalin varlığı, personelin tecrübesi, vejetasyon lokalizasyonu, vejetasyon boyutları ve eşlik eden romatizmal ya da dejeneratif kapak hastalığının bulunmasıdır. TTE’de 5 mm’nin altındaki vejetasyonlar %25 oranında tespit edilirken, bu oran 6 mm’nin üzerindeki vejetasyonlarda %80’lere ulaşmaktadır. Protez kapak varlığında TTE’nin tanı değeri çok düşer. TEE ise %88-100 duyarlılık ve %91-100 özgüllük ile tercih edilmesi gereken tanı yöntemidir. Negatif TEE sonucunun negatif prediktif değeri %68-97’ dir. Ekokardiyografik olarak vejetasyonun aktif yada iyileşmiş olup olmadığını ayırt etmek mümkün değildir. Antibiyoterapiden 3 hafta sonra ekokardiyografik inceleme yapıldığında; vejetasyonların %30 oranında kaybolduğu, %18 küçüldüğü, % 41 değişmediği 15 Tablo 3. Modifiye Duke Kriteleri Kesin İnfektif Endokardit Patolojik Kriterler--vejetasyon, embolize olmuş vejetasyon ya da intrakardiyak apseden, kültür ya da histoloji ile etkenin gösterilmesi --vejetasyon ve intrakardiyak apse gibi patolojik lezyonlarda histolojik olarak aktif endokarditin gösterilmesi Klinik Kriterler Majör Kriterler: 1)Pozitif Kan Kültürü-I. İE için tipik olan etkenlerin en az 2 ayrı kültürde üremesi (Viridans streptokoklar, St.bovis, HACEK, S.aureus ya da primer odak yokluğunda enterokoklar) II. İE’e neden olabilecek etkenlerin sürekli olarak kültürde üremesi (12 saatten daha fazla ara ile alınan ≥2 kültürde üreme ya da 1.’si ve sonuncusu arasında enaz 1 saat olan 3 kültürde ya da daha fazla kültürde üreme olması) III. Coxiella burnetti için tek kan kültüründe üreme ya da antifaz I IgG antikor titresi>1:800 olması 2)Endokardiyal Tutulum Göstergesi I. Pozitif ekokardiyogram-a.kapak ya da destek yapılarda, kaçak jetinin çarptığı yerlerde, implante materyallerin üzerinde hareketli kalp içi kitle (vejetasyon) b.Apse c.Protez kapakta yeni kısmi ayrışma (dehisens) II. Yeni gelişmiş valvüler kaçak 16 Tablo 3. Modifiye Duke Kriterleri-devamı Minör Kriterler: -Predispoze kalp hastalığı ya da uyuşturucu madde kullanımı -≥38ºC olan ateş -Vasküler fenomen: majör arteryel emboli, septik pulmoner infarkt, mikotik anevrizma, intrakraniyal kanama, konjonktival kanama, Janeway lezyonu -İmmünolojik fenomen: glomerulonefrit, Osler nodülü, Roth lekesi, romatoid faktör pozitifliği -Mikrobiyolojik kanıt (majör kriteleri karşılamayan kan kültürü üremesi ya da serolojik bulgu) ve %11 büyüdüğü saptanır. Vejetasyonun ayırıcı tanısında; trombüs, tümöral yapılar (papiller fibroelastom), infektif olmayan ve kapakla ilgili kitleler (Libman –Sacks endokarditi, Behçet hastalığı, karsinoid ve akut romatizmal ateş kitleleri) varlığında gözlenebilir (1). Kapak yetersizliği; kapak perforasyonu, vejetasyonun neden olduğu koaptasyon kusuru ya da korda rüptürü nedeniyle olabilir. Aort ve mitral kapak hasarında TEE doğru bilgi verir. Perivalvüler yayılım ve miyokardiyal apsenin saptanmasında TEE daha sensitiftir. Spektral ve renkli Doppler yöntemleri ile, fistül, psödoanevrizma, apse ve kapak perforasyonu doğru şekilde tespit edilebilir (4). Başvuru sırasındaki TTE ve TEE’de bulgu saptanamayan ancak endokardit şüphesi devam eden hastalarda 7-10 gün sonra TTE tekrarlanmalıdır. Bu süreçte daha önce 17 saptanamayan vejetasyonlar büyüyüp daha belirgin hale gelebilir. Eğer tekrar yapılan TEE negatif ise İE tanısından uzaklaşılır (14). 2.1.7.2. Kan Kültürü En az 3 kan kültürü en az 1 saat ara ile alınmalıdır. Bir kan kültür seti 1 aerop ve 1 anaerop ortam içermelidir. Minimum 5 mL, optimali 10 mL kan her seferinde ayrı bir venden alınır. Septik hastalar hariç antibiyotik tedavisi kültürde üreme olana kadar ertelenmelidir. Başvuru sırasında eğer hasta antibiyotik alıyorsa, antibiyotikler kesildikten 3-7 gün sonra kan kültürü alınmalıdır. Üreme olan hastalar için, antibiyotik duyarlılık testleri yapılmalı ve MİK lar belirlenmelidir (1). 2.1.7.3. Kültür Negatif Endokardit (KNE) KNE’in en sık nedeni daha önceki antibiyotik tedavisidir. Yavaş üreyen etkenlerden şüpheleniliyorsa (HACEK grubu, Abiotophia, Nocardia, Neisseria, Brucella gibi) inkübasyon uzun tutulmalıdır. Ayrıca KNE’de cerrahi ile çıkarılan tüm materyaller kültüre ve patolojik incelemeye gönderilmelidir (15,16). Bazı mikroorganizmalar için serolojik inceleme gereklidir. Bartonella, Legionella, Chlamydia ve Coxiella burnetti için serolojik inceleme önerilir. Özellikle C.burnetti için, faz I antijenine karşı oluşan IgG yapısındaki antikorlar tanıda önemlidir (1). KNE’de polimeraz zincir reaksiyonu (PCR) üremesi zor olan (T.whippelii gibi) ya da ölü olan bakterileri tanımada faydalı olabilir. PCR özellikle cerrahi ile çıkarılmış kapaklarda, kültürden daha duyarlıdır (17). 18 2.1.8. TEDAVİ 2.1.8.1. Antimikrobiyal Tedavi Septik tabloda olmayan hastalarda tedaviye kültürlerde üreme olduktan sonra başlanır. Tedavi sırasında, artık üreme olmayana kadar 24-48 saatte bir kan kültürü almaya devam edilir. Operasyon sonrasında tam doz ve süre antibiyotik tedavisi tekrarlanır. Antimikrobiyal tedavide kombine edilen ilaçların aynı zamanda verilmesi sinerjistik etkinin görülmesi için gereklidir (13). Penisiline yüksek düzeyde duyarlılığı olan viridans streptokoklar ve St.bovis’ te (MİK≤0.12 µg/mL) 4 haftalık penisilin ya da seftriaksonla ≥%98 kür sağlanır. Ampisilin penisiline alternatiftir. Gentamisin eklenmesi sinerjistik etkiyi sağlar. Bu grup hastalarda, komplikasyonun eşlik etmediği durumlarda, penisilin ya da seftriaksonun günde tek doz gentamisin ile kombinasyonunun 2 hafta süreyle verilmesi yeterli olabilir. Penisilin ya da seftriaksonu tolere edemeyen hastalarda vankomisin verilebilir (13) (Tablo 4). Penisiline relatif olarak dirençli olan viridans streptokoklar ve St.bovis’ te (MİK>0.12 µg/mL ve MİK≤0.5 µg/mL) 4 haftalık penisilin ya da seftriakson tedavisine ilk 2 hafta için günde tek doz gentamisin eklenir (Tablo 5). Abiotrophia defectiva ve Granulicatella türleri, Gemella türleri, ve penisiline dirençli viridans streptokoklar ve St.bovis’ e (MİK>0.5 µg/mL) bağlı gelişen endokarditin tedavisi daha zordur. Bunlar enterokokkal endokardit gibi tedavi edilirler (Tablo 10 ). Penisiline yüksek düzeyde duyarlılığı olan viridans streptokoklar ve St.bovis’in (MİK≤0.12 µg/mL) neden olduğu PKE’de, 6 hafta penisilin ya da seftriakson, gentamisinle birlikte ya da tek başına verilmelidir (Tablo 6). Penisiline rölatif olarak dirençli olan olgularda (MİK>0.12 µg/mL) ilk 2 hafta gentamisin eklenmelidir (Tablo 7). 19 Tablo 4- Penisiline yüksek düzeyde duyarlılığı (MİK≤0.12 µg/mL) olan viridans streptokoklar ve St.bovis’ e bağlı gelişen NKE’de tedavi tedavi İlaç I.Kristalize penisilinG* Doz ve Uygulama 12-18 milyon U/24 h i.v devamlı inf. Süre 4 hft veya 4-6 eşit dozda veya seftriakson II. Kristalize penisilinG¹ 2 g/24 h i.v/i.m tek dozda 4 hft 12-18 milyon U/24 h i.v devamlı inf. 2 hft veya 6 eşit dozda veya seftriakson 2 g/24 h i.v/i.m tek dozda 2 hft ve gentamisin 3 mg/kg/24 h iv/im tek dozda 2 hft III.Vankomisin² 30 mg/kg/24 h IV 2 eşit dozda 2g/24 h’i aşmayacak 4 hft *>65 yaş, renal fonksiyonları bozuk hastalarda tercih edilir. ¹Kardiyak, ekstrakardiyak apse ve komplikasyonu olmayan stabil hastalarda 2 haftalık rejim önerilebilir. ²Penisilini tolere edemeyen hastalarda Tablo 5- Penisiline rölatif olarak dirençli olan (MİK>0.12 µg/mL ve MİK≤0.5 µg/mL) viridans streptokoklar ve St.bovis ‘in neden olduğu NKE’de tedavi İlaç I.Kristalize penisilin G Doz ve Uygulama 24 milyon U/24 h i.v devamlı inf. Süre 4 hft veya 4-6 eşit dozda veya seftriakson 2 g/24 h i.v/i.m tek dozda 4 hft ve gentamisin 3 mg/kg/24 h iv/im tek dozda 2 hft II.Vankomisin* 30 mg/kg/24 h IV 2 eşit dozda 2g/24 h’i aşmayacak 4 hft *Penisilini tolere edemeyen hastalarda 20 Tablo 6. Penisiline yüksek düzeyde duyarlılığı olan (MİK≤0.12 µg/mL) viridans streptokoklar ve St.bovis’in neden olduğu PKE’de tedavi İlaç I.Kristalize penisilin G Doz ve Uygulama 24 milyon U/24 h i.v devamlı inf. Süre 6 hft veya 4-6 eşit dozda veya seftriakson 2 g/24 h i.v/i.m tek dozda 6 hft ve gentamisin 3 mg/kg/24 h iv/im tek dozda 2 hft (ya da sadece penisilin G veya seftriakson) II.Vankomisin* 30 mg/kg/24 h IV 2 eşit dozda 2g/24 h’i aşmayacak 6 hft *Penisilini tolere edemeyen hastalarda Tablo 7.Penisiline rölatif olarak dirençli olan (MİK>0.12 µg/mL) viridans streptokoklar ve St.bovis’in neden olduğu PKE’de tedavi İlaç I.Kristalize penisilin G Doz ve Uygulama 24 milyon U/24 h i.v devamlı inf. Süre 6 hft veya 4-6 eşit dozda veya seftriakson 2 g/24 h i.v/i.m tek dozda 6 hft ve gentamisin 3 mg/kg/24 h iv/im tek dozda 6 hft II.Vankomisin* 30 mg/kg/24 h IV 2 eşit dozda 2g/24 h’i aşmayacak *Penisilini tolere edemeyen hastalarda 21 6 hft Uyuşturucu madde bağımlılarında (UMB), oksasilin duyarlı S.aureus’ a (OSSA) bağlı gelişen sağ kalp endokarditinde, komplikasyon yok ise, 2 haftalık betalaktam ve aminoglikozid kombinasyonu ile tedavi yeterlidir. Bu hastalarda glikopeptidler ile yapılan tedavi daha az yeterlidir. OSSA’ a bağlı gelişen sol kalp endokardirlerinde 6 haftalık nafsilin tedavisinin yanına ilk 3-5 gün gentamisin eklenmelidir (Tablo 8). KNS’ın çoğunda ve giderek artan oranlarda S.aureus‘ ta oksasiline direnç gelişmektedir (ORSA). Bu hastalarda vankomisin kullanılmalıdır. Vankomisini tolere edemeyen hastalarda trimetoprim-sülfometoksazol, doksisiklin, minosiklin ya da linelozid denenebilir. Nativ kapak stafilokok endokarditinde rifampinin rutin kullanımı önerilmez. Vankomisine kısmen ya da tamamen duyarlı stafilokoklar için henüz optimal tedavi seçeneği yoktur. KNS’a bağlı PKE’de genelde oksasilin direnci mevcuttur. Bu hastalarda 6 hafta vankomisin ve rifampin ile 2 hafta gentamisin önerilir. S.aureus’a bağlı PKE’inde mortalite yüksektir ve muhakkak kombinasyon tedavisi önerilir. Bu hastalarda eğer etken OSSA ise nafsilin ya da oksasilin ile rifampin kombine edilir ve ilk 2 hafta gentamisin önerilir. Etken ORSA ise vankomisin ve rifampin kombine edilir ve yine ilk 2 hafta gentamisin eklenir. (Tablo 9) (13). Enterokoklara bağlı gelişen endokarditlerde rutin olarak penisilin ve vankomisin için invitro duyarlılık testleri (MİK belirlenmesi) ile gentamisin ve streptomisine yüksek düzeyde olan direnç testleri yapılmalıdır. Streptokoklar ile kıyaslandığında, enterokoklar penisilin, ampisilin ve gentamisine relatif olarak daha dirençlidirler. Bakterisidal etki için bu antibiyotikler gentamisin ve streptomisinle kombine edilmelidirler. Penisilin, vankomisin ve aminoglikozidlere duyarlı enterokoklar için, penisilin ya da ampisilin ile aminoglikozidler kombine edilir (Tablo 10). Gentamisin ve streptomisinden hangisine duyarlı ise o verilir ancak ikisine de duyarlı ise gentamisin tercih edilir. 3 aydan daha az süredir semptomu olan 22 Tablo 8. Prostetik materyal yokluğunda Stafilokoklara bağlı gelişen endokarditte tedavi İlaç Doz ve Uygulama Süre A.Oksasilin duyarlı ise I.Nafsilin ya da oksasilin¶ 12g/24 h iv 4-6 eşit dozda 6 hft ve gentamisin* 3 mg/kg iv 2-3 eşit dozda 3-5gün II.Sefazolin 6 g/24 h iv 3 eşit dozda 6 hft ve gentamisin* 3 mg/kg iv 2-3 eşit dozda 3-5gün 30 mg/kg/24 h iv 2 eşit dozda 6 hft B.Oksasiline dirençli ise I.Vankomisin ¶Penisiline duyarlı ise (MİK≤0.1 µg/mL) nafsilin/oksasilin yerine penisilin G 24 milyon U/24h kullanılabilir. *Gentamisin kullanımı tercihe bağlıdır, etkinliği kanıtlanmamıştır. Tablo 9. Prostetik materyal varlığında Stafilokoklara bağlı gelişen endokarditte tedavi İlaç Doz ve Uygulama Süre A.Oksasilin duyarlı ise I.Nafsilin ya da oksasilin¶ 12g/24 h iv 6 eşit dozda ≥6 hft ve rifampin 900 mg/24 h iv/po 3 eşit dozda ≥6 hft ve gentamisin 3 mg/kg iv 2-3 eşit dozda 2 hft I.Vankomisin 30 mg/kg/24 h iv 2 eşit dozda ≥6 hft ve rifampin 900 mg/24 h iv/po 3 eşit dozda ≥6 hft ve gentamisin 3 mg/kg iv 2-3 eşit dozda 2 hft B.Oksasiline dirençli ise ¶Penisiline duyarlı ise (MİK≤0.1 µg/mL) nafsilin/oksasilin yerine penisilin G 24 milyon U/24h kullanılabilir. 23 NKE’de tedavi 4 hafta, diğer NKE ve PKE’de 6 hafta olmalıdır. Penisilin, streptomisin ve vankomisine duyarlı ancak gentamisine dirençli enterokoklara bağlı gelişen endokarditlerde, aminoglikozid olarak streptomisin tercih edilir (Tablo 11). Penisiline dirençli ancak vankomisin ve aminoglikozidlere duyarlı enterokkal endokarditte, beta laktamaz üreten suşlarda ampisilinsulbaktam ve gentamisin, intrinsik penisilin direnci olanlarda vankomisin ve gentamisin kullanılması önerilir (Tablo 12). Penisilin, vankomisin ve aminoglikozidlere dirençli enterokokkal endokarditte, tedavi oldukça zorlaşır (Tablo 13). Enterokoklar MİK≤4 µg/mL ise vankomisine duyarlı, 8-16 µg/mL arasında ise orta düzeyde dirençli, MİK>16 µg/mL ise tam dirençli kabul edilir. Bu hastalarda linezolid, imipenem-silastatin +ampisilin veye seftriakson+ampisilin denenebilir. İnfeksiyon hastalıkları uzmanı ile konsültasyon planlanır. Öncelikli cerrahi de bu hastalardaki diğer bir seçenektir (13). Gram-negatif basillerden HACEK grubu (Haemophilus parainfluenzae, H aphrophilus, H paraphrophilus, H influenzae, Actinobacillus actinomycetemcomitans, Cardiobacterium hominis, Eikenella corrodens, Kingella kingae, ve K denitrificans) NKE’nin %5-10’ unu oluştururlar. Kültürlerde oldukça yavaş çoğalırlar ve uzun inkübe edilmeleri gerekebilir (18 ). HACEK grubu mikroorganizmalar eskiden ampisiline duyarlı iken artık betalaktamaz üreten suşları mevcuttur. Betalaktamaz üreten ve üretmeyen suşların her ikisi de seftriakson, ampisilin-sulbaktam ve florokinolonlara duyarlıdırlar (19) (Tablo 14). KNE’ de daha önceden antibiyotik alımı mevcutsa verilecek ampirik tedavi S.aureus, streptokoklar, enterokoklar ve HACEK grubuna yönelik olmalıdır. Bu gruba ampisilinsulbaktam ve gentamisin kombinasyonu verilebilir. KNE’den erken PKE’de ORSA’u kapsayacak şekilde vankomisin verilmelidir. Geç PKE’de etken genelde streptokoklar ya da OSSA’ tur (Tablo 15). 24 Tablo 10. Penisilin, vankomisin ve aminoglikozidlere duyarlı enterokokkal endokardit ve Abiotrophia defectiva, Granulicatella türleri, Gemella türleri ve penisiline dirençli viridans streptokoklar ve St.bovis’ e (MİK>0.5 µg/Ml) bağlı gelişen endokarditte tedavi İlaç Doz ve Uygulama Süre I.Ampisilin 12g/24 h iv 6 eşit dozda 4-6 hft veya kristalize penisilin G 18-30 milyon U/24 h i.v devamlı inf. 4-6 hft veya 6 eşit dozda ve gentamisin 3 mg/kg/24 h iv/im 3 eşit dozda 4-6 hft III.Vankomisin¶ 30 mg/kg/24 h IV 2 eşit dozda 6 hft 2g/24 h’i aşmayacak ve gentamisin 3 mg/kg/24 h iv/im 3 eşit dozda 6 hft ¶Penisilini tolere edemeyenlerde önerilir. Tablo 11. Penisilin, streptomisin ve vankomisine duyarlı ancak gentamisine dirençli enterokokkal endokarditte tedavi İlaç Doz ve Uygulama Süre I.Ampisilin 12g/24 h iv 6 eşit dozda 4-6 hft veya kristalize penisilin G 24 milyon U/24 h i.v devamlı inf. 4-6 hft veya 6 eşit dozda ve streptomisin 15 mg/kg/24 h iv/im 2 eşit dozda 4-6 hft III.Vankomisin¶ 30 mg/kg/24 h IV 2 eşit dozda 6 hft 2g/24 h’i aşmayacak ve streptomisin 15 mg/kg/24 h iv/im 2 eşit dozda ¶Penisilini tolere edemeyenlerde önerilir. 25 6 hft Tablo 12. Penisiline dirençli ancak vankomisin ve aminoglikozidlere duyarlı enterokkal endokarditte tedavi İlaç Doz ve Uygulama Süre Betalaktamaz üreten suşlarda I.Ampisilin 12g/24 h iv 4 eşit dozda 6 hft ve gentamisin 3 mg/kg/24 h iv/im 3 eşit dozda 6 hft II.Vankomisin 30 mg/kg/24 h IV 2 eşit dozda 6 hft (penisilin intoleransı varsa) 2g/24 h’i aşmayacak ve gentamisin 3 mg/kg/24 h iv/im 3 eşit dozda 6 hft 30 mg/kg/24 h IV 2 eşit dozda 6 hft İntrinsik penisilin direnci varsa I.Vankomisin 2g/24 h’i aşmayacak ve gentamisin 3 mg/kg/24 h iv/im 3 eşit dozda 6 hft Tablo 13. Penisilin, vankomisin ve aminoglikozidlere dirençli enterokoklara bağlı gelişen NKE veya PKE’de tedavi İlaç Doz ve Uygulama Süre E.faecium Linezolid 1200 mg/24 h iv/po 2 eşit dozda ≥8 hft 22.5 mg/kg/24 h iv 3 eşit dozda ≥8 hft İmipenem/cilastatin 2 g/24 h iv 4 eşit dozda ≥8 hft ve ampisilin 12 g/24 h iv 6 eşit dozda ≥8 hft Seftriakson 2 g/24 h iv/im tek doz ≥8 hft ve ampisilin 12 g/24 h iv 6 eşit dozda ≥8 hft veya Quinupristin-dalfopristin E.faecalis veya 26 Tablo 14. HACEK grubunun etken olduğu NKE ve PKE’de tedavi İlaç Doz ve Uygulama Süre* I.Seftriakson 2 g/24 h iv/im tek dozda 4 hft 12 g/24 h iv 4 eşit dozda 4 hft 1000 mg/24 h po veya 4 hft 800 mg/24 h iv 2 eşit dozda 4 hft veya II.Ampisilin-sulbaktam veya III.Siprofloksasin¶ ¶ Siprofloksasin, seftriakson ve ampisilin-sulbaktam’a intoleransı olanlarda verilir. *PKE’de tedavi süresi 6 haftadır. Fungal endokardit daha çok immünsuprese hastalarda ya da kalp içi prostetik materyali olan hastalarda gözlenir. Tedavideki gelişmelere rağmen mortalite oldukça yüksektir. Ensık etken candida türleridir, çoğunlukla kültürde ürer. İkinci neden olan aspergillus türleri ise daha çok yeni replase edilmiş protez kapaklarda endokardite yol açarlar ve genelde kültürde üremezler. Fungal endokarditte tedavi iki aşamalıdır: önce infeksiyonun kontrolü (amfoterisin B) daha sonra cerrahidir (20). 27 Tablo 15. Kültür negatif endokarditlerde tedavi (Bartonella endocarditis dahil) İlaç Doz ve Uygulama Süre I.Ampisilin 12g/24 h iv 4 eşit dozda 4-6 hft ve gentamisin 3 mg/kg/24 h iv/im 3 eşit dozda 4-6 hft II.Vankomisin 30 mg/kg/24 h IV 2 eşit dozda 4-6 hft (penisilin intoleransı varsa) 2g/24 h’i aşmayacak ve gentamisin 3 mg/kg/24 h iv/im 3 eşit dozda 4-6 hft ve siprofloksasin 1000 mg/24 h po veya 4-6 hft Nativ Kapak ve Geç PKE (>1 yıl) 800 mg/24 h iv 2 eşit dozda Erken PKE (<1 yıl) Vankomisin 30 mg/kg/24 h iv 2 eşit dozda 6 hft ve gentamisin 3 mg/kg iv 2-3 eşit dozda 2 hft ve sefepim 6 g/24 h iv 3 eşit dozda 6 hft ve rifampin 900 mg/24 h iv/po 3 eşit dozda 6 hft Şüpheli Bartonella Seftriakson 2 g/24 h i.v/i.m tek dozda 6 hft ve gentamisin 3 mg/kg/24 h iv/im 3 eşit dozda 2 hft ve doksisiklin 200 mg/kg/24 h iv/po 2 eşit dozda 6 hft (veya sadece seftriakson ve gentamisin) Dökümente edilmiş Bartonella Doksisiklin 200 mg/kg/24 h iv/po 2 eşit dozda 6 hft ve gentamisin 3 mg/kg/24 h iv/im 3 eşit dozda 2 hft 28 2.1.8.2. Cerrahi Tedavi Aktif endokardit vakalarının %30’unda cerrahi uygulanır. Kardiyak patolojiler belirginleşmeden cerrahi uygulandığında prognoz iyidir. Aktif endokardit sırasında cerrahi endikasyonlar: I. KY, cerrahi için en sık görülen endikasyondur. Akut aort yetersizliğine bağlı KY’de cerrahi acil gereklidir ve hayat kurtarıcıdır. Akut mitral yetersizliği için de erken cerrahi önerilir. II. 7-10 günlük uygun tedaviye rağmen persiste eden infeksiyon III. Perivalvüler yayılım olması (apse, psödoanevrizma, fistül, kapak perforasyonu) IV. Antimikrobiyal tedavi ile kontrol altına alınamayan dirençli mikroorganizmaların neden olduğu endokarditlerde de cerrahi önerilir (Mantarlar, brucella, coxiella, s.lugdunensis, vankomisin ve gentamisine yüksek derecede dirençli enterokoklar) V. 10 mm’den büyük, öz. mitral kapak anterior leaflet üzerinde mobil vejetasyon VI. Uygun antibiyotik tedavisi altında rekürren emboli VII. Erken PKE’de VIII. Hemodinamik olarak anlamlı protez kapak disfonksiyonlarında Perioperatif dönemde hastanın oral antikoagulanı kesilir ve heparine geçilir (1). 2.1.9. Komplikasyonlar 2.1.9.1. Kalp Yetersizliği İE’de KY kötü bir prognostik bulgudur. Daha çok aort kapak (%29’ unda), sonra sırasıyla mitral kapak (%20’sinde) ve triküspit kapak (%8’inde) infeksiyonları yol açar. KY, kapak perforasyonu (Resim 1), protez kapak ayrışması (Resim 2), mitral korda rüptürü, dev vejetasyona bağlı kapak obstrüksiyonu ve ani intrakardiyak şantlara bağlı akut olarak gelişebilir. Uygun antibiyotik tedavisine rağmen ilerleyici kapak yetersizliği ve sol ventrikül 29 Resim 1. Mitral kapak endokarditi olan hastamızın midözefajiyal (40º) TEE görüntüsü. Color flow Doppler ile mitral kapak anterior leaflet perforasyonu izlenmekte Resim 2. Mitral mekanik protez kapakta ayrışma nedeniyle acil operasyona alınan hastamızın operasyonla çıkarılan kapağı. Kapak üzerinde vejetasyonlar izlenmekte 30 disfonksiyonuna bağlı olarak ta KY gelişebilir. KY ile birlikte olan endokarditte olumsuz cerrahi sonuç belirleyicileri, NYHA fonksiyonel sınıf III-IV, renal yetersizlik ve ileri yaştır. Yine de endokardit sonucu gelişen KKY’de erken cerrahi olumlu sonuçları nedeniyle önerilir (13). 2.1.9.2.Embolik Olaylar İE hastalarının %22-50’inde sistemik embolizasyon gelişir. Emboli daha çok akciğer, koroner arterler, dalak, kemik ve ekstremiteleri ilgilendirir. Embolilerin %65’i SSS ile ilgilidir ve bunların da %90’ını orta serebral artere olanlar oluşturur (21). Embolik komplikasyonlar en sık S.aureus, Candida, HACEK, ve Abiotrophia’nın neden olduğu endokarditlerde gözlenir. Emboli riski antimikrobiyal tedavinin ilk 2 haftasında en fazladır, sonra giderek azalır. Ancak tedavi ile vejetasyon büyüyorsa emboli riski devam eder (22). Genellikle, mitral kapak üzerinde olan vejetasyonların, aort kapak üzerinde olanlara göre emboli riski daha fazladır. Mitral kapak anterior leaflet’te ise posterior leaflet’e göre risk daha fazladır. Özellikle 10 mm’nin üzerindeki mobil vejetasyonlarda emboli riski artmıştır. Bazı çalışmalarda streptokokkal endokarditte, bazılarında ise stafilokok ve mantar endokarditlerinde emboli riskinin artmış olduğu saptanmıştır (13). Emboliyi önlemede stafilokok endokarditinde intravenöz aspirinin faydası hayvan deneylerinde gösterilse de, insanlarda oral 325 mg aspirinin vejetasyon rezolüsyonu veya emboli üzerine etkisinin olmadığı saptanmıştır (23). Varfarin tedavisi altında olan hastalarda tanı konar konmaz standart heparin tedavisine geçilmelidir. Bir kez emboli olanlarda tekrarlama olasılığı 1 ay içinde % 50 dolaylarındadır. Beyin embolisi sonrası; eğer tomografik incelemede kanama eşlik etmiyorsa, kan-beyin bariyeri bozulmadan ilk 72 saatte kardiyak cerrahi uygulanmalıdır (1). 31 2.1.9.3. Perianüler Komplikasyonlar Perianüler komplikasyonlar, yüksek mortalite, daha fazla KY riski ve daha sık cerrahiye gidişle ilişkilidirler. NKE’de %10-40 oranında izlenir ve aort kapak tutulumu daha fazladır (Resim 3). PKE’inde bu oran oldukça fazladır. Hastaların %56-100’ünde perianüler tutulum izlenir (Resim 4). Perianüler apseler daha çok PKE’de olur. Persistan ateş, rekürren emboli, kalp bloğu, KY ve yeni patolojik üfürüm perianüler yayılımın klinik göstergeleri olabilir. EKG’de atriyovantriküler blok olmasının apse varlığını göstermedeki pozitif prediktif değeri %88’dir, ancak sensitivitesi düşüktür. Perivalvüler apseleri tanımada TTE ‘nin sensitivitesi %18-63 iken, TEE’nin sensitivitesi %76-100, spesifisitesi %95, pozitif prediktif değeri %87-89’dur. Perianüler komplikasyonların tedavisi cerrahidir. Özellikle aort kapak replasmanı için homogreftler tercih edilmelidir. Antibiyotik penetransının iyi olması nedeniyle endokardit relaps riski daha azdır (13). 2.1.9.4. Mikotik Anevrizmalar Mikotik anevrizmalar (MA) damar duvarındaki vaza vazorumlara septik embolilerin yerleşmesi sonrasında infeksiyonun damar duvarı boyunca içe ve dışa doğru yayılmasıyla gelişir. En sık serebral arterlerde gelişir. Rüptüre olmamış intrakraniyal MA’da mortalite %30 iken, rüptüre olmuş vakalarda %80’dir. Semptomu olmayan hastalarda rutin tarama önerilmez. Semptomu olan hastalarda kontrastlı tomografi ya da manyetik rezonans inceleme ile tespit edilebilir. Aydınlatılamayan olgularda serebral anjiyo ile kesin tanı konabilir. Distalde olan intrakraniyal MA’lar için antibiyotik tedavisi altında takip önerilirken, daha proksimalde olup büyüme eğilimi olanlar için cerrahi düşünülmelidir. Extrakraniyal MA’lar rüptüre olmaya daha eğilimlidirler ve tedavileri cerrahidir (24,25,26). 32 Resim 3. Üstteki resimde hastalarımızdan birinin TEE kısa aks (49º) görüntüsü. Biküspit aort kapak ve ince ekolüsen alan şeklinde izlenen aort kökü absesi Resim 4. Aortik mekanik protez kapak ve septalarla birçok poşa ayrılmış aort kökü absesi olan hastamızın TEE kısa aks (40º) görüntüsü 33 2.1.9.5. Akut Böbrek Yetersizliği PKE ve NKE’ de akut böbrek yetersizliği kötü bir prognostik göstergedir. Endokardit seyrinde akut böbrek yetersizliği sanıldığından da fazla oranda görülür. Bazı hastalarda endokarditin ilk bulgusu olabilir. İE seyrinde gözlenen böbrek yetersizliğinin sebepleri: • İmmün kompleks glomerülonefriti • Multi-organ yetersizliğinin bir parçası • Antibiyotiklere bağlı nefrotoksisite • Postoperatif böbrek yetersizliği • Embolilere bağlı böbrek infarktı • Tanı yöntemlerinde kullanılan kontrasta bağlı Akut infeksiyon sonrası hastalarda kalıcı nefropati nadir gözlenir. Postoperatif periyotta ve ciddi sepsis durumunda hemofiltrasyon faydalı olabilir (1). 2.1.10. Korunma İskemik kalp hastalığına bağlı valvüler lezyonlarda infektif endokardit açısından risk mevcudiyetini gösteren yeterli miktarda çalışma yoktur. Koroner arter cerrahisi ve perkütan koroner girişimler de bu kategori içinde değerlendirilirler. Yayınlanan serilerde sekundum tipi atriyal septal defekt (ASD), kapatılmış ventriküler septal defekt (VSD), izole pulmoner darlık (PD), Fontan ve Mustard operasyonları sonrası infektif endokardite rastlanmadığı vurgulanmasına rağmen, özellikle sekundum ASD’nin kateter ile kapatılmasından sonraki 1 yıllık periyodda antibiyoterapi önerilmektedir. Ekokardiyografinin rutin kullanımda daha sık uygulanmasının ardından sıklıkla karşılaşılan MVP’de; belirgin leaflet kalınlaşması olmadığı, yetersizliğin eşlik etmediği yada kalsifikasyonun izlenmediği durumlarda profilaksi gerekmez. Pacemaker ya da ICD implantasyonu da endokardit proflaksisi gerektirmeyen durumlar içinde yer alır (Tablo 16). 34 Ülkemizde RKH ensık gördüğümüz İE proflaksisi gerektiren kalp hastalığıdır. Yaşam süresinin uzadığı Avrupa ülkelerinde romatizmal kalp hastalığı yerini dejeneratif kapak hastalığına bırakmıştır. MVP’li hastalarda mitral yetersizliği, leaflet kalınlaşması (≥5 mm), kalsifikasyon, holosistolik üfürüm ve özellikle primer MVP ‘de olduğu gibi miksomatöz dejenerasyon eşlik ediyorsa; mutlaka antibiyotik proflaksisi uygulanmalıdır. Biküspit aort kapak ve aort koarktasyonu siyanotik olmayan KKH kategorisinde yer alır. Tıpkı PDA, VSD, sekundum ASD dışındaki ASD’ler gibi endokardit proflaksisi önerilmektedir. Bu hasta grubunda cerrahi ya da kateter tekniği ile düzeltme yapıldıktan sonra, eğer rezidüel lezyon yada şant gelişmez ise endokardit profilaksisi gerekliliği ortadan kalkar. Protez kapaklarda (biyoprotez ve homogreft kapaklar dahil ) endokardit riski doğal kapaklara göre 5-10 kat artış gösterir. Bu nedenle bu hasta profilinde mutlaka antibiyotik profilaksisi uygulanmalıdır. Hipertrofik kardiyomiyopati olgularında obstrüktif ya da nonobstrüktif olsun, MY ve sistolik öne hareket (SAM) eşlik ediyorsa endokardit riski belirgin şekilde artmaktadır (1) (Tablo-17). Tablo 16. İE proflaksisi önerilmeyen durumlar • İzole sekundum ASD • Cerrahi olarak düzeltilmiş ASD, VSD, PDA olguları (6. aydan sonra rezidüel şant yoksa) • Koroner arter by-pass cerrahisi • Mitral valv prolapsusu (mitral yetersizliği veya leaflet kalınlaşmasının eşlik etmediği olgular) • Fizyolojik veya fonksiyonel veya masum üfürümler • Kapak sekeli olmayan geçirilmiş akut romatizmal ateş ve Kawasaki hast. • Pacemaker ,ICD ve stent implantasyonu 35 Tablo 17. İE proflaksisi önerilen durumlar I )Yüksek riskli kalp hastalıkları • Protez kapaklar (biyoprotez ve homogreft protez dahil) • Geçirilmiş bakteriyel endokardit hikayesi • Kompleks konjenital siyanotik kalp hastalıkları (Tek ventrikül fizyolojisi, büyük arter transpozisyonu, Fallot tetralojisi vs…) • Cerrahi olarak uygulanan sistemik-pulmoner şant ve conduit’ler II) Orta riskli kalp hastalıkları • Sekundum ASD dışında siyanotik olmayan konjenital kalp hastalıkları (VSD,PDA vs.) • Sonradan edinilmiş kapak hastalıkları (Romatizmal kapak hastalıkları, dejeneratif kapak hastalıkları) • Hipertrofik obstrüktif ya da nonobstrüktif kardiyomiyopati • Mitral valv prolapsusu (mitral yetersizliği ve/veya leaflet kalınlaşması) 2.1.10.1. Endokardit Riski Taşıyan Girişimler Gerek tanısal, gerekse terapötik girişimler bakteriyemi riski taşırlar. Bu risk dağılımı orofarinks girişimlerinde en yüksek, genitoüriner sistem girişimlerinde orta düzeyde iken gastrointestinel sistem girişimlerinde en alt düzeydedir (1). Endokardit açısından risk taşıyan dental girişimler ve profilaksi önerileri Tablo 18’de gösterilmiştir. 36 Tablo 18. Dental girişimler ve endokardit proflaksisi I.Endokardit profilaksisi önerilen girişimler • Diş çekimi • Periyodontal cerrahi girişimleri • Dental implantasyon • Endodontik kanal tedavisi ve apeks cerrahisi • Subgingival antibiyotik fibril yada strip uygulaması • Ligament içi lokal anestetik madde enjeksiyonu • Kanama riski olan diş temizleme işlemi II.Endokardit profilaksisi önerilmeyen girişimler • Operatif yada prostodontik diş restorasyonu • Ligament dışı lokal anestetik madde enjeksiyonu • Postoperatif sütür alımı • Çıkarılabilir prostodontik veya endodontik araç uygulaması • Florid tedavisi • Oral radyogram çekimi • Diş kaplama Endokardit açısından risk taşıyan genitoüriner, gastrointestinal ve solunum yolu girişimleri ve profilaksi önerileri Tablo 19’da gösterilmiştir. 37 Tablo 19. Gastrointestinal, genitoüriner, solunum sistemi girişimlerinde İE proflaksisi gerektiren ve gerektirmeyen durumlar I.Endokardit profilaksisi önerilen girişimler Solunum sistemi • Tonsillektomi ve/veya adenoidektomi • Solunum sistemi mukozasını ilgilendiren cerrahi girişimler • Rijid bronkoskop ile uygulanan bronkoskopi işlemi ve biyopsi Gastrointestinal sistem • Özefagus varisleri skleroterapisi işlemi • Özefagus striktür dilatasyonu • Endoskopik retrograd kolanjiyografi • Safra yolları cerrahisi • İntestinal mukozayı ilgilendiren cerrahi prosedürler Genitoüriner sistem • Prostat cerrahisi • Sistoskop • Üretra dilatasyonu II.Endokardit profilaksisi önerilmeyen girişimler Solunum sistemi • Endotrakeal entübasyon • Esnek bronkoskop ile uygulanan bronkoskopi işlemi ve biyopsi Gastrointestinal sistem • Transözefajiyal ekokardiyografi • Endoskopi ve biyopsi • Timpanastomi ve tüp implantasyonu 38 Tablo 19. Devam’ı Genitoüriner sistem • Vaginal histerektomi • Vaginal doğum • Sezeryan ile doğum • Üretral kateterizasyon • Dilatasyon ve küretaj • Terapötik abortus • Sterilizasyon prosedürleri • Rahim içi araç uygulaması • Sünnet Diğerleri • Kardiyak kateterizasyon ve PTCA • Pace-maker ,ICD ve stent implantasyonu • Deri insizyonu ve biyopsi 2.1.10.2. Antibiyotik Proflaksisi Sadece yüksek ve orta riskli hastalara antibiyotik proflaksisi önerilir. Antibiyotik profilaksisinde amaçlanan; dental, oral, solunum sistemi ve özefagus girişimlerinde viridans streptokoklara ve HACEK grubu mikroorganizmalara karşı, gastrointestinal ve genitoüriner girişimlerde ise enterokoklar, St. bovis ve enterobakter ailesine karşı savunmadır (27). Proflaktik antibiyotik rejimleri, dental, oral, solunum sistemi, gastrointestinal ve genitoüriner sistem ile ilgili girişimlerde, altta yatan kardiyak hastalığın getirdiği risk göz önünde bulundurularak düzenlenmiştir. Kesin kanıtlanmış etkinliği gösterilmemiş olsa da tüm hastalara antibiyotik proflaksisi önerilir (Tablo 20). 39 Tablo 20. Antibiyotik proflaksisi I.Dental, oral, solunum sistemi ve özefagus girişimlerinde proflaksi Klinik durum Antibiyotik Doz Standart proflaksi Amoksisilin 2 g PO, girişimden 1saat önce Oral alamayanlarda Ampisilin 2 gr i.v/i.m. girişimden 30 dk önce Penisilin alerjisi varsa Klindamisin veya 600 mg PO, girişimden 1 saat önce Sefaleksin/Sefadroksil veya 2 g PO, girişimden 1 saat önce Azitromisin/Klaritromisin 500 mg PO, girişimden 1 saat önce II.Genitoüriner ve alt gastrointestinal sistem girişimlerinde proflaksi Klinik durum Antibiyotik Doz Yüksek riskli hastalarda Ampisilin 2 g i.m/i.v ve gentamisin 1.5 mg/kg i.v/i.m¶ takiben girişimden 30 dk önce Ampisilin girişimden 6 saat sonra Yüksek riskli, penisilin Vankomisin 1 g i.v 1-2 saat süreli allerjisi olan hastalarda ve gentamisin 1.5 mg/kg i.v/i.m¶ g’den 30 dk önce bitmeli Orta riskli hastalarda Amoksisilin veya 2 g PO, girişimden 1saat önce Ampisilin 2 gr i.v/i.m. girişimden 30 dk önce Vankomisin 1-2 saat süreli, girişimden 30 dk önce bitmeli Orta riskli, penisilin alerjisi olan hastalarda ¶ Gentamisin dozu 120 mg’ı aşmamalıdır. 40 2.2. B-TIP NATRIURETİK PEPTİD Nörohormonların plazma seviyeleri kardiyovasküler prognoz ve tedaviye yanıtı değerlendirmede önemlidir. B-tip natriüretik peptid ya da brain natriüretik peptid (BNP) primer olarak ventriküllerde depolanan, basınç ve volüm yüklenmesine ve hasarlanmaya yanıt olarak salgılanan 32 aminoasitlik bir nörohormondur. Natriüretik ve vazodilatatör etkilere sahiptir. Atılımı yüksek oranda böbrekler ve karaciğerden gerçekleşir. Miyokard kitlesi göz önüne alındığında dominant olarak sol ventrikülden salınmaktadır. Sol ventrikül sistolik ve diyastolik disfonksiyonunda, akut koroner sendromlarda, kapak hastalıklarında, pulmoner embolide ve KKH’da plazma BNP düzeyleri yükselmektedir. KY’nin teşhisinde, tedavi stratejisinin belirlenmesinde, tedaviye yanıtın değerlendirilmesinde, mortalite ve morbiditeyi belirlemesinde önemlidir. Yine akut koroner sendromlarda yüksek riskli hasta grubunun belirlenmesinde, miyokard infarktüsü sonrası dönemde prognostik marker olarak önemlidir. Dekompanse KY’nin tedavisinde kullanılan infüzyon şeklindeki preperatları ise pulmoner kapiller saplama basıncında ve sol ventrikül end-diyastolik basıncında azalma, kardiyak outputta artış oluşturarak semptomatik düzelme sağlamaktadır ancak yaşam beklentisini artırdığı ispat edilmemiştir. Konu üzerindeki araştırmalar devam etmektedir (28). ProBNP’nin aminoterminal bölgesinin 76 aminoasitlik kalıntısı NT-proBNP yakın zamanda tespit edilmiş ve kardiyak bozulma sonucu plazma seviyelerindeki artış gösterilmiştir. Normal hastalarda plazma seviyeleri BNP ile benzerken, kardiyak bozulma sonunda NT-proBNP seviyeleri BNP’ye göre daha hızlı ve daha yüksek miktarda artmaktadır. BNP ye oranla daha yüksek stabilite ve daha uzun yarılanma ömrüne sahip olması nedeniyle daha spesifik bir marker olarak düşünülmektedir. Yapılan çalışmalarda BNP gibi NTproBNP’nin de ventriküler volüm ve basınç yüklenmesinin ve ventrikülün özellikle iskemik hasarlanmasının kuvvetli bir prediktörü olduğu ortaya konulmuştur. Günümüzde biventriküler 41 volüm ve basınç yüklenmesinin ve ventriküler hasarlanmanın teşhisinde, tedavi planlanmasında, tedavi takibinde, yüksek riskli grupların belirlenmesinde ve mortalite ve morbiditenin öngörülmesinde yardımcı bir biyokimyasal parametre olarak kullanılmaktadır (28, 29). Ayrıca BNP ve NT-proBNP’ nin ciddi sepsis ve septik şokta arttığı gösterilmiştir. Bu hastalarda sol ventrikül disfonksiyonu olsun olmasın, natriüretik peptidlerin prognostik öneminin olduğu da kanıtlanmıştır (30,31,32,33). 42 3.GİRİŞ VE AMAÇ Tüm medikal, cerrahi ve yoğun bakım olanaklarındaki ilerlemelere rağmen, İE hala hastane içi mortalitesi yüksek bir hastalıktır (yaklaşık olarak %20) (34,35). Ölüm ve komplikasyonlar açısından yüksek riskli hastaların belirlenmesi, hastalığın klinik sonlanımının daha iyi olmasına yol açacaktır (36). İE’te tanı koymak ve prognozu saptamak oldukça zordur. Prognozu belirlemek için, birçok klinik ve ekokardiyografik parametreler değerlendirilmiştir ancak çelişkili sonuçlar alınmıştır. Bunun nedeni ise, çeşitli tanı kriterlerinin oluşu, hastalığın heterojen karakteri, İE çalışmalarının az sayıda hasta ile ve çoğunlukla retrospektif olarak yapılmasıdır (36). Artmış natriüretik peptid düzeyleri; KY, miyokard infarktüsü ve septik şok gibi hastalıklarda kalp disfonksiyonu ve ölümün öngörücüsüdür (30,37-40) BNP sol ventrikül gerilmesi ve diyastol sonu basınç ya da hacim artışı sonucu ventrikülden salınır (28). NTproBNP düzeyinin septik şokta belirgin olarak arttığı saptanmıştır. Bu artışın nedeni olarak sepsisin uyardığı ventriküler dilatasyon gösterilmiştir (31). NT-proBNP, İE’li hastalarda sürekli bakteriyemi ve KY nedeniyle yükselebilir. Bu çalışmanın amacı bu biyokimyasal belirtecin İE’li hastalardaki prognostik değerinin belirlenmesidir. 4.METODLAR 4.1.Hasta grubunun özellikleri Mayıs 2004 ve Mayıs 2005 tarihleri arasında hastanemize İE şüphesi ile başvuran 235 hasta değerlendirildi. Bu hastalardan 52 tanesine modifiye Duke kriterlerine (41) göre kesin İE tanısı kondu. Pacemaker ve sağ kalp endokarditi olan 10 hasta çalışma dışı bırakıldıktan sonra sol kalp endokarditi tanısı konan 42 hasta, çalışmaya prospektif olarak dahil edildi. Her hasta için; yaş, cinsiyet, predipozan kalp hastalığı, infeksiyonun lokalizasyonu, endokarditin tipi, tutulan kapak, sebep olan mikroorganizma, ekokardiyografik bulgular, kalple ilgili ya da 43 kalp dışı komplikasyonlar, verilen tedavi, uygulanan cerrahi girişimler ve ölüm kaydedildi. Tüm hastalardan yazılı olarak aydınlatılmış onam alındı ve bu çalışma hastanemizin etik komitesi tarafından uygun görüldü. 4.2.Ekokardiyografik inceleme Tüm hastalara standart TTE uygulandı. Klinik endikasyonlar dahilinde 27 hastaya (%65) TEE uygulandı. Tüm ekokardiyografik incelemeler hastaneye yatışın ilk 3 günü içinde yapıldı. Tüm ekokardiyografik incelemeler, Wingmed Vivid System 5 cihazında, ‘phasedarrey dublex’ multifrekans transduser kullanılarak yapıldı. Doppler incelemelerde 2.5 MHz, doku görüntülemede ise 2.5-3.5 MHz problar ve ‘second harmonic’ görüntüleme, TEE için ise 5MHz problar kullanıldı. İki boyutlu görüntülemede standart parasternal uzun ve kısa eksen ve apikal 4 ve 2 boşluk pencereler kullanıldı. İki boyutlu ve M-mode inceleme ile sol ventrikül sistolik ve diyastolik çapları, sol ventrikül ejeksiyon fraksiyonu (Teicholtz metodu ile), sağ ventrikül sistolik ve diyastolik çapları ve sol atriyum çapı standart kriterlere göre ölçüldü. Vejetasyon, apse, yeni dehisens (ayrışma) ve yeni ciddi kapak yetersizliği değerlendirildi. Vejetasyon, kapak ya da miyokardiyal yüzeylere tutunan, düzensiz şekilli ve hareketli kitle şeklinde tarif edildi. Abse, valvüler infeksiyon varlığında, valvüler anulus ya da perivalvüler dokuda izlenen anormal ekolüsen alan olarak tarif edildi (42). Prostetik kapak ayrışması (dehisens), prostetik kapağın en az tek yönde, 15º den daha fazla sallanma hareketi olmasıyla belirlendi (43). Kapak yetersizlikleri semikantitatif olarak değerlendirildi. Valvüler perforasyon, kommissürler dışındaki leaflet doku devamlılığında bozulma (44) ve renkli akım Doppler’de mitral kapak için sistolde, aort kapak için diyastolde izlenen, leaflet dokusunun içinden geçen, yüksek hızlı, ekzantrik jet olarak tarif edildi (45). 44 4.3.Kan kültürleri Her hastadan, her seferinde farklı bir venden, en az 1 saat ara ile en az 3 set (aerob ve anaerob) kan kültürü alındı. Hastanın ateşi 38 ºC’nin üzerinde ise ek kan kültürleri alındı. Gereken hastalardan spesifik serolojik testler için özel örnekler alındı ve gereken hastalarda operasyonda çıkarılan kapak ve diğer örnekler patolojik ve mikrobiyolojik inceleme için kullanıldı. 4.4.Medikal ve cerrahi tedavi Kan kültürleri alındıktan sonra genel durumu kötü olan hastalara hemen, diğer hastalara ise kültürde üreme olduktan sonra antimikrobiyal tedavi başlandı. Hastalara, kültürde üreyen mikroorganizma ve yapılan antibiyogram duyarlılık testlerine uygun antibiyotik verildi. Aktif fazda erken cerrahi endikasyonları kılavuzlara uygun olarak belirlendi (1). Erken cerrahi, uygun doz ve sürede uygulanan antimikrobiyal tedavi bitmeden uygulanan cerrahi olarak tarif edildi. 4.5. Nt-proBNP ölçümü Hastalardan, ekokardiyografik incelemeden sonra, 20 dakikalık istirahat periyodunu takiben, Nt-proBNP ölçümü için kan örnekleri alındı (EDTA’lı tüplere antekübital venden 10 mL). Tüm örnekler antibiyotik tedavisine başlamadan ve cerrahi öncesi elde edildi. Örnekler, +4 oC’de 1500 rpm’de 5 dakika santrifüj edildi ve elde edilen üst faz plazma örnekleri ölçüm zamanına kadar –20 oC de saklandı. Nt-proBNP analizleri Elecsys Roche Diagnostics ticari kitleri kullanılarak yapıldı. 4.6.Klinik sonlanım Klinik sonlanım olarak, erken cerrahi ve hastane içi ölümden oluşan bileşik sonlanım noktası saptandı. Cerrahi sonrası hastanede ölen hastalar için sonlanım, ölüm olarak belirlendi. 45 4.7.İstatistiksel analiz Tüm bulgular SPSS 11.5 istatistik programı ile analiz edildi. Devamlı değişkenler ortalama±standart sapma olarak belirtildi. NT-proBNP seviyeleri normal dağılım göstermediğinden, analiz için logaritmik değerleri kullanıldı. Devamlı değişkenleri kıyaslamak için, Student-t ya da Mann-Whitney U testi, kategorik değişkenler için Chi-square ya da Fisher’s exact test kullanıldı. p<0.05 değeri istatistiksel olarak anlamlı kabul edildi. Sürekli değişkenlerin korelasyonunu belirlemede Spearman ve Pearson bağıntı analizleri kullanıldı. Klinik, ekokardiyografik ve hormonal parametrelerden, klinik sonlanımın bağımsız belirleyicisini araştırmak için, ünivaryant ve multivaryant stepwise Cox proportional hazard regresyon analizi kullanıldı. Log Nt-proBNP’nin olumsuz klinik olayları belirlemedeki yeterliliği, ROC analizi ile değerlendirildi. Spesifisite ve sensitivitenin optimal değerlerini belirlemek için, ROC eğrisindeki en iyi spesifisite ve sensitivite noktasına en yakın değer tespit edildi. Log Nt-proBNP seviyeleri bu değerin üzerinde ve altında olan grupların olaysız sağkalım oranlarını karşılaştırmak için Kaplan-Meier sağkalım analizi yapıldı. 5.BULGULAR Klinik sonlanım olan ve olmayan 2 grubun özellikleri tablo 21’de (sayfa 47) özetlenmiştir. 42 hastadan, 33’ü erkek (%78), 9’u kadın idi (%22) ve yaşları 9 ile 75 arasında değişmekteydi (ortanca yaş:44). Hastaların 34’ünde NKE, 8’inde PKE mevcut idi. Tutulan kapaklar sırasıyla, aort (20 hasta), mitral (15 hasta) ve aort ile birlikte mitral kapak (7 hasta) şeklinde saptandı. Altta yatan kalp hastalıkları; 11 (%26) hastada biküspit aort kapak, 8 (%19) hastada romatizmal kapak hastalığı, 8 (%19) hastada dejeneratif kapak hastalığı, 8 (%19) hastada mekanik protez kapak, 1 (%2) hastada ventriküler septal defekt, 1 (%2) hastada mitral kapak prolapsusu ve 1 (%2) hastada obstrüktif hipertrofik kardiyomiyopati olarak saptandı. 4 hastada kardiyak anomali saptanmadı. Uyuşturucu madde bağımlılığı olan ve daha önce endokardit geçiren hasta yoktu. 46 Tablo 21. Klinik sonlanım (KS) açısından hastaların bazal klinik ve laboratuvar özelliklerinin karşılaştırılması KS (+) (n=32) KS (-) (n=10) p Klinik özellikler Yaş (yıl) 45.8 (±14.3) Erkek cinsiyet 25 (%78) 8 (%80) AD NYHA fonksiyonel sınıf Ortalama 2.88 (±0.94) 1.6 (±0.84) 0.001 22 (%69) 2 (%20) 0.01 S.aureus infeksiyonu 8 (%19) 1 (%10) AD Atriyal fibrilasyon 11 (%34) 1 (%10) AD Başka merkezden transfer 24 (%75) 8 (%80) AD Tutulan kapak Aort 14 (%44) 6 (%60) AD Mitral 12 (%37) 3 (%30) AD Aort+Mitral 6 (%19) 1 (%10) AD Sol ventrikül EF, % 62.4±13.2 66.3±10.4 AD Sol atriyum çapı, mm 50.9±10.9 37.6±8.9 0.001 Ciddi kapak yetersizliği 24 (%86) 4 (%40) 0.05 Kreatinin, mg/dL 1.67±1.4 0.98±0.5 0.05 Log Nt-proBNP 9.1±1.3 6.4±1.5 0.0001 Albümin, mg/dL 3.1±0.5 3.4±0.7 AD CRP, mg/L 15.7±19.4 10.4±10.6 AD ESR, mm/h 66.1±39.9 69.8±41.7 AD Lökosit, x10³/µL 13.2±8.6 11±3.3 AD Hemoglobin, gr/dL 10.5±2.01 10.7±2.9 AD Sınıf III-IV 42.5 (±23.2) AD Ekokardiyografik bulgular Laboratuvar bulguları NYHA, New York Heart Association; CRP, C-reaktif protein; ESR, eritrosit sedimantasyon hızı; AD, anlamlı değil; EF, ejeksiyon fraksiyonu 47 5.1.Ekokardiyografik bulgular TTE ve TEE ile hastaların hepsinde vejetasyon tespit edildi. Hastaların 8’inde (%19) apse ya da psödoanevrizma, 3’ünde (%7) protez kapak ayrışması, 13’ünde (%31) kapak perforasyonu, 2’sinde (%5) korda rüptürü saptandı. İleri valvüler yetersizlik 28 hastada (%66) mevcut idi (14 hastada ileri aort yetersizliği, 10 hastada ileri mitral yetersizliği ve 4 hastada ikisi birden). 5.2.Mikrobiyolojik özellikler Endokardite neden olan mikroorganizma olarak, streptococcus viridans (%19), diğer streptokoklar (%7), staphylococcus aureus (%21), koagülaz negatif stafilokoklar (%2), enterokoklar (%7), brucella (%5), gram negatif basiller (%5). 14 (%33) hastada mikrobiyolojik etken tanımlanamadı. Bu hastalardan %71’i başvuru sırasında antibiyotik almaktaydı. 5.3.Cerrahi tedavi 42 hastadan 29’una (%69) erken cerrahi uygulandı (0-30. günler arasında, ortanca 6.gün). Sadece bir hasta cerrahi tedaviyi reddetti ve 28. günde protez kapak ayrışması nedeniyle öldü. 29 hastadan, 7’sine (%24) başvurunun ilk 24 saati içinde, 12’sine (%41) 1 ve 7. günler arasında, 10 hastaya ise (%35) 7-30. günler arasında cerrahi uygulandı. Erken cerrahi endikasyonları ise; 16 hastada (%55) ileri kapak yetersizliği, 5 hastada (%17) emboli eşlik etsin etmesin büyük (>10 mm) ve mobil vejetasyon, 5 hastada apse (%17) ve 3 hastada (%11) protez kapak ayrışması ya da ileri paravalvüler kaçak idi. 5.4.Klinik olaylar ve mortalite 9 (%22) hastada hastane içi ölüm gerçekleşti (4-50. günler arasında, ortanca 26.gün). Bu hastalardan 3 tanesine cerrahi tedavi uygulanmadı (1 hasta cerrahi tedaviyi reddetti, 2 hasta ise ciddi ek hastalıklar nedeniyle opere edilmedi). Cerrahi uygulanan 29 hastadan 48 6’sında ölüm gözlendi. Tüm ölüm nedenleri; 3 hastada kalp yetersizliği, 2 hastada septik şok, bir hastada multiorgan disfonksiyonu, 1 hastada postoperatif hemorajik şok, 1 hastada serebral hemoraji ve 1 hastada akut böbrek yetersizliği olarak saptandı. 5.5.NT-proBNP ile klinik ve ekokardiyografik parametreler arasındaki ilişki Bazal NT-proBNP düzeyleri 153 ile 119470 pg/mL arasında saptandı (ortanca değeri 4460 pg/mL, ortalama değeri 16542±28166). NT-proBNP düzeylerinin semptomatik durum ile çok iyi korelasyon gösterdiği izlendi (p<0.0001, R=0.60). NT-proBNP değerleri, NYHA sınıf I hastalarda 2005±3075 pg/mL, sınıf II hastalarda 7808±16220 pg/mL, sınıf III hastalarda 21616±30586 pg/mL, ve sınıf IV hastalarda 31354±39209 pg/mL olarak belirlendi (p<0.001). NT-proBNP düzeyleri ile sol atriyum çapı (p<0.003, R=0.46), mitral yetersizliği (p<0.006, R=0.41), triküspit yetersizliği (p=0.014, r=0.37) ve kreatinin düzeyleri (p<0.01, r=0.39) arasında da anlamlı korelasyon saptandı. Yaş, ejeksiyon fraksiyonu (EF), aort yetersizliği, CRP ve lökosit sayısı ile ilişki izlenmedi. 5.6.Klinik sonlanımın prediktörleri Klinik sonlanımın prediktörlerini saptamak için yapılan ünivaryant ve multivaryant Cox proportional hazard regresyon analizlerinin sonuçları Tablo 22’te (sayfa 50) gösterilmektedir. Ünivaryant analizde, log Nt-proBNP, NYHA fonksiyonel sınıf III-IV semptomatoloji, sol atriyum çapı ve ciddi kapak yetersizliği, erken cerrahi ve ölüm ile ilişkili bulundu. Multivaryant analize, ünivaryant analizde anlamlı çıkan parametrelerin yanı sıra kreatinin düzeyleri de dahil edildi. Multivaryant analizde ise, log Nt-proBNP (HR=1.54 [95% CI: 1.2-1.9], p<0.001) klinik sonlanımın tek bağımsız prediktörü olarak bulundu. Diğer klinik ve biyolojik faktörlerden, CRP, lökosit sayısı, hemoglobin ve albumin düzeylerinin prognoz ile ilişkisi saptanmadı. Log Nt-proBNP’nin klinik sonlanımı belirlemedeki yeterliliği 49 Tablo 22. Klinik sonlanımın belirlenmesinde ünivaryant ve multivaryant analizler Ünivaryant p Multivaryant HR (95% CI) χ2 p HR (95% CI) χ2 Log Nt-proBNP 0.001 1.5 (1.2-1.9) 14 0.001 1.54 (1.2-1.9) 13.9 NYHA sınıf III-IV 0.002 3.3 (1.5-7.03) 9.3 … … … Sol atriyum çapı 0.02 1.4 (1.1-1.8) 5.9 … … … Kreatinin 0.1 1.2 (0.96-1.49) 2.8 … … … Ciddi kapak yetersizliği 0.04 2.4 (1.06-5.3) 4.4 … … … NYHA,New York Heart Association 50 ROC analizi ile değerlendirildi. Spesifisite ve sensitivitenin optimal değerlerini belirlemek için, ROC eğrisindeki en iyi spesifisite ve sensitivite noktasına en yakın değer tespit edildi. Log NT- proBNP’nin en yüksek sensitivite (%94) ve spesifisite (%72) gösterdiği değer 7.3 ve bunun pg/mL cinsinden karşılığı 1500 olarak bulundu. Eğri altında kalan alan ise (EAA) 0.76 olarak saptandı (Figür 1, sayfa 52). Plazma NT pro-BNP seviyeleri 1500 pg/mL’nin üzerinde ve altında olan hastaların olaysız sağkalım oranlarını pg/mL karşılaştırmak için KaplanNT-proBNP=1500 NT-proBNP=1500 pg/mL Meier sağkalım analizi yapıldı. Olaysız sağkalım oranının, NT-proBNP plazma seviyeleri 1500 pg/mL’nin altında olan hastalarda anlamlı olarak daha yüksek olduğu tespit edildi (Figür 2, sayfa 53). ROC Curve 1,00 ,75 ,50 EAA = 0.76 (95% CI, 0.56-0.97) Sensitivity ,25 Sensitivite 0,00 0,00 ,25 ,50 ,75 1,00 Spesifisite 1 - Specificity Figür 1. Log NT-proBNP’nin klinik sonlanımı belirlemedeki değerini gösteren ROC analizi 51 2345 01D E N ,0 T02468 v a - e y p n s r o t B F N r P e <>e 1 S 5 u 0 r0 v p i g v / a m l l Olaysız Sağkalım Günler Figür 2. NT-proBNP değeri 1500 pg/mL altında ve üstünde kalan İE’li hastaların, olaysız sağkalım oranlarının karşılaştırıldığı Kaplan-Meier eğrisi 52 6.TARTIŞMA Çalışmamızda NT-proBNP’nin İE’li hastalarda risk değerlendirmesinde değerli bir laboratuvar belirteci olabileceğini gösterdik. Sonuçlarımıza göre yüksek riskli sol kalp endokarditi olan hastalarda NT-proBNP seviyeleri anlamlı olarak daha yüksek bulundu. Erken cerrahi uygulanan ya da hastane içi ölüm gözlenen hastaların NT-proBNP düzeyleri, komplike olmayan sol kalp endokarditli hastalara nazaran anlamlı olarak daha yüksek idi. Ayrıca daha önce yapılmış çalışmalarda kalp yetersizliği hastalarında saptandığı gibi, NTproBNP düzeyleri ile semptomlar arasında kuvvetli ilişki gözledik. Daha önce yapılmış çalışmalarda CRP, prokalsitonin (PCT), albümin, kreatinin ve lökosit sayısı gibi birçok laboratuvar belirteci İE’li hastalarda prognostik parametre olarak önerilmiştir. Bir çok araştırma CRP’ye yönelik yapılmıştır (46,47). Bir çalışmada antimikrobiyal tedavi ile CRP düzeylerindeki gerilemenin iyi klinik sonlanımın belirleyicisi olduğu gösterilmiştir. Lökositozun da klinik değerlendirme de önemi gösterilmiştir ancak eritrosit sedimantasyon hızının prognostik değeri saptanmamıştır (48). Birçok çalışmada sistemik bakteriyel infeksiyonları diğer infeksiyonlardan ayırmada PCT’nin CRP’den daha iyi olduğu gösterilmiş (49), hatta İE’li hastalar üzerinde yapılmış bir araştırmada medikal tedaviye olan yanıtı değerlendirmede ve erken cerrahiye gidecek hastaları belirleme de PCT’nin oldukça faydalı olduğu bulunmuştur (50). Ancak bu inflamasyon belirteçlerinin İE’li hastalardaki prognostik rolü rutin klinik kullanımla kendini göstermemiştir. NT-proBNP, İE için yeni bir prognostik biyomarker olabilir. Sol kalp endokarditi olan hastalardaki belirgin NT-proBNP artışından birçok faktör sorumlu olabilir: 1. Yeni ciddi kapak yetersizliği akut kalp yetersizliğine yol açabilir, bu da sol ventrikül doluş basıncının yükselmesine ve sol ventrikül duvar gerilmesine yol açar. NTproBNP yükselmesinin nedeni bu olabileceği gibi önceden var olan kalp yetersizliğinin kötüleşmesi de olabilir. Çalışmamızda, beklediğimiz gibi NT-proBNP seviyelerinin 53 sol atriyum çapı, mitral yetersizliği ve triküspit yetersizliği ile korelasyonunu saptadık ancak EF ve aort yetersizliği ile ilşki gözlemedik. Bu bulgu ile İE’li hastalarda NT-proBNP salınımının tek nedeni düşük EF olamayacağını gösterdik. 2. Natriüretik peptidlerin ciddi sepsis ve septik şokta anlamlı olarak yükseldiğini (30,31,32) biliyoruz, dahası NT-proBNP’nin ciddi sepsiste ölümün belirleyicisi olduğu gösterilmiştir (32). NT-proBNP’nin artışı, sepsisin neden olduğu sol ventrikül genişlemesine ikincil olabilir. Septik şokta biventriküler dilatasyon ve azalmış kontraktilite ile karakterize miyokardiyal depresyon olabilir. Bunun muhtemel nedeni septik şok sırasında salınan kardiyodepresan faktörlerdir (tümör nekroze edici faktör ve interlökin 1β) (51,52). Yeni yapılan bir çalışmada Maeder ve arkadaşları, genel yoğun bakımda EF’u normal olan sepsisli hastalarda BNP seviyelerinin ciddi sistolik kalp yetersizliğindeki kadar yükselebileceğini göstermişlerdir (33). Mueller ve arkadaşları, inflamatuvar bir belirteç olan PCT’nin, İE’li hastalarda sepsisin de dahil diğer bakteriyel infeksiyonlardan daha fazla yükseldiğini göstermişlerdir (53). IE, sürekli bakteriyemi ile seyreden ciddi intravasküler infeksiyondur. Dolayısıyla İE’te, inflamatuvar tablonun yol açtığı kardiyak patolojileri en az sepsisteki kadar ciddi izleyebiliriz. Sitokin aracılı miyokardiyal depresyon İE’li hastalarda da gelişebilir ancak sol ventrikül EF; azalmış sistemik vasküler rezistans (54), mitral yetersizliği ve hiperdinamik tablo nedeniyle olduğundan fazla hesaplanıyor olabilir. 3. NT-proBNP yükselmesi, altta yatan kalp hastalığı tarafından tetiklenebilir (aort darlığı, mitral darlığı, pulmoner hipertansiyon, obstrüktif hipertrofik kardiyomiyopati gibi). 4. Azalmış böbrek fonksiyonları da NT-proBNP artışına yol açabilir (55). İE’te akut renal komplikasyonlara bağlı ya da önceki kronik renal hastalıklara bağlı azalmış glomerüler filtrasyon hızı, NT-proBNP’nin klirensini azaltabilir. Çalışmamızda, yüksek kreatinin düzeyi olan (kreatinin>2mg/dL) 8 hastanın NT-proBNP değerlerini, kreatinin düzeyi normal ya da normale yakın olan (kreatinin<2) 34 hastadan anlamlı oranda daha yüksek saptadık 54 (39538±35349 pg/mL yerine 11131±23710 pg/mL, p=0.009). Ancak NT-proBNP’nin kreatinin düzeylerinden bağımsız olarak klinik sonlanımın belirleyicisi olduğunu gösterdik. 5- Genel durumu çok kritik olan hastalarda, mekanik ventilasyon (bir hastada) sağ ventrikül yüklenmesine yol açarak (56) ya da norepinefrin sol ve sağ ventrikül ardyükünü artırarak (57) NT-proBNP salgılanmasına neden olabilir. Sol kalp endokarditli hastalarda NT-proBNP artışının en muhtemel nedeni, kalpte oluşan ciddi yapısal hasar ve sol ventrikül duvar stresinin artışıdır. Böylece NT-proBNP, İE’li hastalarda klinik sonlanımı belirlemede faydalı, yeni bir hemodinamik ve biyolojik parametre olabilir. 7.ÇALIŞMA KISITLILIKLARI Çalışma hastalarımızın sayısı göreceli olarak azdı, bu nedenle sonuçlarımızın daha geniş hasta gruplarında pekiştirilmesi gerekmektedir. Ayrıca hastalarımızın çoğunluğunun başvuru sırasındaki klinik durumu referans merkez olmamızın sonucu olarak kötüydü (yüksek NYHA fonksiyonel sınıf, renal yetersizlik ve sepsis gibi). Ek olarak, hastalarımızın altta yatan kalp hastalıkları oldukça çeşitliydi, dolayısıyla NT-proBNP seviyeleri bu farklılıktan etkilenmiş olabilir. Acil cerrahi tedaviye giden hastalara koroner anjiyo uygulanamadı ve koroner arter hastalığının varlığı ekarte edilemedi. 55 8.SONUÇ NT-proBNP, sol kalp infektif endokarditli hastalarda, daha agresif tedavi uygulanacak ya da cerrahi tedaviden fayda görecek yüksek riskli hasta grubunun belirlenmesinde kullanılabilecek yardımcı bir belirteçtir. 56 9. KAYNAKLAR 1. Horstkotte D, Follath F, Gutschik E, Lengyel M, Oto A ve ark. Task Force Members on Infective Endocarditis of the European Society of Cardiology; ESC Committee for Practice Guidelines (CPG); Document Reviewers. Guidelines on prevention, diagnosis and treatment of infective endocarditis executive summary; the task force on infective endocarditis of the European society of cardiology. 2004 February. 2. Van Der Meer JT, Thompson J, Valkenburg HA ve ark. Epidemiology of bacterial endocarditis in Nederlands. Arch Intern Med 1992;152:1863-68. 3. Lamas CC, Eykyn SJ. Hospital acquired native valve endocarditis: analysis of 22 cases presenting over 11 years. Heart 1998;79:442-7 4. Mylonakis E, Calderwood SB. Infective endocarditis in adults. New Engl J Med 2001;345:18:1318-1330. 5. Karchmer AW. Infective Endocarditis. In Braunwald E, Zipes DP, Bonow RO, Libby P: Heart Disease A Textbook of Cardiovascular Medicine 7th Edition. Philadelphia, W.B. Saunders Company 2005:1633-1658. 6. Patel R, Piper KE, Rouse MS, Uhl JR, Cockerill FR III, SteckelbergJM. Frequency of isolation of Staphylococcus lugdunensis among staphylococcal isolates causing endocarditis: a 20-year experience. J Clin Microbiol 2000;38:4262-3. 7. Brouqui P, Raolt D. Endocarditis due to rare and fastidious bacteria. Clin Microbiol Rev 14:177, 2001 8. Stein A, Raolt D. Q fever endocarditis. Eur Heart J 16(Suppl B):19, 1995. 9. Durack DT, Lukes AS, Bright DK. New criteria for diagnosis of infective endocarditis: utilization of specific echocardiographic findings. Am J Med 1994;96:200-9. 57 10. Perez-Vazquez A, Farinas MC, Garcia-Palomo JD, Bernal JM, Revuelta JM, GonzalezMacias J. Evaluation of the Duke criteria in 93 episodes of prosthetic valve endocarditis: could sensitivity be improved? Arch Intern Med 2000;160:1185-91. 11. Dodds GA, Sexton DJ, Durack DT, Bashore TM, Corey GR, Kisslo J. Negative predictive value of the Duke criteria for infective endocarditis. Am J Cardiol 1996;77:403-7. 12. Li JS, Sexton DJ, Mick N, et al. Proposed modifications to the Duke criteria for the diagnosis of infective endocarditis. Clin Infect Dis 2000;30:633-8. 13. Baddour LM, Wilson WR, Bayer AS, Fowler VG Jr, Bolger AF, Levison ME; Committee on Rheumatic Fever, Endocarditis, and Kawasaki Disease; Council on Cardiovascular Disease in the Young; Councils on Clinical Cardiology, Stroke, and Cardiovascular Surgery and Anesthesia; American Heart Association; Infectious Diseases Society of America. Infective endocarditis: diagnosis, antimicrobial therapy, and management of complications: a statement for healthcare professionals from the Committee on Rheumatic Fever, Endocarditis, and Kawasaki Disease, Council on Cardiovascular Disease in the Young, and the Councils on Clinical Cardiology, Stroke, and Cardiovascular Surgery and Anesthesia, American Heart Association: endorsed by the Infectious Diseases Society of America. Circulation. 2005 Jun 14;111(23):e394-434 14. Rohmann S, Erbel R, Darius H, Gorge G, Makowski T, Zotz R, Mohr- Kahaly S, Nixdorff U, Drexler M, Meyer J. Prediction of rapid versus prolonged healing of infective endocarditis by monitoring vegetation size. J Am Soc Echocardiogr. 1991;4:465– 474. 15. Hardy DJ, Hulbert BB, Migneault PC. Time to detection of positive BacT/Alert blood cultures and lack of need for routine subculture of 5 to 7-day negative culture. J Clin Microbiol 1992;30:2743-5 58 16. Doem Gv, Davaro R, George M ve ark. Lack of requirement prolong incubation of SeptiChek blood culture bottles in patients with bacteremia due to fastidious bacteria. Diagn Microbiol Infect Dis 1996;24:141-3. 17. Goldenberger D, Altwegg M. Eubacterial PCR: contaminating DNA in primer preperations and its elimination by UV light. J Microbiol Meth 1995;21:27-32 18. Geraci JE, Wilson WR. Symposium on infective endocarditis, III: endocarditis due to gram-negative bacteria. Report of 56 cases. Mayo Clin Proc. 1982;57:145–148. 19. Francioli PB. Ceftriaxone and outpatient treatment of infective endocarditis. Infect Dis Clin N Am. 1993;17:313–322. 20. Pierrotti LC, Baddour LM. Fungal endocarditis, 1995–2000. Chest. 2002;122:302–310. 21. Heiro M, Nikoskelainen J, Engblom E, Kotilainen E, Marttila R, Kotilainen P. Neurologic manifestations of infective endocarditis: a 17-year experience in a teaching hospital in Finland. Arch Intern Med. 2000; 160:2781–2787. 22. Vilacosta I, Graupner C, San Roman JA, Sarria C, Ronderos R, Fernandez C, Mancini L, Sanz O, Sanmartin JV, Stoermann W. Risk of embolization after institution of antibiotic therapy for infective endocarditis. J Am Coll Cardiol. 2002;39:1489 –1495. 23. Chan KL, Dumesnil JG, Cujec B, Sanfilippo AJ, Jue J, Turek MA, Robinson TI, Moher D; Investigators of the Multicenter Aspirin Study in Infective Endocarditis. A randomized trial of aspirin on the risk of embolic events in patients with infective endocarditis. J Am Coll Cardiol. 2003;42:775–780. 24. White PM, Teasdale EM, Wardlaw JM, Easton V. Intracranial aneurysms: CT angiography and MR angiography for detection: prospective blinded comparison in a large patient cohort. Radiology. 2001;219:739–749. 25. Bingham WF. Treatment of mycotic intracranial aneurysms. J Neurosurg. 1977;46:428– 437. 59 26. Mansur AJ, Grinberg M, Leao PP, Chung CV, Stolf NA, Pileggi F. Extracranial mycotic aneurysms in infective endocarditis. Clin Cardiol. 1986;9:65–72. 27. The endocarditis Working Group of the International Society of Chemoteraphy. Leport C. Antibiotic prophylaxis for infective endocarditis. Clin Microbiol Infect. 1998;4 (Suppl 3): S56-61 28. de Lemos JA, Mcguire DK, Drazner MH. B-type natriuretic peptide in cardiovascular disease. Lancet. 2003;362:316-322. 29. Hall C. Essential biochemistry and physiology of (NT-pro) BNP. Eur J Heart Fail 2004;6:257-260 30. Witthaut R, Busch C, Fraunberger P, Walli A, Seidel D, Pilz G, Stuttmann R, Speichermann N, Verner L, Werdan K. Plasma atrial natriuretic peptide and brain natriuretic peptide are increased in septic shock: impact of interleukin-6 and sepsis-associated left ventricular dysfunction. Intensive Care Med. 2003;29:1696 –1702. 31. Chua G, Kang-Hoe L. Marked elevations in N-terminal brain natriuretic peptide levels in septic shock., Crit Care. 2004, 8(4):R248-50. Epub 2004 Jun 15. 32. Brueckmann M, Huhle G, Lang S, Haase KK, Bertsch T, Weiß C, Kaden JJ, Putensen C, Borggrefe M, Hoffmann U. Prognostic value of plasma N-terminal pro brain natriuretic peptide in patients with severe sepsis. Circulation. 2005;112:527–534. 33. Maeder M, Ammann P, Kiowski W, Rickli H. B-type natriuretic peptide in patients with sepsis and preserved left ventricular ejection fraction. Eur J Heart Fail. 2005 Dec;7(7):11647. 34. Hoen B, Alla F, Selton-Suty C, et al. Changing profile of infective endocarditis: results of a 1-year survey in France. JAMA. 2002;288: 75–81. 35. Wallace SM, Walton BI, Kharbanda RK, et al. Mortality from infective endocarditis: clinical predictors of outcome. Heart. 2002;88:53–60. 60 36. Chu VH, Cabell CH, Benjamin DK, Kuniholm EF, Fowler VG, Engemann J, Sexton DJ, Corey GR, Wang A. Early predictors of in-hospital death in infective endocarditis. Circulation. 2004;109: 1745–1749. 37. Hall C, Rouleau JL, Moyè L, de Champlain J, Bichet D, Klein M, Sussex B, Packer M, Rouleau J, Arnold MO, Lamas GA, Sestier F, Gottlieb S, Wun CC, Pfeffer MA. N-terminal proatrial natriuretic factor: an independent predictor of long-term prognosis after myocardial infarction. Circulation. 1994;89:1934 –1942. 38. Gottlieb S, Kukin ML, Ahern D, Packer M. Prognostic importance of atrial natriuretic peptide in patients with chronic heart failure. J Am Coll Cardiol. 1989;13:153–159. 39. Mitaka C, Nagura T, Sakanishi N, Tsunoda Y, Toyooka H. Plasma α-atrial natriuretic peptide concentrations in acute respiratory failure associated with sepsis: preliminary study. Crit Care Med. 1990;18: 1201–1203. 40. Mukoyama M, Nakao K, Saito Y, Ogawa Y, Hosoda K, Suga S, Shirakami G, Jougasaki M, Imura H. Increased human brain natriuretic peptide in congestive heart failure. N Engl J Med. 1990;313:757–758. 41. Li JS, Sexton DJ, Mick N, et al. Proposed modifications to the Duke criteria for the diagnosis of infective endocarditis. Clin Infect Dis 2000;30: 633-8. 42. Daniel WG, Mügge A, Martin RP, Lindert O, Hausmann D, Nonnast-Daniel B, et al. Improvement in the diagnosis of abscesses associated with endocarditis by transesophageal echocardiography. N Engl J Med 1991;324:795-800. 43. Durack DT, Lukes AS, Bright DK. New criteria for the diagnosis of infective endocarditis: utilization of specific echocardiographic findings. Am J Med. 1994;96:200–209. 44. Cziner DG, Rosenzweig BP, Katz ES, Keller AM, Daniel WG, Kronzon I. Transesophageal versus transthoracic echocardiography for diagnosing mitral valve perforation. Am J Cardiol 1992;69: 1495-7. 61 45. von Reyn CF, Levy BS, Arbeit RD, Friedland G, Crumpacker CS. Infective endocarditis: an analysis based on strict case definitions. Ann Intern Med 1981;94:505-17. 46. McCartney AC, Orange GV, Pringle SD, Wills G, Reece IJ. Serum C reactive protein in infective endocarditis. J Clin Pathol 1988;41:44–48. 47. Hogevik H, Olaison L, Andersson R, Alestig K. C-reactive protein is more sensitive than erythrocyte sedimentation rate for diagnosis of infective endocarditis. Infection 1997;25:82– 85. 48. Heiro M, Helenius H, Sundell J, Koskinen P, Engblom E, Nikoskelainen J, Kotilainen P. Utility of serum C-reactive protein in assessing the outcome of infective endocarditis. Eur Heart J. 2005 ;26(18):1873-81. 49. Meisner M. Pathobiochemistry and clinical use of procalcitonin. Clin Chim Acta. 2002;323:17–29. 50. Kocazeybek B, Kucukoglu S, Oner YA. Procalcitonin and C-reactive protein in infective endocarditis: correlation with etiology and prognosis. Chemotherapy. 2003;49:76–84. 51. Kumar A, Thota V, Dee L, Olson J, Uretz E, Parillo JE. Tumor necrosis factor alpha and interleukin 1 beta are responsible for in vitro myocardial cell depression induced by human septic shock serum. J Exp Med. 1996;183:949 –958. 52. Parker MM, Shelhamer JH, Natanson C, Alling DW, Parillo J. Serial cardiovascular variables in survivors and nonsurvivors of human septic shock: heart rate as an early predictor of prognosis. Crit Care Med. 1987;15:923–929. 53. Mueller C, Huber P, Laifer G, Mueller B, Perruchoud AP. Procalcitonin and the Early Diagnosis of Infective Endocarditis. Circulation. 2004;109:1707-1710.) 54. Krishnagopalan S, Kumar A, Parillo JE, Kumar A. Myocardial dysfunction in the patient with sepsis. Curr Opin Crit Care 2002;8: 376–88. 62 55. Vickery S, Price CP, John RI, Abbas NA, Webb MC, Kempson ME, Lamb EJ. B-type natriuretic peptide (BNP) and amino-terminal proBNP in patients with CKD: relationship to renal function and left ventricular hypertrophy. Am J Kidney Dis. 2005;46(4):610-20. 56. Passino C, Maria Sironi A, Favilli B, Poletti R, Prontera C, Ripoli A, Lombardi M, Emdin M Right heart overload contributes to cardiac natriuretic hormone elevation in patients with heart failure. Int J Cardiol. 2005 Sep 15;104(1):39-45. 57. LeDoux D, Astiz ME, Carpati CM, Rackow EC. Effects of perfusion pressure on tissue perfusion in septic shock. Crit Care Med 2000;28:2729–32. 63