Atomun Özellikleri
advertisement

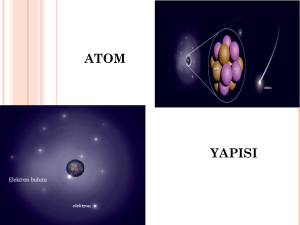
7.SINIF 3.ÜNITE MADDENİN YAPISI VE ÖZELLİKLERİ Dilara SAĞER 20120905053 1 MADDE VE ÖZELLİKLERİ ATOMUN YAPISI Elementlerin özelliğini taşıyan, en küçük yapı birimine atom denir. Kimyasal veya fiziksel olaylarla daha basit bileşenlere ayrılmayan, maddenin en küçük birimine de denebilir. 2 Atomun Özellikleri: Atomlar çekirdek ve yörüngelerinden oluşmalıdır. Çekirdekte proton ve nötronlar, yörüngede ise elektronlar bulunmalıdır. Atomun kütlesi, çekirdeğin kütlesine eşittir. Bir elementi oluşturan tüm atomların, proton sayıları dolyısıyla birbirinin ayrıdır. 3 Proton: Atomun çekirdeğinde bulunun, + yüklü taneciklerdir. Atomun cinsini belirler. Nötr atomlarda, elektron sayısına eşittir. Atomun kütlesine etki eder. 4 Nötron: Atomun çekirdeğinde bulunan yüksüz taneciklere denir. Atomun çekirdek yüküne etki etmezler. Atomun kimyasal özelliklerine etki etmezler. Atomun kütlesine etki ederler. 5 Elektron: Atom çekirdeğinin etrafında hareket eden yüklü taneciklere denir. - yüklü taneciklerdir. Atomun yüküne etki ederler. Atomun kimyasal özelliklerine etki edeler. Atomun kütlesine etkileri ihmal edilir. 6 Nötr Atom: Bir atomdaki proton ve elektron sayıları birbirine eşittir. Örneğin nötr karbon atomunda 6proton varsa 6 elektron vardır. p=e Atomlar elektron alıp verebilir, fakat proton ve nötron alıp veremez. 7 (-) Yüklü Negatif Atom (Anyon): Eğer bir atom dışarıdan elektron alırsa, (-)yük sayısı (+) yük sayısından fazla olur. Bu durumda atom (-)yüklü negatiftir. Örneğin nötr flöur atamu 9elektron 9 protunu varken -1 yük elektron alırsa 10 elektronu olur. 8 (+)Yüklü Pozitif Atom (Katyon): Eğer bir atom elektronunu kaybederse, (+) yük sayısı (-) yük sayısından fazla olur. 9 ELEMENT Aynı cins atomlardan meydana gelen saf maddelere denir. Saftırlar. Homojenlerdir. Belirli erime ve kaynama noktaları vardır. Belirli yogunlukları vardır. Sembollerle gösterilir. Periyodik tabloda gösterilirler. 10 BILEŞIK İki ya da daha fazla cins atomdan meydana gelen saf maddelerdir. Bileşiklerin çoğu molekül yapıdadır. Ancak tuzlar atomik yapıdadır. Bileşikler belirli formüllerle gösterilir. Bileşikle karışımın farkı,bileşikler belirli sayıda element atomunun kimyasal bir bağ ile bağlanmasıyla oluşur. Ancak karışımların belirli bir formülü yoktur. Elementler bir araya gelerek kendi özelliklerini kaybeder, fakat karışımları oluşturan maddeler özelliklerini kaybetmezler. 11 KARIŞIM Birden fazla maddenin kimyasal özellikleri değişmeyecek şekilde bir araya gelmesiyle oluşan madde topluluğudur. Saf maddeler element ve bileşiklerden oluşur. Karışımı oluşturan maddelerin miktarları arasında belirli bir oran yoktur. İstenildiği oranda karıştırılabilirler. Az şekerli veya çok şekerli çay olur. Karışımların belirli bir kimyasal formülleri yoktur. Oksijen elementi, O ile su bileşiği H2O ile gösterilir fakat karışımlarda madde isimleri hepsi birden söylenir. Karışımlar fiziksel yollarla oluşur ve bileşenlerine fiziksel yollarla ayrılırlar. 12 Karışımlar, homojen ve heterojen olmak üzere ikiye ayrılır. Homojen karışımlar: Her tarafında aynı özelliği gösteren, tek bir madde gibi gözüken karışımlardır. Karışımı meydana getiren maddeler gözle veya optik aletlerle görülemezler, Homojen karışımlara genel olarak “çözeltiler” de denir. Tuzlu su, şekerli su, alkollü su, çeşme suyunu homojen karışıma örnek verebiliriz. 13 14 Heterojen karışımlar: Her tarafta aynı özelliği göstermeyen ve içindeki taneciklerin gözle görülebildiği karışımlardır. Heterojen karışımlar kendi aralarında süspansiyon, emülsiyon, aerosol ve koloit gibi gruplara ayrılır. Yer altından çıkarılan maden filizleri, kaya parçaları, odun parçaları, bir bitki yaprağı, sis, ayran, petrol su karışımı, beton parçası, toprak heterojen karışımlara örnek verilebilir. Süt çıplak gözle homojen gibi gözükmesine rağmen mikroskopla bakıldığında (yağ damlacıklarından dolayı) heterojen olduğu gözlenir. Heterojenlik mikroskopla tespit edildiği gibi tyndall ışığı etkisi ile de tespit edilebilir. 15 16 Emülsiyon: Bir sıvıda çözünmeyen başka bir sıvının heterojen olarak bulanık bir şekilde dağılmış hâlidir. Su– zeytinyağı karışımı, su–benzin karışımı, gibi. Süspansiyon: Bir sıvıda çözünmeyen katının heterojen olarak dağılmış şeklidir. Su–kum karışımı, su–tebeşir tozu karışımı gibi. Kolloid: Bir maddenin sıvı içerisinde asılı kalmasıyla oluşan karışımlara denir. Homojen gibi görünürler, karışımı oluşturan maddeler gözle görülemezler, ancak karışımdan ışın demeti veya lazer ışını geçirilerek fark edilebilirler. Duman, jöle, boya gibi maddeler buna örnektir. Aerosol: Bir katı veya sıvının gaz içinde dağılmasıyla oluşan karışımlardır. Sis, sprey, baca dumanı buna örnektir. Aerosol karışımların çoğu koloite örnektir. 17 ALIŞTIRMA Atomu oluşturan temel parçacıklar aşağıdaki seçeneklerden hangisinde doğru olarak verilmiştir? A) Çekirdek,elektron, iyon B) Proton, nötron, iyon C) Proton, nötron, elektron D) Proton, nötron, katman 18 Nötr bir atomun elektron sayısını bulabilmek için aşağıdakilerden hangisinin bilinmesi yeterlidir? I. Yalnız proton sayısı II. Yalnız nötron sayısı III. Yalnız kütle numarası A) Yalnız I B) I, II C) I, III D) I, II, III Aşağıdakilerden hangisi bileşik değildir? A) CO2 B) Co C) NH4 D) H2O 19 I. Elementler sembollerle gösterilir. II. Elementler formülle gösterilir. III. Bileşikler formüllerle gösterilir. Yukarıda verilenlerden hangileri doğrudur? A) Yalnız I B) Yalnız III C) I, II D) I, III 2+ yüklü iyon için aşağıdakilerden hangisi her zaman doğrudur? A) Proton sayısı elektron sayısından 2 eksiktir. B) Proton sayısı elektron sayısından 2 fazladır. C) Proton sayısı nötron sayısından 2 fazladır. D) Proton sayısı nötron sayısından 2 eksiktir 20 KAYNAKÇA http://www.fenokulu.net/portal/Sayfa.php?Git =KonuKategorileri&Sayfa=KonuDigerListesi&ba slikid=176&DigID=206 http://tr.wikipedia.org/wiki/Kar%C4%B1%C5% 9F%C4%B1m http://vimeo.com/23503409 http://www.sanalokulumuz.com/maddeninyapisi-ve-ozellikleri-7sinif-cozumlu-test/143 http://karisim.nedir.com/ 21