moleküler yapılı bileşikler
advertisement

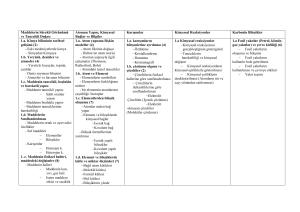
BILEŞIKLER VE FORMÜLLERI Farklı elementlere ait atomların belirli oranlarda bir araya gelerek bağ yapmasıyla oluşan yeni ve saf maddeye bileşik denir. Bileşikler kendilerini oluşturan elementlerden tamamen farklı fiziksel ve kimyasal özelliklere sahiptir. Bileşikler moleküler yapıda olabilecekleri gibi, olmayabilirler de. Örneğin su, su moleküllerinden oluşur. Çünkü suyu oluşturan hidrojen ve oksijen arasında kovalent bağ vardır.( amonyak, karbondioksit, basit şeker, kükürtdioksit gibi.) Bileşikler moleküler yapıda değilse, bileşiği oluşturan atomlar arasında iyonik bağ vardır. Bu tür bileşiklere iyonik yapılı bileşik denir. İyonlar yığınlar halinde düzgün bir örgü oluşturur. ( kalsiyumoksit, sodyumiyodür gibi) Bileşikler içerdikleri elementlere göre adlandırılır. Bileşikleri göstermek için element sembollerini kullanırız. Bunlara formül denir. Bir bileşik formülünde, o bileşiği oluşturan elementlerin sembolleri ve o elementin atomlarından kaç tane olduğu yazılır. Örneğin: CO de 1 karbon atomu, 2 oksijen atomu, HCI’de 1 hidrojen atomu, 1 klor atomu, C H O ‘da 6 karbon, 12 hidrojen, 6 oksijen atomu vardır. BILEŞIKLERIN ÖZELLIKLERI 1- Bileşikler, kendini oluşturan elementlerin özelliklerini göstermezler ve kendini oluşturan elementlerden tamamen farklı fiziksel ve kimyasal özelliklere yani kimliklere sahiptir 2- Bileşiği oluşturan elementler kendi özelliklerini yani kimliklerini kaybederler. 3- Bileşiği oluşturan elementler belirli oranlarda birleşirler. 4- Bileşiği oluşturan element atomları arasında kimyasal bağlar bulunur. 5- Bileşikler oluşurken enerji alışverişi olur. 6- Bileşikler, kimyasal değişmeler sonucu (tepkimelerle) oluşur ve kimyasal yollarla ayrılırlar. 7- Bileşikler en az iki farklı elementten yani atomdan oluşurlar. 8- Bileşiklerin belirli erime, kaynama, donma ve yoğunlaşma sıcaklıkları vardır. 9- Bileşiklerin öz kütleleri sabittir. 10- Bileşikler formüllerle gösterilirler. 11- Bileşikler saf ve homojen maddelerdir. 12- Bileşikler, moleküler yapılı bileşikler ve moleküler yapılı olmayan bileşikler olarak iki çeşittir. 13- (Bileşiklerin en küçük yapı birimleri moleküllerdir). BILEŞIK ÇEŞITLERI Bileşikler moleküler yapılı bileşikler ve moleküler yapılı olmayan bileşikler olarak iki grupta incelenirler. a) Moleküler Yapılı Bileşikler: Bileşikler, farklı cins element atomlarından oluşan moleküllerden oluşmuşsa böyle bileşiklere moleküler yapılı bileşikler denir. Moleküler yapılı bileşikler moleküllerden oluşur. Bileşiklerdeki molekülleri oluşturan atomlar arasında kovalent bağ bulunur. Bileşiğin İsmi Bileğin Formülü Bileşiği Oluşturan Atomlar Su H2O 2 H, 1 O Amonyak NH3 1 N, 3 H Karbon Di Oksit CO2 1 C, 2 O Kükürt Di Oksit SO2 1 S, 2 O Hidrojen Klorür HCl 1 H, 1 Cl Hidrojen Florür HF 1 H, 1 F b) Moleküler Yapılı Olmayan Bileşikler : Bileşikler, moleküllerden oluşmayıp bileşiği oluşturan farklı cins element atomları bir yığın oluşturacak şekilde bir araya gelmişse böyle bileşiklere moleküler yapılı olmayan bileşikler denir. • Moleküler yapılı olmayan bileşiklerdeki iyonlar düzenli bir yığın oluştururlar. • Moleküler yapılı olmayan bileşikler sonsuz örgü tipi bileşiklerdir • Moleküler yapılı olmayan bileşiklerdeki iyonlar düzenli bir örgü oluştururlar. • Moleküler yapılı olmayan bileşikleri oluşturan zıt yüklü iyonlar arasında iyonik bağ bulunur. Bileşiğin İsmi Bileşiğin Formülü Bileşiği Oluşturan İyonlar Kalsiyum Oksit CaO Ca+2 ve O–2 İyonları Sodyum İyodür NaI Na+1 ve I–1 İyonları Sodyum Klorür NaCl Na+1 ve Cl–1 İyonları Alüminyum AlCl3 Klorür Al+3 ve Cl–1 İyonları CaF2 Ca+2 ve F–1 İyonları Alüminyum Al2S3 Sülfür Al+3 ve S–2 İyonları Kalsiyum Florür







![C Elementi [Slayt]](http://s1.studylibtr.com/store/data/000924935_1-effe9d67aa73b7116686c4c63d62e23f-300x300.png)