MOLEKÜLER DNA DİZİ ANALİZ YÖNTEMLERİ
advertisement

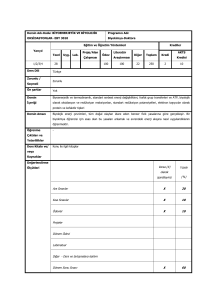
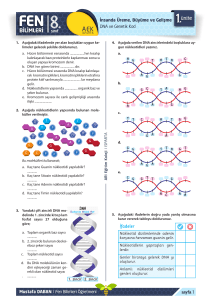
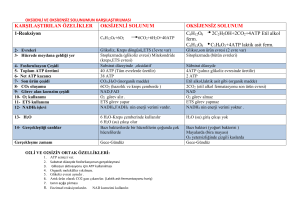
MOLEKÜLER DNA DİZİ ANALİZ YÖNTEMLERİ DNA dizi analizleri ya da sekanslama; DNA birincil (temel) yapılarının belirlenmesinde kullanılan yöntemlerdir, DNA’nın nukleotid dizilerinin saptanması anlamına gelir. DNA dizi analizi, gen yapısı ve genetik kontrol mekanizmaları hakkında bir çok bilgi edinmemizi sağlamıştır. Özellikle kalıtsal hastalıkların meydana gelme ve tedavi süreçleriyle ilgili mekanizmaların anlaşılması için, araştırma yapılan konuya etki eden gen bölgelerinin belirlenmesi gerekir. 2 Bu bakımdan DNA dizi analizlerinin yapılması, tedavi sürecinin başlangıcı ve devamında izlenecek yolu belirleyen en önemli faktördür. DNA dizi analizi ile birçok organizmanın genlerinin yapısı ve organizasyonu hakkında önemli bilgiler elde edilmiştir. Birçok canlı türünün tüm genom haritaları tanımlanmıştır 3 Sıklıkla gen mutasyonları (delesyon, insersiyon vb.) tespiti yada rekombinant DNA oluşum yapılarının tayininde kullanılır Preimplantasyon tanısı, kalıtsal hastalık tayininde oldukça sık kullanılır. Kalıtsal hastalık taşıyan çiftlerde tüp bebek embriyolarından alınan DNA’lar bu yöntemle analiz edilerek taşıyıcı embriyolar elenip, genetik hastalık taşımayanların doğması sağlanmaktadır. 4 Tarihçe DNA’nın 3 boyutlu yapısı, 1953 yılında tanımlandıktan sonra dizi analiz çalışmalarına öncülük oluşturacak ilk denemeler küçük RNA parçaları ile çalışılmış olup, Robert Holley tarafından 1965 yılında tRNA molekülünün dizi analizi yapılmıştır. 1977 yılında Allan Maxam-Walter Gilbert ve Sanger tarafından iki farklı DNA dizi analiz yöntemi bulunmuştur. Otomatik dizi analiz cihazları 1985 yılından itibaren geliştirilmiştir. 1992 yılında 21. kromozomun DNA dizi analizi tamamlanmıştır. 1999 yılında insanın 22. kromozomunun DNA dizisi tamamlanmıştır. 5 Nükleik asitler Nükleik asitler genetik bilginin depolanması ve ifade edilmesinden sorumlu moleküllerdir. DNA ve RNA olmak üzere iki tip nükleik asit vardır. Nükleik asitlerin yapısında: - Pürin ve primidin bazları - Şekerler - Nükleozidler -Nükleotidler -Polinükleotidler 6 Şekerler DNA da 2-deoksiriboz, RNA da ise riboz şekeri bulunur. Nükleik asit şekerlerinin 3 karbon atomuna bağlı OH grubu kendisinden sonra gelen nükleik asit şekerinin 5 karbon atomuna bağlı fosfat grubu ile reaksiyona girerek ester bağı oluşturur. 7 Pürin ve pirimidin bazları Adenin, guanin, hipoksantin ve ksantin pürin bazlarıdır. Adenin ve guanin hem DNA hemde RNA’ nın yapısında bulunmaktadır. Hipoksantin ve ksantin nükleik asit yapısına katılmazlar. Urasil, timin, sitozin ve oratik asit pirimidin bazlarıdır. Sitozin hem DNA hem de RNA’ da, urasil ise sadece RNA’ da bulunur. 8 NÜKLEOZİD: Pürin yada pirimidin bazına şeker eklenmesi ile oluşur. NÜKLEOTİD: Nükleozidlere fosfat grubunun eklenmesi ile ortaya çıkar. Genellikle fosfat grubu şekerin 5 karbonuna ester bağı ile bağlı durumdadır. 9 DNA’NIN YAPISI Nükleotidlerin arasındaki hidrojen bağları iki zinciri bir arada tutar. Nükleotidler birbirlerine şeker-fosfatlar aracılığıyla kovalent bağlanmışlardır. Nükleotid alt birimlerinin birlikte sıralandıkları şekil DNA dizisine kimyasal bir kutupluluk verir. Bir DNA zincirindeki bu kutupluluk bir uca 3̀ ve diğer uca 5̀ ucu adı verilerek belirtilmiştir. . Bir DNA molekülü dört tip nükleotid alt biriminden oluşan iki uzun polinükleotid zincirinden meydana gelmiştir. 10 DNA 11 DNA’nın üç boyutlu yapısı (çift sarmal), iki polinükleotid zincirinin kimyasal ve yapısal özelliklerinden kaynaklanır. İki zincir farklı iplikler üzerindeki bazların arasındaki hidrojen bağlarıyla bir arada tutulduğundan bütün bazlar çift sarmalın iç tarafında, şeker-fosfat omurgası ise iç taraftadır. Her durumda adenin(A), timin(T) ile ve guanin(G) her zaman sitozin(C) ile birleşir. G ve C arasında üç, A ve T arasında iki hidrojen bağı vardır. Bu eşleşmeler baz çiftinin çift sarmal içinde enerji açısından en uygun şekilde paketlenmelerine izin verir. Şeker fosfat omurgası 10 baz çiftinde bir tam dönüşle bir çift sarmal oluşturmak üzere birbirinin etrafında döner. 12 DİZİ ANALİZ YÖNTEMLERİ Geleneksel yöntemler: - Sanger dideoksi yöntemi - Maxam-Gillbert kimyasal degredasyon yöntemi Shotgun Pyrosequencing 13 Her iki geleneksel teknik de üç temel basamaktan oluşmaktadır. • DNA’nın hazırlanması • Reaksiyonlar • Yüksek voltajlı jel elektroforezi 14 • Geleneksel yöntemlerde analiz sırasında tek iplikli DNA parçaları hazırlanır. • DNA dizi analiz yöntemi sırasındaki temel fark DNA parçacıklarının üretilme biçiminden kaynaklanır. •Jel elektroforezi yüksek çözünürlükteki DNA moleküllerini ayrıştırdığı için her iki metot da kullanılır. 15 MAXAM-GİLBERT DİZİLEME YÖNTEMİ Farklı uzunluktaki DNA parçalarının oluşumu ile sonlanan DNA’ yı kesmek için kimyasalların (Hidrazin, dimetil sülfat ya da formik asit) kullanıldığı yöntemdir. Tek bir sekans jelinde 40 klonun analiz edilmesini sağlar. Yöntemin temel prensibi, DNA’ da bulunan bazların kimyasallar kullanılarak değiştirilmesine ve daha sonra değişikliğe uğramış nükleotidlerin (Piperidin) bulunduğu noktalardan zinciri kırması esasına dayanır. 16 Maxam Gilbert yöntemi Pürinlerin kırılmasında dimetil sülfat kullanılır. Bazik ortamda DNA guanin bazından kırılırken asidik ortamda DNA adenin bazından kırılır. Primidin bazlarının kırılması hidrazin ile yapılır. Hidrazin DNA’yı hem sitozin hem de timin bazından kırar. Yüksek tuz derişimi ve bazik ortamda DNA sitozin bazından kırılır. 17 Maxam Gilbert yönteminde kullanılan kimyasallar Özgül baz Baza özgül Baz ayırmada kullanılan Zincir kırmada kullanılan G Dimetil sülfat Piperidin Piperidin A+G Asit Asit Piperidin C+T Hidrazin Piperidin Piperidin C Hidrazin+baz Piperidin Piperidin 18 Maxam Gilbert yöntemi Bu yöntemde nükleotid dizisi saptanacak DNA, önce 5̀ ucunda P ile ya da floresan bir boya ile işaretlenir. DNA’ nın iki iplikçiği birbirinden ayrılarak, ya da DNA uygun bir restriksiyon enzimi ile kesilerek DNA’nın bir ucundan işaretlenmesi sağlanır. İkinci adımda ise DNA molekülleri dört tüpe ayrılarak A, C, G, T nükleotidlerini kırmak için gerekli tepkimeler gerçekleştirilir. 19 Maxam Gilbert yöntemi Reaksiyon sonunda her tüpte farklı pozisyonlardaki hedef nükleotidlerden kırılmış DNA parçaları elde edilir. Sonuçta kırılmanın olduğu pozisyona göre hepsi 5̀ ucundan işaretli ancak boyları birbirinden farklı bir dizi DNA parçası elde edilmiş olur. Elde edilen boyları gittikçe kısalan DNA dizileri jel elektroforezi ile birbirlerinden büyüklüklerine göre ayrılır ve otoradyografi uygulanarak bantlar görüntülenebilir. 20 21 SANGER DİZİLEME YÖNTEMİ Bu yöntem enzimatik DNA sentezine dayanır ve en yaygın kullanılan dizi analiz tekniğidir. Yöntemde dizisi saptanacak olan DNA ipliği yeni sentezlenecek iplik için kalıp olarak kullanılır. DNA sentezi sağlamak için Klenov, Taq DNA polimeraz, ters transkriptaz yada sequenaz enzimlerinden birisi kullanılabilir. 22 Sanger dizi analiz yöntemi Yöntemin temeli, DNA polimerazın dNTP (deoksiribonükleozid trifosfat) ve ddNTP (dideoksiribonükleozid trifosfat) leri de substrat olarak kullanabilmesi esasına dayanır. Teknik olarak dizi analizi 3 basamaktan oluşur. a ) polimeraz zincir reaksiyonu b ) dizileme reaksiyonu c ) jel elektroforezi ve bilgisayarda değerlendirme 23 İŞLEYİŞ DNA tek zincir haline getirilir.Reaksiyona girecek olan karışımda bol miktarda dört çeşit normal nükleotid bulunur. dATP dGTP dCTP dTTP. Karışımda aynı zamanda diziyi rastgele sonlandırmak için farklı renkte flouresan kimyasallarla işaretlenmiş dideoxynukleotidler vardır. ddATP ddGTP ddCTP ddTTP DNA polymerase I ise sentezde zincirin uzaması aşamasında gereklidir. 24 Sanger dizi analiz yöntemi PZR’ da denatürasyon, bağlanma ve uzama basamakları ile hedef DNA çoğaltılır. Dizileme reaksiyonu için gerekenler: -DNA kalıbı -Taq DNA polimeraz (tek zincirli DNA dizisinin saptanmasında tercih edilir. Sıcağa dayanıklı olduğu için yaygın kullanılan enzim türüdür.) -Primer -Deoksinükleotid (d NTP) -Dideoksinükleotid (ddNTP) 25 Sanger dizi analiz yöntemi DNA polimeraz, primer kalıp DNA ve dNTP’ler ortama konulup işaretli nükleotitin yapıya katılması sağlanır. Kullanılan ddNTP’lerin konsantrasyonu diğer maddelerden daha düşük olmalıdır. İşaretleme primere de yapılabilir. İşaretlemeden sonra zincir sonlanması reaksiyonlarına geçilir. 26 Sanger dizi analiz yöntemi Karışım dört kısma ayrılarak dört tüpe konulur. Her tüpe gerekli enzim faktörleriyle birlikte düşük derişimli farklı ddNTP’ler konulur ve inkübe edilir. ddNTP’ler ve dNTP’ler aynı karışıma konduğunda aralarında bir yarışma olur. Substrat olarak dNTP’ler kullanıldığı sürece uzama devam eder. Sentezin herhangi bir noktasında yapıya dideoksi girdiğinde reaksiyon durur. 27 Sanger dizi analiz yöntemi Her tüpte aynı anda birbirinden bağımsız birçok reaksiyon olmuştur. Sonuçta primer sonundan başlayıp prematüre sonlanmaların olduğu bölgelere kadar çeşitli uzunlukta DNA parçaları oluşur. DNA dizi analizi sonucu elde edilen DNA dizileri jel üzerinde gümüş boyama, radyoaktif ve flouresan boyalarla işaretlenerek tespit edilebilir. 28 Sanger dizi analiz yöntemi Dizileme reaksiyonu PZR gibi üç ana basamakta ve 30-40 döngüde gerçekleşir. Sentezlenen DNA ya bir ddNTP’nin katılması 3̀ pozisyonunda OH grubu olmadığı için sentezi durdurur. Reaksiyon sonunda deoksinükleotidlerle uzamış ve ddNTP lerle sonlanmış diziler elde edilir. Sonlandırıcı özellikteki bazlar flouresan boyalarla işaretlenebilir. 29 Bu resim için web sitesi the-scientist.com •Tam boyutlu resim - Aynı boyutlux daha büyük Boyut: 752 × 532 Tür: 109KB JPG Bu görselin telif hakkı korunuyor olabilir. 30 Sanger dizi analiz yöntemi Elde edilen DNA dizilerine jel elektroforezi uygulanabileceği gibi otomatik dizi analizi cihazlarınca okuma yapılabilir. Jel elektoforezinde DNA parçaları elektriksel alanda uzunluklarına göre sıralanır ve DNA dizisi jelden okunur. Poliakrilamid jeller yüksek ayırım gücüne sahiptir. Poliakrilamid jeller uygun süre ve uygun voltajda tek bir nükleotid farkını bile ayırabilir. 31 32 OTOMATİK DİZİ ANALİZİ İnsan Genom Projesi gibi büyük projeler çok sayıda DNA dizi analizi yapılmasını gerektirmektedir. Artan analiz sayısı, uzun zaman ve yüksek iş gücü gerektirir. Bu gelişmeler sonucunda otomasyon kaçınılmaz olmuştur. Otomatik DNA dizi analizleri zaman kazancı yanında, standart çalışma koşulları ve elde edilen sonuçların değerlendirilmesinde de yarar sağlamıştır. Otomatik analizde de Sanger’in enzimatik DNA sentezine dayanan zincir sonlanma yöntemi kullanılmıştır. 33 Otomatik dizi analizi Otomatik DNA dizi analiz cihazları basit olarak sabit bilgisayarda yüklü programlar ile bu programların yönettiği elektroforez sistemini içerir. Elektroforetik ünitelerde bulunan lazer ışık kaynağı ile monokromatik bir ışık oluşturulur. Söz konusu DNA’nın bulunduğu jel matriks bu monokromatik ışık ile taranır. 34 Otomatik dizi analizi Elektroforez süresince DNA’ya bağlanan flouresan boya ışık ile taranan bölgeye geldiğinde uyarılır. Uyarılan boya kendi için karakteristik olan dalga boyunda ışığı geri yansıtır. Yansıyan bu ışık demeti bir dedektör tarafından kaydedilir. Bu veriler bilgisayar programları ile değerlendirilerek sonuçlar grafiksel ya da matematiksel olarak bilgisayar ekranına aktarılır. Dizi analiz cihazları ile 6 bazdan 1000 baza kadar güvenli okuma yapılabilmektedir. 35 Otomatik DNA dizi analizi cihazı Sabit bilgisayarda yüklü programlar Programın yönettiği elektroforez sistemi Poliakrilamid jelin yerini polimer almıştır 36 37 SHOTGUN DİZİLEME YÖNTEMİ Bu yöntemde çok büyük klonlanmış DNA parçaları bir çok parçaya bölünerek alt klonlar halinde dizileme yapılır. DNA parçaları sekanslandıktan sonra orijinal DNA yeniden yapılandırılmaya çalışılır. Bu yöntemde amaç; hem hız kazanmak hem de doğruluk oranı daha yüksek sonuçlara ulaşmaktır. Yaklaşık 10000 bazda 1 hata oranı ile çalışıldığı kabul edilir. Özellikle kromozom analizlerinde ve genom projelerinde tercih edilir. 38 PYROSEKANSLAMA Dizi analizi için en sık kullanılan yöntem olan Sanger metodunun uzun sürmesi, bir çok aşamayı içermesi gibi çeşitli dezavantajlarını ortadan kaldıran, 1986 yılında Pal Nyren tarafından geliştirilmiş bir yöntemdir. Single-nükleotide addition (SNA) yani tek nükleotid eklenmesi yöntemi ile dizi analizi yapmaktadır. 39 PYROSEKANS Sentez yaparak dizi analizi yapma prensibine dayanır. DNA sentezi esnasında açığa çıkan pirofosfat’ların saptanması esasına dayanan bir real-time (gerçek-zamanlı) kantitatif dizi analizi tekniğidir. İşlem PZR ürünlerinin tek zincir DNA (ssDNA) ya dönüşmesi ile başlar . Tek sarmal DNA kalıp olarak kullanılmak üzere izole edilir, her bir primer çifti biotin ile 5' ucundan işaretlenir. 40 Pyrosekans aşamaları 1.Aşama Sekans primeri PZR ile çoğaltılmış olan bir tek zincir DNA ile hibridize edilir. Enzim olarak DNA polimeraz, ATP sülfürilaz, lüsiferaz ve apiraz kullanılır. Substrat olarak adenozin 5‘ fosfosülfat ve lusiferin ile inkübe edilir. 41 Pyrosekans aşamaları 1.Aşama Sekans primeri + ssDNA kalıbı hibridizasyon Enzimler: DNA polimeraz, ATP sülfürilaz, lusiferaz ve apiraz, Substratlar: Adenozin 5’ fosfosülfat (APS) ve lusiferin 42 2. Aşama d NTP (deoksiribonükleotid trifosfat) lardan ilki reaksiyona eklenir. Eğer dNTP kalıp DNA’ daki baza komplementer ise ortamda bulunan DNA polimeraz, bu dNTP’nin DNA sarmalına eklenmesini kataliz eder. dNTP DNA kalıbına bağlanırken dNTP üzerindeki 2 adet fosfat açığa çıkar ve ortama 2 fosfatlı bir yapı olan pirofosfat (Ppi) ortama geçmiş olur. Her nükleotid eklenmesinde bir pirofosfat serbest kalır. 43 3. Aşama Ortama çıkan pirofosfat; ATP sulfurylase yardımı ile ATP’ ye çevrilir. Oluşan ATP’ nin yardımı ile lusiferin, oksilusiferin’ e dönüşür. Oksilusiferin ise görünür bir ışın yayar. Oluşan bu ışın miktarı ATP miktarı ile orantılıdır. Oluşan ışın CCD (kızıl ötesi) kamera ile tespit edilir ve seri tepecik şeklinde kaydedilir. 44 Işınların seri tepecik şeklinde kaydedilmesine Pyrogram adı verilir. Işın pyrogramda bir yükseklik veya tepecik şeklinde görülür. Her bir tepeciğin yüksekliği eklenmiş olan nükleotid sayısıyla orantılıdır. 45 3. Aşama ATP sülfirilaz PPi ATP (Adenosine 5’ fosfosulfat (APS)) lusiferaz Lusiferin oksilusiferin (ATP) 46 Pyrogram Işın miktarı ATP miktarı ile orantılıdır Işın Pyrogram’da bir yükseklik olarak görülür 47 4. Aşama Nükleotid parçalayıcı bir enzim olan apiraz devamlı olarak ATP ve dNTP’ leri parçalar. Böylece ışık oluşumu kesilir. Yani ortamda yeni reaksiyon oluşturacak d NTP ve ATP kalmamış olur ve bu şekilde ortam ikinci nükleotidin ilave edilmesine hazırlanmış olur. Bu teknoloji ile DNA parçacığının 100 nükleotidi okunmuş olur. Dört enzimin yer aldığı bu aşamalar kapalı bir sistemde, plakta ve tek bir kuyucukta yapılabilir. İşlemin süresi kısadır. 48 4. Aşama Apyrase ATP’yi ve bağlanmamış olan dNTP’leri parçalar ışık kesilir. Reaksiyon solüsyonu yenilenir. 49 5. Aşama Komplementer DNA zinciri yapılır. Nükleotid dizisi Pyrogram’daki sinyal tepeciklerinden saptanır. Pyrogram’da iki kat yükseklik gösteren tepecikler eş iki nükleotidin ardarda bağlanması sonucu oluşmaktadır. 50 Pyrosekans Prensibi 51 PZR aşamasından sonra pyrosequencing, sekanslanacak baz sayısına bağlı olarak 10 dakika kadar kısa sürede sonuç verebilmektedir ve kolaylık, eleman, zaman ve maliyet açısından avantajlara sahiptir. Halen bir PZR ürününün dizi analizini yapan en hızlı yöntemdir ve doğruluk oranı oldukça yüksektir. Sanger tekniğindeki gibi işaretli primer, işaretli nükleotid ve jel elektroforezine ihtiyaç olmaması bu tekniğin önemli avantajlarıdır. 52 Kullanım Alanları Metilasyon analizleri Heteroplazmik DNA sekanslaması, Adli tıp analizleri, Viral tiplendirme ve direnç, Bakteriyal tiplendirme ve direnç, Fungal tiplendirme ve direnç, İnsersiyon, delesyon saptanmaları 53 Herhangi bir örnekten elde edilen DNA ve RNA’ ya uygulanabilir. Klinik araştırmaları kolaylaştırmakta ve hızlandırmaktadır; örneğin Alzheimer hastalığı, otoimmün hastalıklar, koroner arter hastalığı, diabet vb… 54 Mikrobiyoloji açısından faydaları Mikrobiyal sekansı 1 saat içinde yapabilmektedir. Gerçek DNA sekans verilerinin klinik olarak uygun bir süre içinde elde edilmesi, Tür tanımlaması ve direnç karakterizasyonunun tek bir sistem içinde yapılabilmesi, Multi-kopya (çok kopyalı) genlerin miktar tayinleri-antibiyotik direnç tanımlaması, viral ve fungal yük ölçülebilir. 55 MİKROBİYOLOJİDE DİZİ ANALİZİ Mikrorganizmaların tanımlanması veya sınıflamadaki yerlerinin belirlenmesi Salgınlara yol açan etkenlerin belirlenmesi İlaç direncinin belirlenmesi Mikroorganizmadaki virülans, metabolik enzimler ve düzenleyici genlerin moleküler seviyede incelenmesi Genotiplerin belirlenmesi Mutant suşların belirlenmesi 56 KAYNAKLAR Uygulamalı moleküler mikrobiyoloji, Prof. Dr. Rıza Durmaz Klinik mikrobiyolojide pyrosekans kursu, Kurs özet kitabı 57 teşekkürler