TEOG Püf Noktalar Maddenin Hâlleri ve Isı mcDt = mcDt
advertisement
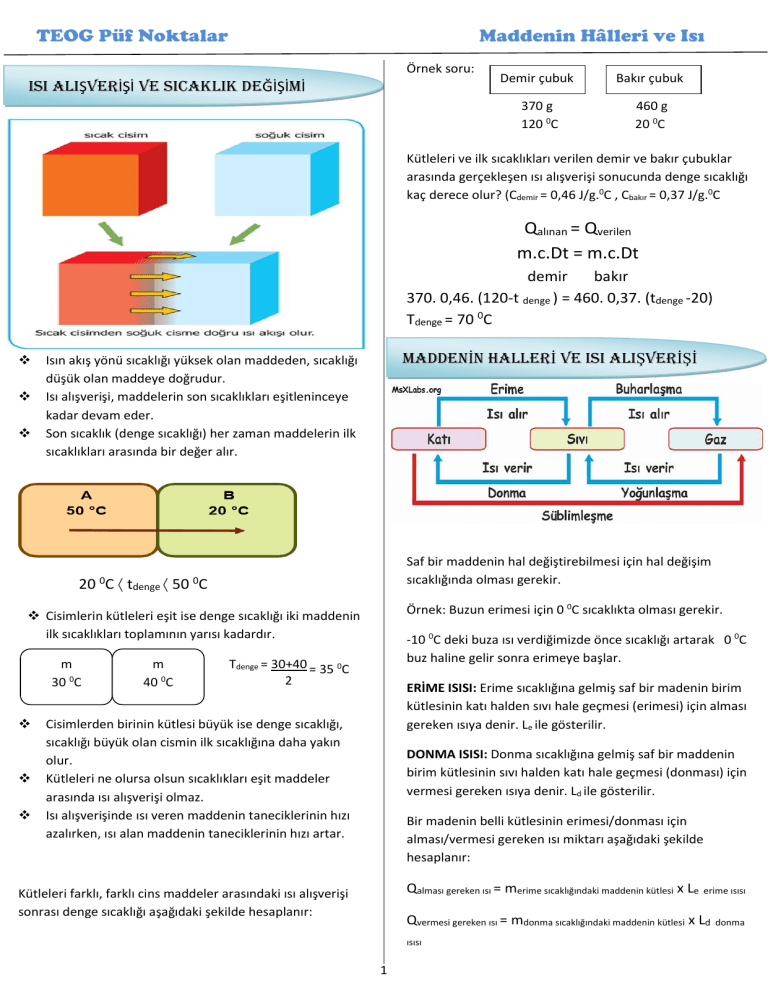
TEOG Püf Noktalar Maddenin Hâlleri ve Isı Örnek soru: ISI ALIŞVERİŞİ VE SICAKLIK DEĞİŞİMİ Demir çubuk Bakır çubuk 370 g 120 0C 460 g 20 0C Kütleleri ve ilk sıcaklıkları verilen demir ve bakır çubuklar arasında gerçekleşen ısı alışverişi sonucunda denge sıcaklığı kaç derece olur? (Cdemir = 0,46 J/g.0C , Cbakır = 0,37 J/g.0C Qalınan = Qverilen m.c.Dt = m.c.Dt demir bakır 370. 0,46. (120-t denge ) = 460. 0,37. (tdenge -20) Tdenge = 70 0C MADDENİN HALLERİ VE ISI ALIŞVERİŞİ Isın akış yönü sıcaklığı yüksek olan maddeden, sıcaklığı düşük olan maddeye doğrudur. Isı alışverişi, maddelerin son sıcaklıkları eşitleninceye kadar devam eder. Son sıcaklık (denge sıcaklığı) her zaman maddelerin ilk sıcaklıkları arasında bir değer alır. Saf bir maddenin hal değiştirebilmesi için hal değişim sıcaklığında olması gerekir. 20 0C tdenge 50 0C Örnek: Buzun erimesi için 0 0C sıcaklıkta olması gerekir. Cisimlerin kütleleri eşit ise denge sıcaklığı iki maddenin ilk sıcaklıkları toplamının yarısı kadardır. m 30 0C m 40 0C -10 0C deki buza ısı verdiğimizde önce sıcaklığı artarak 0 0C buz haline gelir sonra erimeye başlar. Tdenge = 30+40 = 35 0C 2 ERİME ISISI: Erime sıcaklığına gelmiş saf bir madenin birim kütlesinin katı halden sıvı hale geçmesi (erimesi) için alması gereken ısıya denir. Le ile gösterilir. Cisimlerden birinin kütlesi büyük ise denge sıcaklığı, sıcaklığı büyük olan cismin ilk sıcaklığına daha yakın olur. Kütleleri ne olursa olsun sıcaklıkları eşit maddeler arasında ısı alışverişi olmaz. Isı alışverişinde ısı veren maddenin taneciklerinin hızı azalırken, ısı alan maddenin taneciklerinin hızı artar. DONMA ISISI: Donma sıcaklığına gelmiş saf bir maddenin birim kütlesinin sıvı halden katı hale geçmesi (donması) için vermesi gereken ısıya denir. Ld ile gösterilir. Bir madenin belli kütlesinin erimesi/donması için alması/vermesi gereken ısı miktarı aşağıdaki şekilde hesaplanır: Qalması gereken ısı = merime sıcaklığındaki maddenin kütlesi x Le erime ısısı Kütleleri farklı, farklı cins maddeler arasındaki ısı alışverişi sonrası denge sıcaklığı aşağıdaki şekilde hesaplanır: Qvermesi gereken ısı = mdonma sıcaklığındaki maddenin kütlesi x Ld ısısı 1 donma HAL DEĞİŞİM GRAFİKLERİ Suyun Isınma Grafiği BUHARLAŞMA ISISI: Kaynama sıcaklığına gelmiş saf bir madenin birim kütlesinin sıvı halden gaz hale geçmesi (buharlaşması) için alması gereken ısıya denir. Lb ile gösterilir. Suyun Soğuma Grafiği YOĞUNLAŞMA ISISI: Yoğunlaşma sıcaklığına gelmiş saf bir maddenin birim kütlesinin gaz halden sıvı hale geçmesi (yoğunlaşması) için vermesi gereken ısıya denir. Ly ile gösterilir. Qalması gereken ısı = mkaynama sıcaklığındaki maddenin kütlesi x Lb buharlaşma ısısı Qvermesi gereken ısı = myoğunlaşma sıcaklığındaki maddenin kütlesix Ly Saf maddeler hal değiştirirken sıcaklıkları sabit kalır. Çünkü aldıkları ısının tamamını hal değiştirmek için kullanırlar. yoğunlaşma ısısı GÜNLÜK HAYATTA HAL DEĞİŞİMİ VE ISI ALIŞVERİŞİ Günlük hayatta birçok olayda ısı alışverişi ve hal değişimi Günlük hayatta birçok olayda ısı alışverişi ve hal değişimi olayları ile karşılaşırız. olayları ile ka Örnek olarak buzdolabına konulan içeceklerin soğuması, dondurmanın sıcak havada erimesi, elimizde buz tuttuğumuzda elimizin soğuması, sıcak bir kahve veya çayın beklediğinde soğuması, kolanın içine buz attığımızda soğuması, ateşin etrafındaki havayı ısıtması, sıcak bir yemeğin içinde tuttuğumuz metal kaşığın ısınması, ütü yaptığımız kıyafetlerin ısınması verilebilir. Saf maddeler için ayırt edici özelliklerdir. Saf maddelerin erime ısısı= donma ısısı, buharlaşma ısısı= yoğunlaşma ısısı Örnek: 0 0C deki suyun donması için vermesi gereken ısı= 0 0C buzun erimesi için alması gereken ısı Ayrıca güneşte bırakılan karpuzun ısınması ve toprak testideki suyun soğuk olması ısı alışverişi ile açıklanır. Betül ŞAHİN 2












